安徽省马鞍山市花山区2023年中考一模化学试题
试卷更新日期:2023-04-07 类型:中考模拟
一、单选题
-
1. 从化学的角度对下列成语进行解释,其中错误的是( )A、点石成金——化学反应能改变元素种类 B、钻木取火——温度达到可燃物的着火点 C、釜底抽薪——燃烧的条件之一是需要可燃物 D、烈火真金——金在高温下难与其它物质反应2. 我国科学家最新研制出一种新型石墨烯-铝电池,手机使用这种电池,充电时间短,待机时间长。碳、铝元素的相关信息如图,有关说法正确的是( )
 A、它们的化学性质相同 B、碳在地壳中含量最高 C、铝的原子序数为13 D、铝的相对原子质量为26.98g3. 下列实验操作正确的是( )A、
A、它们的化学性质相同 B、碳在地壳中含量最高 C、铝的原子序数为13 D、铝的相对原子质量为26.98g3. 下列实验操作正确的是( )A、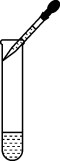 滴加液体
B、
滴加液体
B、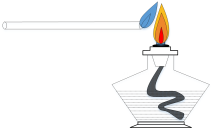 点燃酒精灯
C、
点燃酒精灯
C、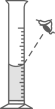 量取液体
D、
量取液体
D、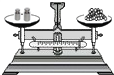 称量固体
4. “宏观-微观-符号”三重表征是化学独特的表示物质及其变化的方法。如图是液化石油气成分之一燃烧前后分子种类变化的微观示意图,下列说法错误的是( )
称量固体
4. “宏观-微观-符号”三重表征是化学独特的表示物质及其变化的方法。如图是液化石油气成分之一燃烧前后分子种类变化的微观示意图,下列说法错误的是( ) A、生成丙与丁物质的质量比为11:6 B、该反应不属于置换反应 C、甲物质的一个分子是由3个碳原子和8个氢原子构成的 D、该反应前后,分子的个数没有改变5. 分类是学习和研究化学常用的方法。下列物质分类正确的是( )A、金属元素:硒、碘、锌 B、氧化物:干冰、生石灰、石灰石 C、合金:生铁、黄铜、不锈钢 D、化石燃料:煤、石油、氢气6. 已知相同条件下(同温、同压),理想气体的分子个数比等于气体的体积比。那么相同体积的甲烷和氢气完全燃烧所需的氧气体积比为(以上均为理想气体)( )A、2:1 B、1:2 C、4:1 D、1:47. 为及时发现家用天然气的泄漏,常在天然气中加入少量具有特殊气味的乙硫醇(C2H5SH)。下列有关乙硫醇的说法正确的是A、乙硫醇由四种元素组成 B、乙硫醇中含有9个原子 C、乙硫醇中碳元素的质量分数最大 D、乙硫醇中碳、氢元素的质量比为4:18. 为探究硝酸钾的溶解性,进行了如图所示实验,结合硝酸钾在不同温度下的溶解度,判断下列说法错误的是( )
A、生成丙与丁物质的质量比为11:6 B、该反应不属于置换反应 C、甲物质的一个分子是由3个碳原子和8个氢原子构成的 D、该反应前后,分子的个数没有改变5. 分类是学习和研究化学常用的方法。下列物质分类正确的是( )A、金属元素:硒、碘、锌 B、氧化物:干冰、生石灰、石灰石 C、合金:生铁、黄铜、不锈钢 D、化石燃料:煤、石油、氢气6. 已知相同条件下(同温、同压),理想气体的分子个数比等于气体的体积比。那么相同体积的甲烷和氢气完全燃烧所需的氧气体积比为(以上均为理想气体)( )A、2:1 B、1:2 C、4:1 D、1:47. 为及时发现家用天然气的泄漏,常在天然气中加入少量具有特殊气味的乙硫醇(C2H5SH)。下列有关乙硫醇的说法正确的是A、乙硫醇由四种元素组成 B、乙硫醇中含有9个原子 C、乙硫醇中碳元素的质量分数最大 D、乙硫醇中碳、氢元素的质量比为4:18. 为探究硝酸钾的溶解性,进行了如图所示实验,结合硝酸钾在不同温度下的溶解度,判断下列说法错误的是( )
温度/℃
10
20
30
40
50
60
KNO3溶解度/g
20.9
31.6
45.8
63.9
85.5
110.0
A、①③中的溶液均为不饱和溶液 B、②③中溶液的质量:③>② C、②③④中溶液的溶质质量分数:③>②>④ D、④中析出晶体的质量是9.9 g9. 科学家用单个分子制成了“纳米车”,它能在人工操纵下运输药物分子到病源处释放以杀死癌细胞。下列有关“纳米车”的说法错误的是( )A、“纳米车”的研制成功说明人类任应用分子上的又一次进步 B、“纳米车”分子不是由原子构成的 C、“纳米车”运输药物分子的过程是肉眼看不见的 D、“纳米车”研制成功说明在一定条件下人可以控制分子运动10. 某容器中含有若干个分子,每个分子都是由两个原子构成的,则该容器内的物质是( )A、单质 B、化合物 C、单质或化合物 D、单质或化合物或混合物11. 学习化学,提高学科核心素养,学会从化学的角度分析问题。下列说法正确的是( )A、铁生锈会导致铁制品全部被腐蚀,铝比铁活泼,因此铝在空气中也会全部被腐蚀 B、可燃物燃烧温度需要达到其着火点,因此降低温度至可燃物着火点以下可灭火 C、进入山洞前要进行灯火试验,因此进入地下煤矿前也要进行灯火试验 D、化学反应元素守恒,因此有氧元素参加的反应,生成物中一定有氧气12. 如图为教材中探究金属活动性顺序的实验,下列有关说法错误的是( ) A、使用未打磨的铝丝进行实验能得到相同的实验现象 B、省略丙实验也能比较Al、Cu、Ag三种金属的活动性 C、甲实验中溶液颜色逐渐变浅至无色 D、实验结束后,乙中溶液的质量减小
A、使用未打磨的铝丝进行实验能得到相同的实验现象 B、省略丙实验也能比较Al、Cu、Ag三种金属的活动性 C、甲实验中溶液颜色逐渐变浅至无色 D、实验结束后,乙中溶液的质量减小二、科普阅读题
-
13. 阅读下面的短文,回答有关问题。
目前,新冠肺炎疫情肆虐全球。为抑制新冠病毒传播,“含氯消毒剂”被广泛使用,其中就包含一种新型灭菌消毒剂﹣﹣ClO2。①在通常情况下,ClO2是一种有刺激性气味的黄绿色气体,②熔点﹣59℃,沸点11℃;③在常温下,1L水中大约能溶解2.9g ClO2;④ClO2受热或者见光易分解,具有强氧化性和很强的腐蚀性,⑤是一种安全,绿色的消毒剂。
(1)、上述材料中属于ClO2的物理性质有(填序号,下同) , 属于ClO2的化学性质有。(2)、下列有关ClO2的说法正确的是____(填字母序号)。A、0℃时,ClO2为黄绿色气体 B、常温下,100mL水中大约能溶解0.29g ClO2 C、用棕色试剂瓶盛装ClO2并置于冷暗处保存 D、ClO2可以代替有毒有害消毒剂(3)、ClO2遇热水生成次氯酸(HClO),氯气(Cl2)和氧气。请写出ClO2与热水反应的符号表达式。三、综合题
-
14. 黄铜渣中约含Zn7%、ZnO31%、Cu50%、CuO5%,其余为杂质。某工厂处理黄铜渣可得到硫酸锌晶体,其主要流程如图。(杂质不溶于水,不参与反应)
已知: ,
 (1)、步骤I中产生气体的化学方程式是。(2)、步骤Ⅱ的操作名称是。(3)、溶液A中的阳离子有(填离子符号);(4)、固体B是(填“纯净物”或“混合物”);(5)、溶液A的质量(填“>”“<”或“=”)溶液C的质量。15. 根据下图完成填空:
(1)、步骤I中产生气体的化学方程式是。(2)、步骤Ⅱ的操作名称是。(3)、溶液A中的阳离子有(填离子符号);(4)、固体B是(填“纯净物”或“混合物”);(5)、溶液A的质量(填“>”“<”或“=”)溶液C的质量。15. 根据下图完成填空: (1)、实验室可用如图装置A制CO2 , 反应的化学方程式是。(2)、装置B和C均可以收集CO2 , 若用B收集则气体应从端(选填“b”或“c”)通入;若用C装置收集,植物油的作用是。(3)、发生装置A用于制取CO2的最大优点是。16. 小明在网上查到一个趣味小实验,用蜡烛测氧气含量可以得到氧气约占空气体积1/5的结论。
(1)、实验室可用如图装置A制CO2 , 反应的化学方程式是。(2)、装置B和C均可以收集CO2 , 若用B收集则气体应从端(选填“b”或“c”)通入;若用C装置收集,植物油的作用是。(3)、发生装置A用于制取CO2的最大优点是。16. 小明在网上查到一个趣味小实验,用蜡烛测氧气含量可以得到氧气约占空气体积1/5的结论。【提出问题】
(1)、小明认为:蜡烛含有碳、氢两种元素,充分燃烧会生成二氧化碳和水,实验结果应该是氧气体积(大于/小于/等于)空气体积的1/5。带着这个疑问,小明按网上的方法进行了如下探究:
(2)、【实验探究1】如图1,在盛有足量水的容器中放一根燃着的蜡烛,然后用盛满空气的玻璃圆筒倒扣住蜡烛。
【现象】
一开始蜡烛继续燃烧,稍后水中冒出几个气泡,然后逐渐熄火,圆筒内液面逐渐上升,最终停留在等分线4处。请你解释进入约1/5体积的水的原因。
(3)、【实验探究2】小明利用课本中红磷测氧气含量的实验装置(气密性良好)继续探究:把红磷换成蜡烛,瓶中水换成足量澄清石灰水。在蜡烛熄灭后打开弹簧夹前,还振荡了瓶中的石灰水,进行这项操作的原因是;写出该操作时发生反应的化学方程式。打开弹簧夹后发现水只进入了约1/10体积。
 (4)、【反思评价】水为何只进入了约1/10体积?
(4)、【反思评价】水为何只进入了约1/10体积?【实验探究3】
小明又继续探究瓶内剩余气体的成分。把点燃的红磷伸入集气瓶内,发现红磷没有立即熄灭,而是燃烧一段时间后再熄灭,同时生成了白色固体物质。
结论:蜡烛燃烧熄灭后剩余气体中含有。
(5)、【交流小结】请依据以上探究分析蜡烛能否测定氧气含量?。(6)、【拓展探究】小明继续对红磷熄灭后的剩余气体进行探究,把点燃的镁条伸入集气瓶内,发现镁条仍然能继续燃烧一段时间,发出黄光同时生成了黄色固体物质。小明猜测黄色固体物质不是镁与氧气反应的生成物,而是与氮气反应的生成物,理由。
(7)、经分析,黄色固体物质是镁与氮气反应生成的氮化镁,已知36g镁在氮气中完全反应可以得到50g氮化镁,求氮化镁的化学式为。(8)、已知:氮化镁可以与水在常温下发生剧烈反应,生成氢氧化镁和一种具有刺激性的气体,请写出该反应的化学方程式。四、计算题
-
17. 现有氯酸钾和二氧化锰的混合物15.5g。加热至不再反应为止,冷却后称得固体质量为10.7g。(1)、产生氧气的质量为。(2)、求混合物中氯酸钾的质量。
-