河南省周口市商水县2023年中考一模化学试题
试卷更新日期:2023-04-03 类型:中考模拟
一、单选题
-
1. 《中国诗词大会》弘扬了中国传统文化。下列诗句反映的物质变化主要为化学变化的是( )A、吹尽狂沙始到金 B、烈火焚烧若等闲 C、花气袭人知骤暖 D、无边落木萧萧下2. 下列材料中,属于有机合成材料的是( )A、棉花 B、腈纶 C、羊毛 D、蚕丝3. 关于Na、Na2O2、Na+和Na2SO4的说法正确的是( )A、都含有钠元素 B、Na2O2中含有氧分子 C、Na和Na+的质子数不同 D、Na2SO4由Na2SO4离子构成4. 2022年我国在抗击新冠肺炎战役中取得了阶段性重大成果,为防控疫情,通常在公共场所使用84消毒液(主要成分是NaClO)进行消毒,NaClO中氯元素的化合价是( )A、+1 B、+5 C、+4 D、05. 下列实验现象描述正确的是( )A、将光亮的铜丝插入稀盐酸中,有气泡产生 B、铁丝在空气中剧烈燃烧,火星四射 C、硫在氧气中燃烧,发出蓝紫色火焰 D、碳在氧气中燃烧发红光,生成二氧化碳6. 根据不同的分类标准,我们可以将同一化学反应分为不同的类别。下列反应中,既属于化合反应又属于氧化反应的是( )A、酒精+氧气水+二氧化碳 B、碳酸→水+二氧化碳 C、氧化钙+水→氢氧化钙 D、磷+氧气五氧化二磷7. 稀释浓硫酸并进行硫酸性质实验的下列操作,正确的是( )A、
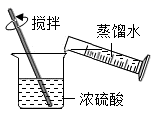 稀释浓硫酸
B、
稀释浓硫酸
B、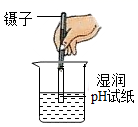 测稀硫酸的pH
C、
测稀硫酸的pH
C、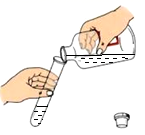 倾倒稀硫酸
D、
倾倒稀硫酸
D、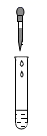 滴加稀硫酸
8. 2022年我国纪念“世界水日”“中国水周”活动主题为“推进地下水超采综合治理 复苏河湖生态环境”。下列关于水的说法中正确的是( )A、大量开采地下水缓解水资源紧张 B、为防止水污染禁止施用农药和化肥 C、城市污水必须经过净化处理后才能排放 D、地下水必须经过沉淀、过滤、消毒、蒸馏后方可饮用9. 在一密闭容器中放入X、Y、Z、W四种物质,在一定条件下发生化学反应,一段时间后,测得有关数据如下表,则关于此反应的认识正确的是( )
滴加稀硫酸
8. 2022年我国纪念“世界水日”“中国水周”活动主题为“推进地下水超采综合治理 复苏河湖生态环境”。下列关于水的说法中正确的是( )A、大量开采地下水缓解水资源紧张 B、为防止水污染禁止施用农药和化肥 C、城市污水必须经过净化处理后才能排放 D、地下水必须经过沉淀、过滤、消毒、蒸馏后方可饮用9. 在一密闭容器中放入X、Y、Z、W四种物质,在一定条件下发生化学反应,一段时间后,测得有关数据如下表,则关于此反应的认识正确的是( )物质
X
Y
Z
W
反应前质量/g
20
2
1
37
反应后质量/g
15
32
1
a
A、Y一定是反应物 B、a=12 C、Z一定是该反应的催化剂 D、参加反应的X、W的质量比为5∶410. 硝酸钾、氯化钠的溶解度曲线如图所示,下列说法正确的是( ) A、除去硝酸钾中少量的氯化钠可采用溶解、蒸发结晶、过滤方法 B、40℃时,100g硝酸钾饱和溶液中含有硝酸钾63.9g C、将硝酸钾溶液由40℃降温至20℃,一定有硝酸钾晶体析出 D、t℃时,硝酸钾和氯化钠的饱和溶液的溶质质量分数一定相等11. 实验室加热固体制取氧气的过程中有以下几个步骤:①点燃酒精灯,加热试管;②熄灭酒精灯;③检查装置气密性;④装入药品,固定试管;⑤用排水法收集氧气;⑥将导管移出水面。选择出正确的操作以及顺序是( )A、③④①⑤⑥② B、③④①⑤②⑥ C、④③①⑤⑥② D、④③①⑤②⑥12. 下列有关物质的性质与用途具有对应关系的是( )A、一氧化碳具有可燃性,可用于工业炼铁 B、酒精具有挥发性,可用于杀菌消毒 C、石墨质软,可作电池电极材料 D、浓硫酸具有吸水性,可用作干燥剂13. 如下图所示的四个图像,不能正确反映对应变化关系的是( )
A、除去硝酸钾中少量的氯化钠可采用溶解、蒸发结晶、过滤方法 B、40℃时,100g硝酸钾饱和溶液中含有硝酸钾63.9g C、将硝酸钾溶液由40℃降温至20℃,一定有硝酸钾晶体析出 D、t℃时,硝酸钾和氯化钠的饱和溶液的溶质质量分数一定相等11. 实验室加热固体制取氧气的过程中有以下几个步骤:①点燃酒精灯,加热试管;②熄灭酒精灯;③检查装置气密性;④装入药品,固定试管;⑤用排水法收集氧气;⑥将导管移出水面。选择出正确的操作以及顺序是( )A、③④①⑤⑥② B、③④①⑤②⑥ C、④③①⑤⑥② D、④③①⑤②⑥12. 下列有关物质的性质与用途具有对应关系的是( )A、一氧化碳具有可燃性,可用于工业炼铁 B、酒精具有挥发性,可用于杀菌消毒 C、石墨质软,可作电池电极材料 D、浓硫酸具有吸水性,可用作干燥剂13. 如下图所示的四个图像,不能正确反映对应变化关系的是( ) A、①KMnO4受热分解 B、②在密闭容器中用足量铜粉测定空气中氧气的含量 C、③向等质量的镁粉和锌粉中分别加入足量稀硫酸 D、④一定温度下,向饱和的氯化钠溶液中加入氯化钠固体并搅拌14. 某同学欲测定K2CO3和Na2CO3固体混合物中金属元素的质量分数,取1.20g样品于烧杯中,加水充分溶解,再加入足量的BaCl2溶液,充分反应后生成1.97g白色沉淀。样品中金属元素的质量分数为( )A、50% B、55% C、45% D、60%
A、①KMnO4受热分解 B、②在密闭容器中用足量铜粉测定空气中氧气的含量 C、③向等质量的镁粉和锌粉中分别加入足量稀硫酸 D、④一定温度下,向饱和的氯化钠溶液中加入氯化钠固体并搅拌14. 某同学欲测定K2CO3和Na2CO3固体混合物中金属元素的质量分数,取1.20g样品于烧杯中,加水充分溶解,再加入足量的BaCl2溶液,充分反应后生成1.97g白色沉淀。样品中金属元素的质量分数为( )A、50% B、55% C、45% D、60%二、填空
-
15. 地壳中含量最高的金属元素与非金属元素形成的化合物的化学式为;空气中含量最高且常用于食品防腐的气体是。16. “侯氏制碱法”是我国化学家发明的一种制取纯碱的方法,其中重要的一步化学方程式是。下一步制取纯碱的化学方程式是。17. 酸碱盐是初中化学重要的内容。

如图甲是氢氧化钠和硫酸反应的微观示意图,从图中可知,酸碱中和反应的实质是;写出该反应的化学方程式 , 此反应的基本类型为。
18. 粗盐中含有难溶性杂质(泥沙等)和多种可溶性杂质(氯化镁、氯化钙)等。某班同学在粗盐提纯实验中,为把少量可溶性杂质CaCl2、MgCl2一并除去,将教材中实验方案修改设计如图所示,请据此回答问题。
操作A和操作B都用到一个玻璃仪器的名字是;溶液b中的溶质有;加过量稀盐酸的目的是(用化学方程式表示,写一个即可)。
19. 波尔多液广泛用于蔬菜、果树等的虫害防治,是由硫酸铜溶液和石灰乳按一定比例混合而成的保护性杀菌剂,请回答:(1)、配制过程中不能用铁制容器,原因是(用化学方程式表示)。(2)、喷洒波尔多液后,不到采摘期的蔬果表面有一些蓝色斑点(一种难溶性碱),蓝色斑点的成分是(填化学式),不易用水清洗,可用厨房中的调味剂浸泡洗去。20. A~D是含有同一种元素的常见物质。它们的转化关系如图所示(“→”表示反应一步实现,部分物质和反应条件已略去),图中标注了物质类别和这种元素的化合价。已知D的相对分子质量为100。 (1)、C物质的用途为;(2)、B、C化学性质不同的原因是;(3)、C、D可以相互转化,写出C→D的化学方程式。
(1)、C物质的用途为;(2)、B、C化学性质不同的原因是;(3)、C、D可以相互转化,写出C→D的化学方程式。三、简答题
-
21. 请从微观角度解释下列问题(1)、蔗糖在热水中比在冷水中溶解得快。(2)、石墨和C60都是由碳元素组成的单质,但物理性质却存在着明显差异。22. 在化学实验操作中,一定要注意实验的安全。(1)、点燃氢气前一定要进行什么操作?(2)、铁丝在氧气中燃烧实验时,在集气瓶中放少量水。写出反应的化学方程式。23. 如下图是配制80克质量分数为10%的氯化钠溶液的操作过程示意图。试回答:
 (1)、B操作中应称量氯化钠的质量是 , 放好砝码和游码后,向托盘中加入氯化钠过程中,若指针偏向分度盘的左边,应进行的操作是。(2)、D操作应选用的量筒(从10mL、100mL中选择),量水时量筒必须平放,视线要与量筒凹液面的处保持水平。(3)、E操作的作用是。24. 某化学学习小组欲除去KCl晶体中的杂质MgSO4和CaCl2得到纯净的KCl晶体。设计主要实验步骤有:①加水溶解;②依次加入过量的Ba(OH)2溶液和K2CO3溶液:③过滤;④加入适量的稀盐酸:⑤蒸发结晶。(1)、写出加入过量Ba(OH)2溶液时发生反应的化学方程式。(2)、写出蒸发过程中玻璃棒的作用。(3)、上述步骤中,若将步骤③和④的顺序顺倒,所得KCl晶体中含有哪些杂质?
(1)、B操作中应称量氯化钠的质量是 , 放好砝码和游码后,向托盘中加入氯化钠过程中,若指针偏向分度盘的左边,应进行的操作是。(2)、D操作应选用的量筒(从10mL、100mL中选择),量水时量筒必须平放,视线要与量筒凹液面的处保持水平。(3)、E操作的作用是。24. 某化学学习小组欲除去KCl晶体中的杂质MgSO4和CaCl2得到纯净的KCl晶体。设计主要实验步骤有:①加水溶解;②依次加入过量的Ba(OH)2溶液和K2CO3溶液:③过滤;④加入适量的稀盐酸:⑤蒸发结晶。(1)、写出加入过量Ba(OH)2溶液时发生反应的化学方程式。(2)、写出蒸发过程中玻璃棒的作用。(3)、上述步骤中,若将步骤③和④的顺序顺倒,所得KCl晶体中含有哪些杂质?四、综合题
-
25. 酸、碱、盐在生活、生产中有着广泛的应用。(1)、在实验室中常用浓硫酸作干燥剂,是利用了浓硫酸的(填字母)。
a.腐蚀性 b.吸水性 c.氧化性 d.酸性
(2)、用稀盐酸除铁锈的化学方程式为 。(3)、如图1所示,向充满CO2气体的烧瓶中,注入100mL饱和氢氧化钠溶液,关闭活塞;连接压强传感器,观察到烧瓶内气压变化图像如图2所示。
①用文字描述烧瓶内压强减小的原因:。
②如何确定反应后烧瓶中溶液是否还含有NaOH:。(请叙述操作、现象、结论)
(4)、从海水得到的粗盐中往往含有泥沙和氯化钙、氯化镁、硫酸钠等杂质,某化学兴趣小组取少量粗盐样品在实验室进行了如下实验:
①操作②中用到的玻璃仪器有玻璃棒、、烧杯。
②按照上图所示实验流程,加入过量的碳酸钠的目的是:。
③写出加入稀盐酸后所发生的反应的化学方程式:。(写出一个即可)
(5)、食用碱的主要成分是碳酸钠,其中含少量氯化钠。取一定质量某品牌食用碱样品投入烧杯中,加入足量的水,搅拌后加入200g溶质质量分数为11.1%的氯化钙溶液,二者恰好完全反应,则该品牌食用碱样品中碳酸钠的质量为多少?