广东省佛山市南海区2023年中考一模化学试题
试卷更新日期:2023-04-03 类型:中考模拟
一、单选题
-
1. 下列物质的用途,主要利用其化学性质的是( )A、
 石墨做电刷
B、
石墨做电刷
B、 氧气用于气割
C、
氧气用于气割
C、 洗涤剂的乳化作用
D、
洗涤剂的乳化作用
D、 干冰用于舞台艺术
2. 掌握化学用语是学好化学的关键。下列化学用语表述正确的是( )A、碳酸钾的化学式:KCO3 B、铜离子:Cu2+ C、+2价的钙元素:Ca+2 D、一个氮分子:N3. 下列标志属于物品回收标志的是( )A、
干冰用于舞台艺术
2. 掌握化学用语是学好化学的关键。下列化学用语表述正确的是( )A、碳酸钾的化学式:KCO3 B、铜离子:Cu2+ C、+2价的钙元素:Ca+2 D、一个氮分子:N3. 下列标志属于物品回收标志的是( )A、 B、
B、 C、
C、 D、
D、 4. 元素周期表是学习和研究化学的重要工具,如图是元素周期表中的一部分。下列说法正确的是( )
4. 元素周期表是学习和研究化学的重要工具,如图是元素周期表中的一部分。下列说法正确的是( ) A、相对原子质量:钙>钪 B、镁原子和钪原子最外层都是2个电子,化学性质相似 C、最外层电子数:镁>钠 D、镁和钙最外层电子数相同,处于同一周期5. 以下实验基本操作正确的是( )
A、相对原子质量:钙>钪 B、镁原子和钪原子最外层都是2个电子,化学性质相似 C、最外层电子数:镁>钠 D、镁和钙最外层电子数相同,处于同一周期5. 以下实验基本操作正确的是( )


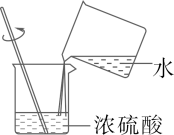
A.加热液体
B.测定溶液pH
C.称量固体
D.稀释浓硫酸
A、A B、B C、C D、D6. 下列叙述正确的是( )A、霉变的大米洗净烧熟后可以食用 B、焊锡、18K黄金、不锈钢、氧化铁都是生活中常见的合金 C、使用乙醇汽油能减少污染,节约石油资源 D、钙、铁、锌、碘是人体所需的微量元素7. 纳米铁粉在空气中不易自燃,但稍加热即可剧烈燃烧,如图是纳米铁粉在锥形瓶中燃烧的实验。下列说法错误的是( ) A、纳米铁粉燃烧的化学方程式为3Fe+2O2
A、纳米铁粉燃烧的化学方程式为3Fe+2O2 Fe3O4
B、水可防止生成物溅落炸裂瓶底
C、激光手电照射使纳米铁粉的着火点降低
D、气球先膨胀后又变小
8. “新冠病毒”正严重威胁人类健康佩戴N95口罩可以有效阻断病毒。口罩中的熔喷布是以聚丙烯(C3H6)n为主要原料制成的过滤材质,铝塑条是在塑料表面涂上一层铝。下列有关说法正确的是( )
Fe3O4
B、水可防止生成物溅落炸裂瓶底
C、激光手电照射使纳米铁粉的着火点降低
D、气球先膨胀后又变小
8. “新冠病毒”正严重威胁人类健康佩戴N95口罩可以有效阻断病毒。口罩中的熔喷布是以聚丙烯(C3H6)n为主要原料制成的过滤材质,铝塑条是在塑料表面涂上一层铝。下列有关说法正确的是( ) A、铝塑条属于合金材料 B、聚丙烯属于有机高分子材料 C、“N95”口罩对病毒的阻断原理与臭氧的消毒杀菌原理相同 D、废弃口罩应密封好,放入“有害垃圾”桶内9. 下列根据实验操作所得出的现象和结论均正确的是( )
A、铝塑条属于合金材料 B、聚丙烯属于有机高分子材料 C、“N95”口罩对病毒的阻断原理与臭氧的消毒杀菌原理相同 D、废弃口罩应密封好,放入“有害垃圾”桶内9. 下列根据实验操作所得出的现象和结论均正确的是( )选项
实验操作
实验现象
结论
A
将活性炭加入红棕色NO2气体中
红棕色消失
活性炭与NO2发生化学反应
B
向紫色石蕊溶液中通入CO2气体
溶液变成红色
不能说明CO2与水反应
C
在CuSO4溶液中插入锌片和铁片
锌片和铁片表面均出现红色固体
金属的活动性:锌>铁>铜
D
向H2O2溶液中加入少量CuO粉末
产生大量气泡
CuO是该反应的催化剂
A、A B、B C、C D、D10. 一定条件下,在一个密闭容器内发生某反应,测得反应前后各物质的质量如图所示:
下列说法正确的是( )
A、x的值为36 B、该反应属于化合反应 C、W由碳、氢两种元素组成 D、W中碳、氢元素质量比为1︰311. 下列实验设计不能达到实验目的的是( )选项
A
B
C
D
实验设计




实验目的
实验探究二氧化碳能与水反应
探究燃烧所需要的条件
验证NH4NO3溶于水吸热
证明CO2与NaOH反应
A、A B、B C、C D、D12. 下列除杂方法正确的是( )A、用过滤的方法除去NaCl中的KNO3 B、CO中混有少量CO2 , 要得到干燥纯净的CO方法:通过足量的NaOH溶液 C、用浓硫酸除去CO气体中的水蒸气 D、要除去MnO2中混有少量的NaCl,方法:加水溶解后过滤13. NSR技术通过BaO和Ba(NO3)2的相互转化实现NOx(氮氧化物)的储存和还原,能有效降低柴油发动机在空气过量条件下的NOx排放。其工作原理如图所示。下列说法正确的是( ) A、BaO、Ba(NO3)2都属于金属氧化物 B、该技术不能缓解酸雨的形成 C、该转化中有两种元素化合价发生改变 D、还原反应: , 则X的化学式为CO214. 甲、乙的溶解度曲线如图所示。下列说法正确的是( )
A、BaO、Ba(NO3)2都属于金属氧化物 B、该技术不能缓解酸雨的形成 C、该转化中有两种元素化合价发生改变 D、还原反应: , 则X的化学式为CO214. 甲、乙的溶解度曲线如图所示。下列说法正确的是( ) A、甲的溶解度随温度升高而减小 B、t2℃时,甲、乙的饱和溶液溶质质量分数大小顺序为:乙>甲 C、加入溶质甲可以将d点甲溶液移至c点,且溶质质量分数增大 D、甲、乙饱和溶液从t2升温到t3 , 仍为饱和溶液15. 下列图像与其对应描述相符的是( )
A、甲的溶解度随温度升高而减小 B、t2℃时,甲、乙的饱和溶液溶质质量分数大小顺序为:乙>甲 C、加入溶质甲可以将d点甲溶液移至c点,且溶质质量分数增大 D、甲、乙饱和溶液从t2升温到t3 , 仍为饱和溶液15. 下列图像与其对应描述相符的是( )

A.氢氧化钠溶液加水稀释
B.把NaOH和NH4NO3固体分别溶于水


C.向一定量的硝酸银溶液中插入铜
D.红磷在盛有一定量空气的密闭容器中燃烧至熄灭
A、A B、B C、C D、D二、填空题
-
16. 近几年,新能源汽车在全球范围内都呈飞速发展态势,中国市场已经跃升为最大的新能源汽车市场,新能源汽车的研发和使用是时代发展的需要。请回答;(1)、目前人们利用最多的化石燃料是煤、天然气和。煤燃烧产生(填化学式)气体会形成酸雨。(2)、如图是类典型的新能源车,其外部车身体板采用碳纤维材料构造,底盘由模压铝合金构成,铝合金属于材料,推测车身体板和底盘共同具有的一个物理性质是。(填字母)

A硬度大 B熔点低 C密度大
(3)、在电动车行驶的过程中,储存在锂离子电池中的能转化为电能。(4)、电池可为新能源汽车提供动力。下列结构示意图表示的粒子与锂原子的化学性质最为相似的是(填微粒符号)。 (5)、新能源汽车除了节约化石燃料外,其主要优点是。17.(1)、类价二维图反映的是元素的化合价与物质类别之间的关系。如图是某同学绘制的关于碳元素的类价二维图。请回答:
(5)、新能源汽车除了节约化石燃料外,其主要优点是。17.(1)、类价二维图反映的是元素的化合价与物质类别之间的关系。如图是某同学绘制的关于碳元素的类价二维图。请回答:
①a点物质的化学式是 , 属于(填有机物或无机物)。
②e对应物质类别是 , 写出c点对应的钠盐与稀盐酸反应的化学方程式。
(2)、如图是氮原子、钠原子结构示意图及甲醛(CH2O)的分子模型。
①写出氮化钠的化学式。
②参照甲醛的分子模型,写出如图所示反应的化学方程式。

三、综合题
-
18. 实验室利用如图装置进行组合,制取并收集氧气或二氧化碳。请回答:

 (1)、实验室用高锰酸钾制取并收集氧气,选择的装置组合是(填序号)。(2)、实验室可以按照“②→⑦→再用⑦→”(填序号)的装置顺序制取纯净的CO2气体,从下面选项中选取合适的试剂放入第一个⑦装置的是(填序号),第二个⑦装置盛放的试剂作用是。
(1)、实验室用高锰酸钾制取并收集氧气,选择的装置组合是(填序号)。(2)、实验室可以按照“②→⑦→再用⑦→”(填序号)的装置顺序制取纯净的CO2气体,从下面选项中选取合适的试剂放入第一个⑦装置的是(填序号),第二个⑦装置盛放的试剂作用是。A浓硫酸 B烧碱溶液 C饱和碳酸氢钠溶液 D纯碱溶液
(3)、检验装置②的气密性时,方法之一:向长颈漏斗内加水,使底端形成液封,用铁夹夹紧胶管,双手紧贴容器外壁,一会儿瓶内的气体增大,看到长颈漏斗颈中有现象,证明气密性好。(4)、用如图中的③装置可以制造十分有趣的“化学喷泉”。将胶头滴管中的NaOH溶液挤进圆底烧瓶时,很快看到长导管顶端产生“喷泉”现象。烧瓶中发生反应的化学方程式是。若将烧瓶内的CO2换成下列四种气体中的(填字母序号)仍可产生“喷泉”现象。A.SO2 B.H2 C.CO D.N2
(5)、某兴趣小组同学利用如图装置收集一瓶(100mL)含氧气体积分数为80%的气体。收集方法是:在100mL集气瓶里装满水,塞紧胶塞并关闭活塞b,打开活塞a通入氧气,把瓶里的水排入量筒,当量筒内的水达到设定的体积后立即关闭活塞a,然后打开活塞b通入空气,把瓶里的水全部排入量筒。则通入氧气的体积和通入空气的体积比约为(填最简整数比)。 19. 同学们对氯化氢与盐酸的化学性质是否相同进行如下探究(盐酸与氯化氢的甲苯溶液的微观示意图1、图2所示)。
19. 同学们对氯化氢与盐酸的化学性质是否相同进行如下探究(盐酸与氯化氢的甲苯溶液的微观示意图1、图2所示)。
【提出问题】氯化氢气体与盐酸的化学性质是否相同?
【资料链接】①氯化氢与甲苯不发生化学反应
②氯化氢气体也可溶于甲苯(一种有机溶剂),氯化氢的甲苯溶液中氯化氢以分子的形式存在。
③向浓盐酸中滴加浓硫酸,会有氯化氢逸出。
【分析与猜想】
(1)、盐酸是氯化氢气体溶于水形成的溶液,在盐酸中存在氢离子、氯离子和。(填微粒符号)(2)、氯化氢与盐酸的化学性质可能不同,猜想的理由是。(3)、【实验准备】制取氯化氢的甲苯溶液(如图所示)
①B装置中浓硫酸的作用是。
②D中装有用实验室常见的某种物质浓溶液浸湿的棉花,其目的是除去尾气中的氯化氢,且该物质与氯化氢反应只生成盐和水。该物质可以是(写化学式),反应类型是。
(4)、【进行实验】用盐酸和氯化氢的甲苯溶液进行对比实验。现象
解释
与氧化铜作用
盐酸:
化学方程式:
氯化氢的甲苯溶液:无明显现象
氯化氢在甲苯中没有解离出氢离子
与紫色石落试剂作用
盐酸:紫色石蕊试剂变为红色
氯化氢的甲苯溶液:
氯化氢在甲苯中没有解离出氢离子
【实验结论】氯化氢与盐酸气体的化学性质不同。
20. 蛇纹石矿可以看做由MgO、Fe2O3、Al2O3、SiO2组成。由蛇纹石制取碱式碳酸镁的实验步骤如图所示:
查阅资料:A.几种物质沉淀和溶解时的pH如坐标图像所示;
B.难溶性碱加热会生成两种氧化物,各元素化合价都不变
(1)、溶解前一般将先蛇纹石研磨,目的是 , 实验室中使用的研磨仪器是。(2)、在环节I中产生的红褐色沉淀的反应方程式是。(3)、进行环节I时,需控制溶液pH=6~7(有关沉淀与溶液pH的关系见如图),此时没有产生沉淀的离子是(写离子符号)。Ca(OH)2不能过量,若Ca(OH)2过量,可能导致(填化学式,下同)溶解和产生沉淀。 (4)、从沉淀混合物A中经过一些操作可提取红色氧化物作颜料,具体操作是:先向沉淀物A中加入氢氧化钠溶液调节pH>13,然后过滤、洗涤、(依次填写实验操作名称),得到的红色氧化物是。(5)、物质循环使用,能节约资源。上述实验中,可以循环使用的物质是。
(4)、从沉淀混合物A中经过一些操作可提取红色氧化物作颜料,具体操作是:先向沉淀物A中加入氢氧化钠溶液调节pH>13,然后过滤、洗涤、(依次填写实验操作名称),得到的红色氧化物是。(5)、物质循环使用,能节约资源。上述实验中,可以循环使用的物质是。四、计算题
-
21. 用“盐酸硫化钡法”生产的BaCl2溶液中常会混有盐酸,为了测定该溶液中BaCl2的溶质质量分数,某同学做了以下实验:取该产品液20g于烧杯中,将100 g Na2CO3溶液分五次加入,所得数据如表所示。
Na2CO3溶液质量/g
20
40
60
80
100
产生沉淀的质量/g
0
3.94
7.88
m
9.85
(1)、表格中m的值是。(2)、请计算样品溶液中BaCl2的质量分数(写出详细的计算过程)。(3)、请画出BaCl2质量随Na2CO3溶液质量的关系图像。(4)、用“盐酸—硫化钡法”生产的BaCl2会产生有毒气体H2S(其水溶液呈酸性)可用碱类物质吸收H2S并制取相关硫化物,如表为H2S回收工艺的各项生产成本:购买
出售
项目
NaOH
Ca(OH)2
Na2S
CaS
单价(元/kg)
2.5
107
2.7
0.9
从上述资料分析,用处理H2S更符合经济效益。