安徽省滁州市全椒县“四校”2023年中考模拟检测联考化学试题
试卷更新日期:2023-04-03 类型:中考模拟
一、单选题
-
1. 八公山豆腐制作工艺有着约两千年的制作历史,下列豆腐制作工艺流程中发生化学变化的是( )A、
 磨浆
B、
磨浆
B、 滤渣
C、
滤渣
C、 煮浆
D、
煮浆
D、 压制成型
2. 加强污染治理和生态建设,科学有序推进绿色发展。下列说法错误的是( )A、加大土壤污染风险防控和修复力度 B、强化固体废物和新污染物治理 C、注重多污染物协同治理联防联控 D、加高工厂烟囱将废气向高空排放3. 中学生需要关注营养与健康。下列有关说法正确的是( )A、长期饮用碳酸饮料代替白开水会影响健康 B、缺碘会引起甲状腺肿大,补充越多越好 C、维生素需要量少,对人体没有什么作用 D、油脂是重要的营养物质,每天应大量摄入4. 规范的实验操作是实验成功的保证。下列实验操作正确的是( )A、
压制成型
2. 加强污染治理和生态建设,科学有序推进绿色发展。下列说法错误的是( )A、加大土壤污染风险防控和修复力度 B、强化固体废物和新污染物治理 C、注重多污染物协同治理联防联控 D、加高工厂烟囱将废气向高空排放3. 中学生需要关注营养与健康。下列有关说法正确的是( )A、长期饮用碳酸饮料代替白开水会影响健康 B、缺碘会引起甲状腺肿大,补充越多越好 C、维生素需要量少,对人体没有什么作用 D、油脂是重要的营养物质,每天应大量摄入4. 规范的实验操作是实验成功的保证。下列实验操作正确的是( )A、 点燃酒精灯
B、
点燃酒精灯
B、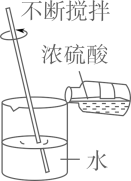 稀释浓硫酸
C、
稀释浓硫酸
C、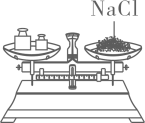 称取氯化钠
D、
称取氯化钠
D、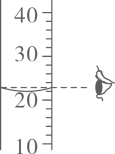 读取液体体积
5. 锶元素广泛存在于土壤、海水中,是一种微量元素,具有防止动脉硬化,防止血栓形成的功能,也可用于制造合金等。如图是锶元素的相关信息,下列说法正确的是( )
读取液体体积
5. 锶元素广泛存在于土壤、海水中,是一种微量元素,具有防止动脉硬化,防止血栓形成的功能,也可用于制造合金等。如图是锶元素的相关信息,下列说法正确的是( ) A、锶原子的中子数为38 B、锶的相对原子质量为87.62g C、锶原子核外有38个电子 D、锶在反应中容易得到电子6. 长春花碱是一种由夹竹桃科植物长春花中提取的抗癌药物,化学式为C46H58N4O9,下列关于长春花碱的说法正确的是( )A、属于碱 B、碳、氢、氧三种元素质量比是46:58:9 C、由117个原子构成 D、碳元素质量分数最高7. 近期,科学家测试了一种新方法:在高温高压下混合水和热空气,以破坏有毒合成物质。在374℃以上,水和有毒物质浆料达到“超临界”状态,水变成了“游离状态”,生成由单个氢原子和氧原子等组成的松散分子,这些分子会摧毁有毒合成物质。下列关于“游离状态水”的说法正确的是( )A、“游离状态水”与普通水物理性质相同 B、“游离状态水”与普通水化学性质相同 C、“游离状态水”中含有氧气 D、可以帮助解决有毒合成物质处理8. 近日,我国科学家通过电催化将二氧化碳与水合成乙酸(CH3COOH),再用乙酸合成葡萄糖。下图是部分化学反应的微观示意图,有关说法正确的是( )
A、锶原子的中子数为38 B、锶的相对原子质量为87.62g C、锶原子核外有38个电子 D、锶在反应中容易得到电子6. 长春花碱是一种由夹竹桃科植物长春花中提取的抗癌药物,化学式为C46H58N4O9,下列关于长春花碱的说法正确的是( )A、属于碱 B、碳、氢、氧三种元素质量比是46:58:9 C、由117个原子构成 D、碳元素质量分数最高7. 近期,科学家测试了一种新方法:在高温高压下混合水和热空气,以破坏有毒合成物质。在374℃以上,水和有毒物质浆料达到“超临界”状态,水变成了“游离状态”,生成由单个氢原子和氧原子等组成的松散分子,这些分子会摧毁有毒合成物质。下列关于“游离状态水”的说法正确的是( )A、“游离状态水”与普通水物理性质相同 B、“游离状态水”与普通水化学性质相同 C、“游离状态水”中含有氧气 D、可以帮助解决有毒合成物质处理8. 近日,我国科学家通过电催化将二氧化碳与水合成乙酸(CH3COOH),再用乙酸合成葡萄糖。下图是部分化学反应的微观示意图,有关说法正确的是( ) A、催化剂在反应后质量减小 B、该技术对温室气体二氧化碳转化有重要意义 C、反应后碳元素质量减少 D、生成的O2与CH3COOH的分子个数比为1:29. 参与家庭劳动,增加劳动技能,锻炼意志品质。下列劳动与所涉及的化学知识相符的是( )
A、催化剂在反应后质量减小 B、该技术对温室气体二氧化碳转化有重要意义 C、反应后碳元素质量减少 D、生成的O2与CH3COOH的分子个数比为1:29. 参与家庭劳动,增加劳动技能,锻炼意志品质。下列劳动与所涉及的化学知识相符的是( )选项
项目
化学知识
A
用气筒给自行车车胎打气
气体分子间隔大
B
轻轻扫地注意扬尘
扬尘分子不断运动
C
用洗涤剂清洗碗筷
洗涤剂溶解油脂
D
用厨余垃圾自制花肥
物质发生剧烈氧化
A、A B、B C、C D、D10. 如图装置可以进行CO还原CuO实验探究。下列说法错误的是( ) A、实验开始前,应该先通一会CO,再加热 B、实验结束前,应该先停止加热,再停止通入CO C、右边酒精灯撤去,换成在管口系紧一个大气球也可以 D、不更换器材,此装置也可以做CO和Fe2O3实验11. 20℃时,将50g氯化钾分成五份依次加到盛有100g水的烧杯中,充分溶解。实验数据如下,下列说法正确的是( )
A、实验开始前,应该先通一会CO,再加热 B、实验结束前,应该先停止加热,再停止通入CO C、右边酒精灯撤去,换成在管口系紧一个大气球也可以 D、不更换器材,此装置也可以做CO和Fe2O3实验11. 20℃时,将50g氯化钾分成五份依次加到盛有100g水的烧杯中,充分溶解。实验数据如下,下列说法正确的是( )序号
①
②
③
④
⑤
氯化钾质量/g
10
25.8
35
36
50
溶液质量/g
110
125.8
135
136
136
A、①溶液为饱和溶液 B、②溶液的溶质质量分数最大 C、③溶液蒸发5g水得到饱和溶液 D、20℃时,氯化钾的溶解度为35g12. 如图,向氢氧化钠溶液(含有酚酞溶液)中逐滴滴加稀盐酸,用温度传感器测得烧杯中溶液温度变化曲线如下。下列判断正确的是( ) A、5s时,已经开始滴加盐酸 B、10s时,溶液由无色变成红色 C、20s时,溶液中溶质有NaCl和HCl D、盐酸与氢氧化钠反应吸热
A、5s时,已经开始滴加盐酸 B、10s时,溶液由无色变成红色 C、20s时,溶液中溶质有NaCl和HCl D、盐酸与氢氧化钠反应吸热二、科普阅读题
-
13. 阅读下列短文,回答问题。
积极探索新型清洁能源有助于促进我国碳达峰、碳中和工作的加速进行,加快产业结构的优化。氢能是一种热值高、能量密度大、来源多样的绿色能源。
现阶段较为成熟的制氢技术路线有3种,即使用煤炭、天然气等化石能源重整制氢,以石油工业副产醇类裂解制氢技术为代表的化工原料高温分解重整制氢,以及电解水制氢。光解水和生物质气化制氢等技术路线仍处于实验和开发阶段,相关技术难以突破,尚未达到规模化制氢的需求。图1给出了目前我国制氢原料占比,图2是主流制氢方法的经济性对比。
 (1)、目前氢气的主要来源是(填“水”或“化石能源”)。不选择另一种来源的原因是。(2)、请写出电解水的化学方程式。(3)、关于能源利用,下列有关说法正确的是____。A、目前人类利用的能源主要是氢能 B、有些化石燃料燃烧不会造成空气污染 C、光解水和生物质气化制氢等技术有待研究
(1)、目前氢气的主要来源是(填“水”或“化石能源”)。不选择另一种来源的原因是。(2)、请写出电解水的化学方程式。(3)、关于能源利用,下列有关说法正确的是____。A、目前人类利用的能源主要是氢能 B、有些化石燃料燃烧不会造成空气污染 C、光解水和生物质气化制氢等技术有待研究三、实验题
-
14. 下列常见的装置常用于初中化学实验室制取气体,请回答有关问题。
 (1)、仪器a的名称是。(2)、用装置A进行高锰酸钾制取氧气,化学方程式为。(3)、用装置B制取二氧化碳,长颈漏斗下端管口应当。(4)、图中用来收集二氧化碳的装置是(填字母)。(5)、向E中通入氧气,现象为。
(1)、仪器a的名称是。(2)、用装置A进行高锰酸钾制取氧气,化学方程式为。(3)、用装置B制取二氧化碳,长颈漏斗下端管口应当。(4)、图中用来收集二氧化碳的装置是(填字母)。(5)、向E中通入氧气,现象为。四、综合题
-
15. 醋酸钙【(CH3COO)2Ca】可用作食品稳定剂、缓冲剂,还是一种很好的食品钙强化剂,吸收效果好。下图是一种生产(CH3COO)2Ca的工艺流程。请回答下列问题:
 (1)、食品钙强化剂中的钙指的是(填“原子”“分子”或“元素”)。(2)、步骤I的CaO中可能混有未分解的石灰石,检验CaO中混有石灰石需要加入的试剂是__。(3)、步骤Ⅱ的化学方程式为。(4)、步骤Ⅲ的化学反应是(填基本反应类型),调节pH需要加入的试剂是。16. 管道疏通颗粒是一种新型厨卫管道深层清洁产品,主要是针对厨卫管道内的油脂、毛发、菜渣、纸棉纤维等物质造成的堵塞进行疏通。某小组欲探究某种管道疏通颗粒中Ca(OH)2、铝粉、缓蚀阻垢剂的用量对疏通效果的影响,进而寻找三者的最佳质量比;并探究该种管道疏通颗粒对下水管道的腐蚀情况。
(1)、食品钙强化剂中的钙指的是(填“原子”“分子”或“元素”)。(2)、步骤I的CaO中可能混有未分解的石灰石,检验CaO中混有石灰石需要加入的试剂是__。(3)、步骤Ⅱ的化学方程式为。(4)、步骤Ⅲ的化学反应是(填基本反应类型),调节pH需要加入的试剂是。16. 管道疏通颗粒是一种新型厨卫管道深层清洁产品,主要是针对厨卫管道内的油脂、毛发、菜渣、纸棉纤维等物质造成的堵塞进行疏通。某小组欲探究某种管道疏通颗粒中Ca(OH)2、铝粉、缓蚀阻垢剂的用量对疏通效果的影响,进而寻找三者的最佳质量比;并探究该种管道疏通颗粒对下水管道的腐蚀情况。查阅资料:Ca(OH)2与铝粉混合遇水后发生化学反应,放大量热和气体,可加快疏通毛发等物质。
(1)、【实验1】按表中数据将各固体物质混合均匀后,加入20mL水,观察到有气体产生,并通过测定反应前后温度的变化比较疏通效果(温度升高值越大,疏通效果越好)。
实验数据记录如下:
序号
Ca(OH)2质量/g
铝粉质量/g
缓蚀阻垢剂质量/g
混合前后温度升高值/℃
①
1.3
0.55
0.18
63
②
1.3
0.75
0.18
78
③
1.3
0.95
0.18
89
④
1.3
1.15
0.18
83
⑤
1.3
0.95
0.04
86
⑥
1.3
0.95
0.09
87
⑦
1.3
0.95
0.27
87
向Ca(OH)2溶液中滴加紫色石蕊溶液显(填序号)。
a.红色 b.紫色 c.蓝色
(2)、要探究铝粉的用量对疏通效果的影响,需对比的实验是①、②和(填实验序号)。(3)、对比实验选择的序号是③、⑤、⑥、⑦,其目的是。(4)、由实验1可得知:Ca(OH)2、铝粉、缓蚀阻垢剂的最佳质量比为。(5)、【实验2】其他条件相同时,改变下水管道材料,测定管道疏通颗粒对各种材料的腐蚀率。实验结果记录如下:
材料
塑料
铜
铁
钢
铝
铝合金
腐蚀率
0.1%
0.4%
0.5%
0.3%
100%
80%
管道疏通颗粒腐蚀率最低的材料是。
(6)、该管道疏通颗粒不宜对材质的下水管道进行疏通。(7)、进行实验2时,需要控制相同的变量有(写2条)。(8)、Ca(OH)2与铝粉混合遇水后发生化学反应的产物之一是Ca(AlO2)2 , 请写出该反应的化学方程式:。五、计算题
-
17. 过氧化氢溶液用途广泛,工业上可用反应制取。(1)、计算16.9gBaO2反应生成H2O2的质量。(2)、该反应产生的过氧化氢溶液浓度不高,欲提高产品浓度,需要对产品进行(填“低温蒸馏”或“高温蒸馏”)。
-
-