广东省湛江市2023届高三一模考试化学试题
试卷更新日期:2023-03-29 类型:高考模拟
一、单选题
-
1. 中华文明源远流长,衣、食、住、行都是中华民族智慧的结晶。下列文明载体与硅酸盐材料有关的是
衣
食
住
行




A.岭南非遗服饰(粤绣)
B.广东小吃(白斩鸡)
C.著名建筑(光孝寺)
D.出行马车(车辇)
A、A B、B C、C D、D2. 下列试剂保存时所选试剂瓶合理的是



A.盛放溴化银固体
B.盛放硫酸溶液
C.盛放硫酸铜固体
D.盛放氢氧化钠溶液
A、A B、B C、C D、D3. 生物体中普遍存在的有机化合物能为生命活动提供物质和能量基础,下列说法错误的是A、麦芽糖及其水解产物均能与银氨溶液发生银镜反应 B、从动物皮中提取的明胶属于蛋白质 C、食用油中含有的油酸易被氧化 D、DNA两条链上的碱基通过共价键配对连接4. 劳动开创未来。下列劳动项目与所述的化学知识正确的是选项
劳动项目
化学知识
A
工厂用铁罐车运输浓硫酸
浓硫酸很难电离出 , 与铁不反应
B
消防演练用泡沫灭火器灭火
与互相促进使水解反应正向进行
C
陶瓷表面上釉
隔绝空气,防止陶瓷被氧化
D
用苯酚和甲醛制备酚醛树脂
酚醛树脂为高分子化合物,该过程发生了加聚反应
A、A B、B C、C D、D5. M、N是两种合成烃,其结构简式如图所示。下列说法错误的是 A、M、N均不溶于水 B、M、N均能发生取代反应和氧化反应 C、N中所有碳原子可能共平面 D、M的一氯取代物有4种(不考虑立体异构)6. 用下列实验装置进行相应实验,其中装置正确且能达到实验目的的是
A、M、N均不溶于水 B、M、N均能发生取代反应和氧化反应 C、N中所有碳原子可能共平面 D、M的一氯取代物有4种(不考虑立体异构)6. 用下列实验装置进行相应实验,其中装置正确且能达到实验目的的是



A.分离碘单质和
B.蒸发溶液,制备晶体
C.制备氢氧化铁胶体
D.乙醇脱水制乙烯
A、A B、B C、C D、D7. 硅与碳同主族,是构成地壳的主要元素之一,下列说法正确的是A、单质硅和金刚石中的键能: B、和中化合价均为-4价 C、中Si原子的杂化方式为sp D、碳化硅硬度很大,属于分子晶体8. 物质的类别和核心元素的化合价是研究物质性质的两个重要维度,下图为氮、硫及其部分化合物的价类二维图,下列说法错误的是 A、坐标轴左侧区域代表的是氮及其化合物 B、的转化均能一步实现 C、c、d和i、j均属于酸性氧化物 D、f与l可以是同一种物质9. X、Y、Z、W为原子序数依次增大的前四周期元素,X与Y、Z均能形成多种常见二元化合物,Y、Z形成的某化合物是参与光合作用的主要气体,基态原子中X、Y、Z的价电子数之和等于W的价电子数,下列说法正确的是A、W属于d区元素 B、原子半径: C、氢化物沸点: D、X与W的最外层电子数相等10. 化学工业为疫情防控提供了强有力的物质支撑。亚氯酸钠(NaClO2)具有强氧化性,受热易分解,可作漂白剂、食品消毒剂等,以氯酸钠等为原料制备亚氯酸钠的工艺流程如下图所示。
A、坐标轴左侧区域代表的是氮及其化合物 B、的转化均能一步实现 C、c、d和i、j均属于酸性氧化物 D、f与l可以是同一种物质9. X、Y、Z、W为原子序数依次增大的前四周期元素,X与Y、Z均能形成多种常见二元化合物,Y、Z形成的某化合物是参与光合作用的主要气体,基态原子中X、Y、Z的价电子数之和等于W的价电子数,下列说法正确的是A、W属于d区元素 B、原子半径: C、氢化物沸点: D、X与W的最外层电子数相等10. 化学工业为疫情防控提供了强有力的物质支撑。亚氯酸钠(NaClO2)具有强氧化性,受热易分解,可作漂白剂、食品消毒剂等,以氯酸钠等为原料制备亚氯酸钠的工艺流程如下图所示。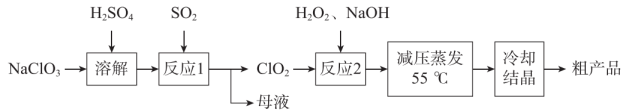
下列说法错误的是
A、“母液”中主要成分是 B、“反应2”中氧化剂与还原剂的物质的量之比为 C、“减压蒸发”可以降低蒸发时的温度,提高产品产率 D、以生成时转移电子数目来衡量,相同质量的消毒能力是的2.5倍11. 乙二胺( )是一种重要的有机化工原料,下列关于乙二胺的说法错误的是 A、易溶于水,其水溶液显碱性 B、键角大于键角 C、第二周期中第一电离能大于C小于N的元素只有一种 D、中,提供孤电子对形成配位键的是12. 下列实验操作所观察到的实验现象正确且能得出相应实验结论的是
)是一种重要的有机化工原料,下列关于乙二胺的说法错误的是 A、易溶于水,其水溶液显碱性 B、键角大于键角 C、第二周期中第一电离能大于C小于N的元素只有一种 D、中,提供孤电子对形成配位键的是12. 下列实验操作所观察到的实验现象正确且能得出相应实验结论的是选项
实验操作
实验现象
实验结论
A
向盛有3.0mL无水乙醇的试管中加入一小块金属钠
缓慢产生气泡
乙醇分子中羟基氢的活泼性小于水分子中的氢
B
向盛有2.0mL甲苯的试管中加入3滴酸性溶液,用力振荡
紫色褪去
甲苯中含有碳碳双键,可被酸性溶液氧化
C
向含有少量的溶液中滴加少量稀溶液
产生白色沉淀
D
用玻璃棒蘸取溶液滴在试纸上
试纸先变蓝,后褪色
溶液呈中性
A、A B、B C、C D、D13. 常温下,和溶液中含磷微粒的物质的量分数与溶液的关系分别如图所示,向等物质的量浓度的和混合溶液中加入适量的溶液,下列说法错误的是 A、由图可知是二元酸 B、时, C、常温下,的反应平衡常数 D、溶液由3变为6.6的过程中,水的电离程度增大14. 宏观辨识与微观探析是化学学科核心素养之一,下列关于次氯酸盐性质实验对应的反应方程式书写正确的是A、将足量的二氧化碳通入溶液中: B、验证“84”消毒液与洁则剂不能混合的原因: C、用溶液吸收废气中的制石膏乳: D、将硫酸铬溶液滴入含的强碱性溶液中:15. 双极膜在电化学中应用广泛,它是由阳离子交换膜和阴离子交换膜复合而成。双极膜内层为水层,工作时水层中的解离成和 , 并分别通过离子交换膜向两侧发生迁移。三碘甲烷()又名碘仿,在医药和生物化学中用作防腐剂和消毒剂。电解法制取碘仿的工作原理如图所示,反应原理为 , 下列说法错误的是
A、由图可知是二元酸 B、时, C、常温下,的反应平衡常数 D、溶液由3变为6.6的过程中,水的电离程度增大14. 宏观辨识与微观探析是化学学科核心素养之一,下列关于次氯酸盐性质实验对应的反应方程式书写正确的是A、将足量的二氧化碳通入溶液中: B、验证“84”消毒液与洁则剂不能混合的原因: C、用溶液吸收废气中的制石膏乳: D、将硫酸铬溶液滴入含的强碱性溶液中:15. 双极膜在电化学中应用广泛,它是由阳离子交换膜和阴离子交换膜复合而成。双极膜内层为水层,工作时水层中的解离成和 , 并分别通过离子交换膜向两侧发生迁移。三碘甲烷()又名碘仿,在医药和生物化学中用作防腐剂和消毒剂。电解法制取碘仿的工作原理如图所示,反应原理为 , 下列说法错误的是 A、电极N连接直流电源的负极 B、电解一段时间后,硫酸溶液浓度降低 C、电极M上的主要反应为 D、每制备1mol三碘甲烷,理论上双极膜内解离16. 氨气在工业上应用广泛,已知反应 , 反应相同时间,的体积百分数随温度的变化情况如图所示,下列相关描述正确的是
A、电极N连接直流电源的负极 B、电解一段时间后,硫酸溶液浓度降低 C、电极M上的主要反应为 D、每制备1mol三碘甲烷,理论上双极膜内解离16. 氨气在工业上应用广泛,已知反应 , 反应相同时间,的体积百分数随温度的变化情况如图所示,下列相关描述正确的是 A、线上的点均代表平衡时刻的点 B、逆反应速率: C、b点时 D、平衡常数值:
A、线上的点均代表平衡时刻的点 B、逆反应速率: C、b点时 D、平衡常数值:二、非选择题
-
17. 某实验小组为探究含硫化合物的性质,设计如下实验探究的氧化性。
实验操作:向小试管中加入溶液,并滴入两滴淀粉溶液,无明显变化,再加入少量溶液,试管中溶液立即变蓝。取上层清液检验,证明溶液中存在。
(1)、与反应的离子方程式为。(2)、检验该溶液中存在的具体操作及现象为。(3)、实验结论:的氧化性(填“强于”或“弱于”)。已知:可与发生反应:。为了进一步探究与的反应速率,小组同学设计下表实验:
试验编号
溶液/
溶液/
蒸馏水/
0.4%的淀粉溶液/滴
溶液/
变色时间/
Ⅰ
4.0
0
4.0
2
2.0
立即
Ⅱ
4.0
1.0
3.0
2
2.0
30
(4)、上述两实验中均加入了不同体积的蒸馏水,其目的为。加入溶液后溶液变蓝的时间明显增长,小组同学对此提出两种猜想:
猜想1:先与反应,消耗完后才与反应;
猜想2:与反应的速率远低于与反应的速率。
为验证上述猜想,小组同学补充下表实验:
试验编号
KI溶液/
碘水/
溶液/
0.4%的淀粉溶液/滴
溶液/
实验现象
Ⅲ
2
0
20
10
0
0.2
下层溶液显浅紫色
Ⅳ
0
5
20
0
2
20
溶液先变蓝,后迅速褪色,一段时间后又变蓝
(5)、验证猜想1的实验设计为(填“实验Ⅱ”或“实验Ⅳ”下同),验证猜想2的实验设计为。(6)、下层溶液显浅紫色的原因为。(7)、由上述实验可知(填“猜想1”或“猜想2”)成立。18. 镍钴锰酸锂材料是近年来开发的一类新型锂离子电池正极材料,具有容量高、循环稳定性好、成本适中等优点,这类材料可以同时有效克服钴酸锂材料成本过高、磷酸铁锂容量低等问题,工业上可由废旧的钴酸锂、磷酸铁锂、镍酸锂、锰酸锂电池正极材料(还含有铝箔、炭黑、有机黏合剂等),经过一系列工艺流程制备镍钴锰酸锂材料,该材料可用于三元锂电池的制备,实现电池的回收再利用,工艺流程如下图所示: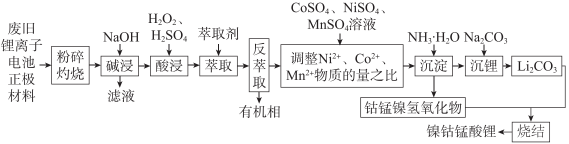
已知:①粉碎灼烧后主要成分是、、、MnO、Fe2O3、;
②萃取剂对选择性很高,且生成的物质很稳定,有机相中的很难被反萃取
请回答下列问题:
(1)、正极材料在“灼烧”前先粉碎的目的是。(2)、“碱浸”的目的是 , 涉及的化学方程式是。(3)、“酸浸”时加入的作用是。(4)、上述工艺流程中采用萃取法净化除去了 , 若采用沉淀法除去铁元素,结合下表,最佳的pH范围是。开始沉淀时pH
1.5
3.4
6.3
6.6
6.7
7.8
完全沉淀时pH
3.5
4.7
8.3
9.2
9.5
10.4
(5)、镍钴锰酸锂材料中根据镍钴锰的比例不同,可有不同的结构,其中一种底面为正六边形结构的晶胞如图所示。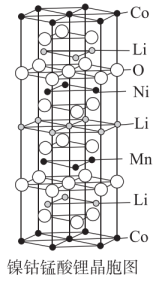
①该物质的化学式为 , 写出基态Mn原子价层电子的轨道表示式。
②已知晶胞底面边长是anm,高是bnm,一个晶胞的质量为Mg,计算该晶胞的密度(用计算式表示)。
19. 碳达峰、碳中和是现在需要继续完成的环保任务,的综合利用成为热点研究对象,作为碳源加氢是再生能源的有效方法,加氢可以合成甲醇,Olah提出“甲醇经济”概念,认为甲醇会在不久的将来扮演不可或缺的角色,通过加氢生产甲醇是有希望的可再生路线之一,该过程主要发生如下反应:反应Ⅰ:
反应Ⅱ:
(1)、①相关键能如下表,则 , 该反应的活化能(填“大于”“小于”或“等于”)。化学键
键能
436
1071
464
803
②若K1、K2分别表示反应Ⅰ、反应Ⅱ的平衡常数,则的平衡常数K=(用含K1、K2的代数式表示)。
③已知的正反应速率( k为正反应的速率常数),某温度时测得数据如下:
1
0.02
0.01
2
0.02
0.02
a
则此温度下表中a=。
(2)、据文献报道,基纳米材料作为高性能催化剂可将电还原为高能量密度的 , 不同催化剂对生成的法拉第效率与电极电势的变化如图所示(已知法拉第效率是指实际生成物和理论生成物的百分比),为了保证生成甲醇的法拉第效率,最合适的电势及最佳催化剂是。 (3)、在催化剂作用下,发生上述反应Ⅰ、Ⅱ,达平衡时的转化率随温度和压强的变化如图,判断p1、p2、p3的大小关系: , 解释压强一定时,的平衡转化率呈现如图变化的原因:。
(3)、在催化剂作用下,发生上述反应Ⅰ、Ⅱ,达平衡时的转化率随温度和压强的变化如图,判断p1、p2、p3的大小关系: , 解释压强一定时,的平衡转化率呈现如图变化的原因:。 (4)、某温度下,初始压强为 , 向容积为的恒容密闭容器中充入、发生反应Ⅰ、Ⅱ,平衡时的转化率是50%,体系内剩余 , 反应Ⅱ的平衡常数K=。20. 化合物H是用于合成某种镇痛药的医药中间体,利用烃A合成H的某路线如下图所示:
(4)、某温度下,初始压强为 , 向容积为的恒容密闭容器中充入、发生反应Ⅰ、Ⅱ,平衡时的转化率是50%,体系内剩余 , 反应Ⅱ的平衡常数K=。20. 化合物H是用于合成某种镇痛药的医药中间体,利用烃A合成H的某路线如下图所示:
已知:
回答下列问题:
(1)、A的化学名称为;D中的官能团名称为。(2)、由B生成C时需要加入的试剂和反应条件为。(3)、由C生成D的反应类型为。(4)、由G生成H的化学方程式为。(5)、 的同分异构体中含六元碳环的有种(不考虑立体异构),写出其中一种核磁共振氢谱有6组峰的结构简式。 (6)、参照上述合成路线设计以D为原料合成高分子化合物
的同分异构体中含六元碳环的有种(不考虑立体异构),写出其中一种核磁共振氢谱有6组峰的结构简式。 (6)、参照上述合成路线设计以D为原料合成高分子化合物 的路线(无机试剂任选)。
的路线(无机试剂任选)。