上海市虹口区2023年中考一模化学试题
试卷更新日期:2023-03-24 类型:中考模拟
一、单选题
-
1. 空气中含量增加导致温室效应加剧的物质是( )A、氧气 B、氮气 C、稀有气体 D、二氧化碳2. 下列物质由两种元素组成的是( )A、Cl2 B、KClO3 C、CH4 D、C2H6O3. 属于氧化物的是( )A、O3 B、CaO C、BaCl2 D、KMnO44. 与金刚石互为同素异形体的物质是( )A、石墨 B、木炭 C、一氧化碳 D、大理石5. 属于纯净物的是( )A、碘酒 B、五水合硫酸铜 C、大理石 D、液态空气6. 某化合物由X元素和氧元素组成,X元素的化合价为+3价,氧元素的化合价为-2价,该物质的化学式是( )A、X3O2 B、X2O3 C、XO3 D、X3O7. 属于化学变化的是( )A、燃料燃烧 B、矿石粉碎 C、打磨玉器 D、剪裁布料8. 属于分解反应的是( )A、H2CO3CO2↑+H2O B、S+O2SO2 C、H2+CuOCu+H2O D、CuSO4+2NaOH=Na2SO4+Cu(OH)2↓9. 属于溶液的是( )A、汽水 B、酸奶 C、米糊 D、泥浆10. 四种食物近似的pH如下,其中呈碱性的是( )A、苹果:2.9~3.3 B、草莓:3.0~3.5 C、菠菜:5.1~5.7 D、鸡蛋清:7.6~8.011. 10mL水与10mL酒精混合后体积小于20mL,主要原因是( )A、分子的质量小 B、分子的体积小 C、分子之间有间隙 D、分子由原子构成12. 细铁丝在氧气中燃烧的化学方程式书写正确的是( )A、3Fe+O4Fe3O4 B、3Fe+2O2=Fe3O4 C、3Fe+2O2Fe3O4 D、2Fe+O2FeO13. 如图所示进行水电解实验,说法正确的是( )
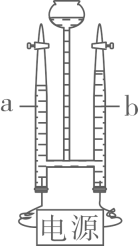 A、a、b两处产生气体的质量比为1:2 B、a处气体体积比b处小说明其溶解度较大 C、液体减少的体积等于生成气体的体积之和 D、可以用燃着的木条检验a、b两处产生的气体14. 某反应的化学方程式是SiO2+2C2X↑+Y,相关分析正确的是( )A、SiO2可能是气体 B、X是一氧化碳 C、Y是金属单质 D、反应前后元素的存在形态均改变
A、a、b两处产生气体的质量比为1:2 B、a处气体体积比b处小说明其溶解度较大 C、液体减少的体积等于生成气体的体积之和 D、可以用燃着的木条检验a、b两处产生的气体14. 某反应的化学方程式是SiO2+2C2X↑+Y,相关分析正确的是( )A、SiO2可能是气体 B、X是一氧化碳 C、Y是金属单质 D、反应前后元素的存在形态均改变二、多选题
-
15. 下列物质中,含有1mol氧原子的是( )A、约6.02×1023个一氧化碳分子 B、122.5g氯酸钾 C、18mL水(密度为1.0g/cm3) D、32g氧气16. 某温度时,三种气体溶解度曲线如图所示,下列说法正确的是( )
 A、气体都难溶于水 B、该温度时,甲的溶解度最大 C、该温度时,三种气体中丙的溶解度受压强影响最小 D、该温度时,相同质量的甲、乙、丙溶液,压强减小,甲溶液质量变化最大17. t℃时,向100g、50%的硝酸钾溶液中加入甲(不与水或硝酸钾反应),溶液中硝酸钾的质量分数随加入甲的质量变化情况如图所示。下列分析正确的是( )
A、气体都难溶于水 B、该温度时,甲的溶解度最大 C、该温度时,三种气体中丙的溶解度受压强影响最小 D、该温度时,相同质量的甲、乙、丙溶液,压强减小,甲溶液质量变化最大17. t℃时,向100g、50%的硝酸钾溶液中加入甲(不与水或硝酸钾反应),溶液中硝酸钾的质量分数随加入甲的质量变化情况如图所示。下列分析正确的是( ) A、甲可以是氯化钠溶液 B、甲可以是浓度小于25%的硝酸钾溶液 C、溶液中硝酸钾的质量可能变大 D、溶液中水的质量可能不变
A、甲可以是氯化钠溶液 B、甲可以是浓度小于25%的硝酸钾溶液 C、溶液中硝酸钾的质量可能变大 D、溶液中水的质量可能不变三、填空题
-
18. 化学与我们的生活息息相关。(1)、用物质的化学式填空:
空气中含量最多的气体是;
引起酸雨的主要物质是;
用于填充高空探测气球的稀有气体是。
(2)、自来水生产中,加入活性炭的作用是;可以用于杀菌消毒的物质是。(3)、如图所示的实验可测定空气中氧气的体积分数。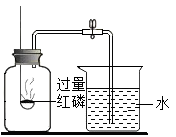
红磷燃烧的化学方程式是;实验中使用的红磷需过量,目的是。
(4)、实验室用3%的过氧化氢溶液和二氧化锰为原料制取氧气,反应的化学方程式是;二氧化锰的作用是。四、综合题
-
19. 实验室制取二氧化碳的装置如图所示。
 (1)、该实验收集气体的方法是。(2)、生成0.01mol二氧化碳时,参加反应的碳酸钙是多少摩尔?(根据化学方程式列式计算)(3)、收集一定量二氧化碳后,夹紧弹簧夹,试管中液面逐渐下降,此时溶液中的溶质是。20. 海水晒盐是获得粗盐的一种方法,粗盐的主要成分是氯化钠。(1)、海水晒盐的主要过程如下图所示。
(1)、该实验收集气体的方法是。(2)、生成0.01mol二氧化碳时,参加反应的碳酸钙是多少摩尔?(根据化学方程式列式计算)(3)、收集一定量二氧化碳后,夹紧弹簧夹,试管中液面逐渐下降,此时溶液中的溶质是。20. 海水晒盐是获得粗盐的一种方法,粗盐的主要成分是氯化钠。(1)、海水晒盐的主要过程如下图所示。
I、海水进入蒸发池后,经风吹日晒,水分逐渐减少,但无晶体析出,说明原海水是氯化钠的(选填“饱和”或“不饱和”)溶液。
II、蒸发池内,溶液中氯化钠的质量分数(选填“变大”“变小”或“不变”)。
III、上述过程中采用的结晶方法是。
(2)、某粗盐样品中除氯化钠外还含有少量泥沙和氯化镁。温度(℃)
0
10
20
40
溶解度
(g/100g水)
氯化钠
35.7
35.8
36.0
36.4
氯化镁
52.9
53.6
54.6
57.5
I、40℃时,溶解度较大的物质是。
II、20℃时,300g水中最多能溶解氯化钠g。
III、20℃时,取10g该粗盐样品,放入30g水中,充分溶解后过滤,得到39.7g滤液。请分析样品中的可溶性物质是否已全部溶解并说明理由。
21. 某小组用碳、一氧化碳分别与等质量的氧化铜反应制取铜,实验装置如下图所示。 (1)、【实验一】碳与氧化铜反应制取铜
(1)、【实验一】碳与氧化铜反应制取铜A处发生反应的化学方程式是;B中的现象是。
(2)、加热至不再产生气体时,应夹紧弹簧夹、熄灭酒精喷灯,待冷却至室温后取出剩余固体。按上述顺序操作的目的是。(3)、【实验二】一氧化碳与氧化铜反应制取铜开始实验时,下列操作正确的顺序是。
a、通入一氧化碳一段时间
b、点燃C处酒精灯
c、点燃E处酒精灯
d、检验k处气体纯度
(4)、实验二有尾气处理装置,该装置是(选填“C”“D”或“E”)。(5)、经测定,上述两个实验中氧化铜均全部转化为铜、实验一中剩余固体的质量大于实验二中剩余固体的质量,则实验一剩余固体的成分是。
-