河南省周口市川汇区2023年中考一模化学试题
试卷更新日期:2023-03-24 类型:中考模拟
一、单选题
-
1. 民以食为天,下列美食中富含维生素的是( )A、合川桃片 B、奉节脐橙 C、江津老白干 D、城口老腊肉2. 为相对原子质量的测定作出了卓越贡献的科学家是( )A、侯德榜 B、屠呦呦 C、拉瓦锡 D、张青莲3. 归类整理是学习理化的一种重要方法。下列归类正确的是( )A、氯酸钾、高锰酸钾、氯化钾都是盐 B、氦气、氖气、氯气都是稀有气体 C、橡胶、沥青、食盐都是非晶体 D、石油、电能、太阳能都是一次能源4. 化学推动了社会进步,使我们的世界变得绚丽多彩。下列事实中,发生了化学变化的是( )A、汽油挥发 B、用乙醇汽油做燃料驱动汽车 C、海水晒盐 D、切割大理石做建筑材料5. 人类生存需要新鲜的空气,下列情况不会造成空气污染的是( )A、绿色植物的光合作用 B、海洋、陆地生物的腐烂 C、汽车、飞机尾气的排放 D、煤、石油等燃料的燃烧6. 材料的合理使用使我们的生活更加便捷,下列物品的材料不属于有机合成材料的是( )A、塑料水杯 B、不锈钢锅 C、合成橡胶轮胎 D、涤纶衣服7. 下列各组物质中,都由离子构成的一组是( )A、铜、硫酸铜 B、干冰、金刚石 C、氯化钠、C60 D、硫酸铜、氯化钠8. 化肥是农作物丰产的保障,下列属于复合肥的是( )A、KCl B、CaHPO4 C、KNO3 D、(NH4)2SO49. 下列实验操作或实验方案设计不能达到实验目的的是( )A、稀释浓硫酸

B、量取一定体积的水
B、量取一定体积的水 C、测定空气中氧气含量
C、测定空气中氧气含量 D、探究铁生锈需要氧气
D、探究铁生锈需要氧气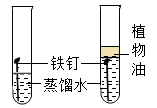 10. 2022年6月5日神舟十四号载人飞船发射成功,NiFe2O4可作为催化剂将航天员呼出的CO2转化为O2 , 已知NiFe2O4中Fe为+3价,则Ni的化合价为( )A、+1 B、+2 C、+3 D、+411. 水与人类的生产生活息息相关,下列关于水和溶液的说法正确的是( )A、自然界中的水过滤后即变成纯水 B、碱溶液的pH>7,则pH>7的溶液一定是碱溶液 C、氯化钾溶液加水稀释的过程中,氯化钾的质量不变 D、氢氧化钠溶液和浓硫酸都可用来干燥氧气12. 往AgNO3、Cu(NO3)2的混合溶液中加入一些铁粉,待充分反应后再过滤,不可能存在的情况是( )A、滤纸上有Ag、Cu,滤液中有AgNO3、Fe(NO3)2 B、滤纸上有Ag,滤液中有Cu(NO3)2、Fe(NO3)2 C、滤纸上有Ag、Cu,滤液中有Cu(NO3)2、Fe(NO3)2 D、滤纸上有Ag、Cu、Fe,滤液中只有Fe(NO3)213. 下列图像不能正确反应其对应关系的是( )A、
10. 2022年6月5日神舟十四号载人飞船发射成功,NiFe2O4可作为催化剂将航天员呼出的CO2转化为O2 , 已知NiFe2O4中Fe为+3价,则Ni的化合价为( )A、+1 B、+2 C、+3 D、+411. 水与人类的生产生活息息相关,下列关于水和溶液的说法正确的是( )A、自然界中的水过滤后即变成纯水 B、碱溶液的pH>7,则pH>7的溶液一定是碱溶液 C、氯化钾溶液加水稀释的过程中,氯化钾的质量不变 D、氢氧化钠溶液和浓硫酸都可用来干燥氧气12. 往AgNO3、Cu(NO3)2的混合溶液中加入一些铁粉,待充分反应后再过滤,不可能存在的情况是( )A、滤纸上有Ag、Cu,滤液中有AgNO3、Fe(NO3)2 B、滤纸上有Ag,滤液中有Cu(NO3)2、Fe(NO3)2 C、滤纸上有Ag、Cu,滤液中有Cu(NO3)2、Fe(NO3)2 D、滤纸上有Ag、Cu、Fe,滤液中只有Fe(NO3)213. 下列图像不能正确反应其对应关系的是( )A、 加热一定高锰酸钾固体产生氧气
B、
加热一定高锰酸钾固体产生氧气
B、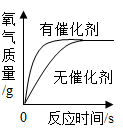 加热两份等质量的氯酸钾制取氧气
C、
加热两份等质量的氯酸钾制取氧气
C、 用红磷燃烧法测定空气中氧气含量时瓶内压强的变化
D、
用红磷燃烧法测定空气中氧气含量时瓶内压强的变化
D、 电解水一定质量的水
14. 现将足量氢气通过45g灼热的氧化铜和铜的混合物(铜和氢气不反应)。完全反应后称量剩余固体质量为37g。计算原混合物中氧化铜的质量为( )A、20g B、32g C、40g D、42g
电解水一定质量的水
14. 现将足量氢气通过45g灼热的氧化铜和铜的混合物(铜和氢气不反应)。完全反应后称量剩余固体质量为37g。计算原混合物中氧化铜的质量为( )A、20g B、32g C、40g D、42g二、填空题
-
15. 空气中体积分数含量最高的气体是(填化学用语,下同)。我国化学家侯德榜创造的联合制碱法为制碱工业做出巨大贡献,联合制碱法中的“碱”是指。16. 氮化镓是生产5G芯片的关键材料之一。氮的原子结构示意图和镓在元素周期表中的信息如图所示。氮原子最外层电子数为;镓在化合物中显+3价,氮化镓的化学式为 。
 17. 下图是a、b、c三种固体物质的溶解度曲线,请回答问题。
17. 下图是a、b、c三种固体物质的溶解度曲线,请回答问题。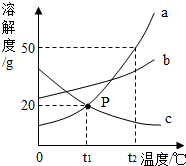 (1)、图中P点所表示的意义是。(2)、将c物质的不饱和溶液转变成饱和溶液可采取的方法有(写出一种即可)。(3)、将t2℃时a、b、c三种物质饱和溶液的温度降到t1℃时,三种溶液中溶质的质量分数由大到小的排列顺序是。18. 通过晾晒海水或煮盐井水等,可以得到粗盐。(1)、海水“晒盐”得到的粗盐中含有少量的泥沙等不溶性杂质,可通过下列步骤制取精盐:
(1)、图中P点所表示的意义是。(2)、将c物质的不饱和溶液转变成饱和溶液可采取的方法有(写出一种即可)。(3)、将t2℃时a、b、c三种物质饱和溶液的温度降到t1℃时,三种溶液中溶质的质量分数由大到小的排列顺序是。18. 通过晾晒海水或煮盐井水等,可以得到粗盐。(1)、海水“晒盐”得到的粗盐中含有少量的泥沙等不溶性杂质,可通过下列步骤制取精盐:溶解→过滤→(填写操作步骤)。
(2)、如果两次过滤后滤液仍浑浊,原因可能是(写出一种即可)。(3)、粗盐提纯实验中,先称取5.0g粗盐,量取10mL水只溶解4.0g粗盐,最终得到3.6g精盐,则精盐的产率是。19. 将稀硫酸慢慢滴入盛有氢氧化钠溶液的烧杯中,用温度计测量烧杯中溶液的温度随加入稀硫酸的质量变化曲线如图所示: (1)、在滴加稀硫酸的过程中,烧杯中溶液的pH逐渐(选填“增大”“减小”或“不变”)。(2)、该反应的化学方程式为。(3)、图中C点对应的溶液中大量存在的离子有(填写离子符号)。
(1)、在滴加稀硫酸的过程中,烧杯中溶液的pH逐渐(选填“增大”“减小”或“不变”)。(2)、该反应的化学方程式为。(3)、图中C点对应的溶液中大量存在的离子有(填写离子符号)。三、综合题
-
20. A~F是初中化学常见的物质,它们之间的转化关系如图所示。图中“一”表示两种物质间能发生化学反应,“→”表示两种物质间的转化关系。已知A可以用来检验CO2 , B、E是两种组成元素相同的液体,C、F是两种组成元素相同的气体,(其中部分反应条件、反应物及生成物已略去)。请回答下列问题:
 (1)、E物质的化学式为;(2)、B→A反应的化学方程式为;(3)、D一F的基本反应类型为。21. 请用所学化学知识解释下列生活中常见的现象。(1)、从很远的地方就能闻到花香。(2)、测量体温时,水银温度计里的汞柱会升高。22. 气体的鉴别。(简要写出实验步骤,现象及结论)(1)、如何鉴别一瓶无色无味气体是否是二氧化碳?(2)、两瓶无色无味气体,一瓶是氧气,一瓶是空气,如何进行鉴别?23. 将过量的锌粒逐渐加入到一定质量FeCl2和CuCl2的混合溶液中,如图所示为反应过程溶液中FeCl2的质量随加入锌的质量的变化情况。
(1)、E物质的化学式为;(2)、B→A反应的化学方程式为;(3)、D一F的基本反应类型为。21. 请用所学化学知识解释下列生活中常见的现象。(1)、从很远的地方就能闻到花香。(2)、测量体温时,水银温度计里的汞柱会升高。22. 气体的鉴别。(简要写出实验步骤,现象及结论)(1)、如何鉴别一瓶无色无味气体是否是二氧化碳?(2)、两瓶无色无味气体,一瓶是氧气,一瓶是空气,如何进行鉴别?23. 将过量的锌粒逐渐加入到一定质量FeCl2和CuCl2的混合溶液中,如图所示为反应过程溶液中FeCl2的质量随加入锌的质量的变化情况。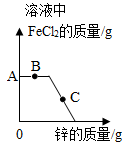 (1)、请写出B 点时发生反应的化学方程式。(2)、反应后溶液的质量比反应前溶液的质量增大,请说明原因。24. 实验室常选用下列装置制取和收集气体。
(1)、请写出B 点时发生反应的化学方程式。(2)、反应后溶液的质量比反应前溶液的质量增大,请说明原因。24. 实验室常选用下列装置制取和收集气体。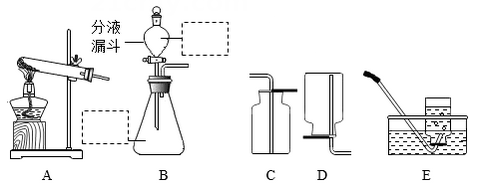 (1)、写出用A装置制取实验室一种常见气体的化学方程式。(2)、选取B装置制取二氧化碳气体时,请在虚线框内写出所需物质。(3)、已知氨气的密度比空气小,且极易溶于水,应该选用哪个装置收集氨气?25. 化学通过帮助我们认识和改造物质世界,为我们解决能源,材料和环境等重大问题,从而促进社会和谐发展。(1)、材料的应用与发展,大大方便了人们的生活,可用于制造人造骨、航天飞机等的钛合金属于材料(填“有机合成材料”“金属材料”“无机非金属材料”“复合材料”)。(2)、节能、减排、低碳、环保是当今世界的主旋律。
(1)、写出用A装置制取实验室一种常见气体的化学方程式。(2)、选取B装置制取二氧化碳气体时,请在虚线框内写出所需物质。(3)、已知氨气的密度比空气小,且极易溶于水,应该选用哪个装置收集氨气?25. 化学通过帮助我们认识和改造物质世界,为我们解决能源,材料和环境等重大问题,从而促进社会和谐发展。(1)、材料的应用与发展,大大方便了人们的生活,可用于制造人造骨、航天飞机等的钛合金属于材料(填“有机合成材料”“金属材料”“无机非金属材料”“复合材料”)。(2)、节能、减排、低碳、环保是当今世界的主旋律。①开发 (举一例)等新能源,不仅可以部分解决化石能源紧缺问题,还可以减少对环境的污染。
②煤燃烧时加入石灰石成生石灰作为固硫剂制成型煤,可以减少 (填化学式)。气体和氮的氧化物等有害气体的排放,有效减少酸雨的形成。
(3)、烧碱是一种重要的工业原料。试回答下列问题:氢氧化钠有很强的腐蚀性,如果不小心站到皮肤上要立即用大量的水冲洗,然后涂上(填“硼酸溶液”、“碳酸氢钠溶液”、“石灰水”)。(4)、在工业上可以用纯碱和石灰石为原料制备氢氧化钠,主要流程如图所示: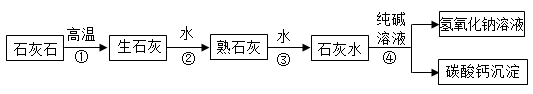
上述流程中,步骤①所涉及的反应类型为反应(填“化合”、“分解”,“置换”、“复分解”)写出上述转化流程步骤④中所发生反应的化学方程式。
(5)、现取100gCuCl2溶液倒入烧杯中,慢慢向烧杯中加入溶质质量分数为10%的NaOH溶液,反应过程中产生沉淀的质量与所加入NaOH溶液的质量关系如图所示。试回答: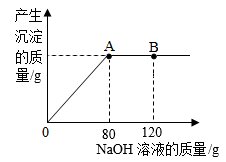
①当加入NaOH溶液120g时(即图中B点),烧杯中溶液里大量存在的阳离子是(填离子符号)。
②当加入NaOH溶液80g时(即图中A点),恰好完全反应试通过计算求产生沉淀质量。(计算结果精确至0.1g)