2022--2023学年中考化学第一轮复习专题 10 常见酸碱盐及化学肥料
试卷更新日期:2023-03-24 类型:一轮复习
一、单选题
-
1. 下列说法正确的是A、向某固体上滴加稀盐酸,有气泡产生,则该固体一定是碳酸盐 B、稀有气体可做保护气,则可做保护气的一定是稀有气体 C、取少量溶液于试管中,滴加氯化钡溶液,有白色沉淀生成,证明该溶液中一定有硫酸根离子 D、碱溶液能使酚酞溶液变红,则能使酚酞溶液变红的物质不一定是碱溶液2. 某实验小组使用pH传感器探究稀盐酸和氢氧化钠溶液的反应,实验过程中溶液pH的变化如图所示。下列说法中,正确的是
 A、图中a点时的溶液pH>7,呈酸性 B、图中c点时的溶液里溶质只有氯化钠 C、该实验是将氢氧化钠溶液滴加到稀盐酸中 D、该反应的微观实质是H+和OH﹣结合生成H2O3. 下列各组中的两种物质,在溶液中不能发生复分解反应的是( )A、H2SO4与NaOH B、KNO3与NaCl C、BaCO3与HCl D、NaOH与CuSO44. 下列有关粗盐提纯过程的叙述错误的是( )A、除去食盐水中的可溶性杂质,可以采用化学方法 B、除去食盐水中可溶性杂质的化学原理为:使杂质离子以沉淀或气体的形式从食盐水中分离出来 C、除去食盐中难溶性杂质的方法属于化学方法 D、粗盐提纯过程中既有化学方法,又有物理方法5. 化学与生产生活息息相关。下列有关说法中,不合理的是( )A、农业上,常用烧碱中和土壤的酸性 B、焙制面包时加入小苏打做膨松剂 C、工业生产中储运烧碱,可用铁桶盛装 D、硫酸铜可用于配制农用杀菌剂波尔多液6. 下列叙述中,正确的是( )A、打开盛浓硫酸的试剂瓶,瓶口会产生白雾 B、浓硫酸露置于空气中,溶质质量分数会变大 C、pH的大小与一定量溶液中所含H+或 OH-的数量多少有关 D、露置于空气中的固体氢氧化钠,其成分不会发生变化7. 下列除杂和鉴别方法不正确的是( )
A、图中a点时的溶液pH>7,呈酸性 B、图中c点时的溶液里溶质只有氯化钠 C、该实验是将氢氧化钠溶液滴加到稀盐酸中 D、该反应的微观实质是H+和OH﹣结合生成H2O3. 下列各组中的两种物质,在溶液中不能发生复分解反应的是( )A、H2SO4与NaOH B、KNO3与NaCl C、BaCO3与HCl D、NaOH与CuSO44. 下列有关粗盐提纯过程的叙述错误的是( )A、除去食盐水中的可溶性杂质,可以采用化学方法 B、除去食盐水中可溶性杂质的化学原理为:使杂质离子以沉淀或气体的形式从食盐水中分离出来 C、除去食盐中难溶性杂质的方法属于化学方法 D、粗盐提纯过程中既有化学方法,又有物理方法5. 化学与生产生活息息相关。下列有关说法中,不合理的是( )A、农业上,常用烧碱中和土壤的酸性 B、焙制面包时加入小苏打做膨松剂 C、工业生产中储运烧碱,可用铁桶盛装 D、硫酸铜可用于配制农用杀菌剂波尔多液6. 下列叙述中,正确的是( )A、打开盛浓硫酸的试剂瓶,瓶口会产生白雾 B、浓硫酸露置于空气中,溶质质量分数会变大 C、pH的大小与一定量溶液中所含H+或 OH-的数量多少有关 D、露置于空气中的固体氢氧化钠,其成分不会发生变化7. 下列除杂和鉴别方法不正确的是( )选项
物质(括号内为杂质)
加入试剂和方法
A
CO2(CO)
点燃
B
CaO固体(CaCO3)
高温煅烧
C
鉴别硬水和软水
加入肥皂水
D
区分白酒和白醋
闻气味
A、A B、B C、C D、D8. 对化学反应 A+B=C+D 的下列说法中正确的是 ( )A、若 A 是稀硫酸,则生成物质中一定有水 B、若C,D 是盐和水,则A,B 一定是酸和碱 C、若 A 是可溶性碱,B 是可溶性盐,则 C 一定是沉淀 D、若 A,B,C,D 都是化合物,则该反应不一定是复分解反应9. 某校化学小组在利用稀硫酸和氢氧化钠溶液探究酸碱中和反应时,利用数字化传感器测得烧杯中溶液pH的变化,其图像如图所示。下列说法错误的是( ) A、该实验是将氢氧化钠溶液滴入到盛有稀硫酸的烧杯中 B、b点表示稀硫酸和氢氧化钠溶液恰好完全反应 C、图中c点所示溶液中含有两种溶质 D、该反应的实质是H+和OH-结合生成H2O10. 钾肥有增强植物抗倒伏能力的功能。下列物质能用作钾肥的是( )A、CO(NH2)2 B、K2SO4 C、Ca3(PO4)2 D、NH4H2PO4
A、该实验是将氢氧化钠溶液滴入到盛有稀硫酸的烧杯中 B、b点表示稀硫酸和氢氧化钠溶液恰好完全反应 C、图中c点所示溶液中含有两种溶质 D、该反应的实质是H+和OH-结合生成H2O10. 钾肥有增强植物抗倒伏能力的功能。下列物质能用作钾肥的是( )A、CO(NH2)2 B、K2SO4 C、Ca3(PO4)2 D、NH4H2PO4二、填空题
-
11. 按要求从氢气、碳酸钠、甲烷、氢氧化钙、盐酸、硫酸六种物质中选择合适的物质。(1)、将其化学式填写在下列横线上。
①一种可燃性气体单质;
②天然气的主要成分;
③一种微溶于水的碱;
④水溶液显碱性的盐;
⑤一种挥发性酸。
(2)、2022年11月29日晚,我国申报的“中国传统制茶技艺及其相关习俗”在摩洛哥拉巴特召开的联合国教科文组织保护非物质文化遗产政府间委员会第17届常会上通过评审,列入联合国教科文组织人类非物质文化遗产代表作名录。自古以来,中国人就种茶、采茶、制茶和饮茶,发展出绿茶、黄茶、黑茶、白茶、乌龙茶、红茶六大茶类及花茶等再加工茶,2000多种茶品供人饮用与分享。①茶叶中的茶多酚,有较好的抗癌、防治心血管病和抗辐射作用。EGCG(分子式为C22H18O11)是茶多酚中的一种主要成分,C22H18O11由种元素组成,属于(填“混合物”“纯净物”“化合物”“氧化物”中的两项)。

②茶叶中含有咖啡因(分子式为C8H10O2N4),咖啡因具有兴奋中枢神经、消除疲劳、帮助消化等功效。在咖啡因中,每个分子共含有个原子,碳元素与氧元素的质量之比为(填最简整数比)。
③保护环境,健康生活。下列有关饮品的说法错误的是(填选项序号之一)。
A.喝碳酸饮料代替喝水 B.适量喝茶有益身体健康
C.过量饮酒对身体有害 D.喝牛奶能补充钙元素
12. 氢氧化钠固体吸收而潮解,氢氧化钠暴露在空气中易变质,用化学方程式表示 。在生活中氧化钙常用做食品干燥剂,其原理用化学方程式表示。13. 下列物质组合能发生复分解反应的有。(填序号)①K2CO3+CaCl2
②H2SO4+KCl
③CuO+HCl
④Fe+CuSO4
⑤CO2+NaOH
⑥K2SO4+BaCl2
⑦BaCO3+NaOH
14. 长期盛放澄清石灰水的试剂瓶内壁往往附着一层白色固体.这层白色固体是怎样形成的;主要成分是什么;石灰水用完以后,如何除去瓶壁上的白色固体;写出有关反应的化学方程式。15. 酸、碱、盐的溶解性表是学习化学的重要工具之一。下表是部分酸、碱、盐在水中的溶解性(20℃),请回答下列问题。阴离子
阳离子
OH-
NO3-
CO32-
Cl-
K+
溶
溶
溶
溶
Ba2+
溶
溶
不
溶
Cu2+
不
溶
不
溶
(1)、上述阴、阳离子形成不溶性碱的化学式为 , 形成复合肥料的化学式为。(2)、KOH溶液和Ba(NO3)2溶液(填“能“或“不能“)反应,理由是。(3)、下列各组离子在水溶液中能大量共存的是_______________ 。A、OH-、H+、Ba2+、NO B、OH-、Ba2+、K+、Cl- C、CO 、K+、Ba2+、Cl- D、CO 、Cu2+、NO 、K+三、简答题
-
16. 有三种白色粉末,分别是硝酸铵、硫酸铵和尿素,请设计一个实验方案,把这三种物质区分开来.简要写出实验的操作、现象和结论.17. 学习了单质、氧化物、酸、碱、盐的性质后,发现有很多不同类别的物质在发生反应时都有盐生成(其它物质省略),如图所示。请回答:
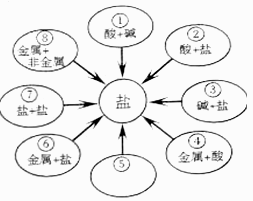 (1)、若盐是硫酸钾,则①中发生反应的化学方程式为。
(1)、若盐是硫酸钾,则①中发生反应的化学方程式为。
(2)、若盐是氯化亚铁,则在已显示的变化中可以通过置换反应来实现的有(填序号)。(3)、若盐是硝酸铜,由⑦来实现的化学方程式为:。(4)、图中⑤处应补充的文字是(写一种,不能与图中已有信息重复)。四、综合题
-
18. 为了除去食盐(主要成分为NaCl)样品中含有少量的氯化镁和硫酸钠杂质,某学生根据氯碱工业中精制食盐水的基本原理,运用所学知识设计了如图所示①至⑤步除杂方案:

请根据上述除杂方案,回答下列问题:
(1)、沉淀甲是;滤液C中的溶质是;操作⑤中加入过量盐酸的作用是。(2)、若在操作②中改为加过量的KOH溶液,固体丁中可能含有的杂质是。五、实验探究题
-
19. 某兴趣小组的同学为了探究某些酸碱盐之间的反应,进行以下实验:(1)、【设计实验1】
实验操作
实验现象
实验结论
把稀盐酸滴入分别盛有硝酸银、氢氧化钠、碳酸钠和硫酸钠溶液的四只烧杯中。
硝酸银溶液烧杯中有白色沉淀
硝酸银能和盐酸反应,反应的方程式为:
氢氧化钠、硫酸钠中均无现象
不能确定氢氧化钠、硫酸钠是否能和盐酸反应
碳酸钠溶液烧杯中
碳酸钠能和稀盐酸反应
(2)、【实验讨论】甲同学判断稀盐酸和硫酸钠溶液不能发生反应,他的依据是。
(3)、【提出问题】如何设计实验验证盐酸与氢氧化钠能发生化学反应?【设计实验2】
实验操作
预期实验现象
实验结论
步骤1:将2滴酚酞试液滴入氢氧化钠溶液中并振荡
溶液呈
盐酸与氢氧化钠能发生化学反应
步骤2:向步骤1所得溶液中逐滴滴加稀盐酸
(4)、【实验讨论】请你评价该实验方案是否可行(填写“可以”或“不可以”)。
(5)、【总结提升】稀盐酸与氢氧化钠溶液反应的微观示意图如图所示。
从微观角度分析,该反应的实质是。
(6)、通过以上实验分析,对于无明显现象的反应,验证反应发生的思路可以是:①验证生成物是否存在;
②验证是否消失。
(7)、【拓展探究】某小组同学在实验过程中,取用氢氧化钠溶液和碳酸钠溶液时标签忘记贴了。小明说用酚酞试剂检测一下,小红提出这个方案不行。你认为他们谁说的合理 , 并说明理由。
20. 为探究盐酸的化学性质,某化学小组做了如下实验。 (1)、上述反应中无明显现象的为(填字母序号,下同),有白色沉淀出现的是;B试管中所发生反应的化学方程式为。(2)、将反应后D和E试管中的废液倒入一个洁净的烧杯中,观察到烧杯中先有气泡产生,后有白色沉淀出现。将烧杯中的混合物过滤,得到白色沉淀和无色滤液。同学们对滤液中溶质的成分进行探究。
(1)、上述反应中无明显现象的为(填字母序号,下同),有白色沉淀出现的是;B试管中所发生反应的化学方程式为。(2)、将反应后D和E试管中的废液倒入一个洁净的烧杯中,观察到烧杯中先有气泡产生,后有白色沉淀出现。将烧杯中的混合物过滤,得到白色沉淀和无色滤液。同学们对滤液中溶质的成分进行探究。【提出问题】滤液中溶质的成分是什么?
【假设与猜想】
猜想一:NaCl
猜想二:NaCl和CaCl2
猜想三:NaCl、Ca(OH)2和HCl
猜想四:。
(3)、【讨论与交流】经讨论同学们一致认为猜想是错误的。(4)、【实验与结论】实验步骤
实验现象
实验结论
取少量滤液于试管中,滴加适量碳酸钠溶液
无现象
猜想四成立
取少量滤液于试管中,滴加适量
-