陕西省延安市富县2022-2023学年九年级上学期期末化学试题
试卷更新日期:2023-03-22 类型:期末考试
一、单选题
-
1. 臭氧(O3)主要分布在距离地面10~25km的高空,能吸收大部分紫外线,保护地球生物。它属于( )A、氧化物 B、单质 C、化合物 D、混合物2. 下列气体在空气中达到一定的体积分数,遇明火不可能发生爆炸的是( )A、天然气 B、氢气 C、氮气 D、一氧化碳3. 物质的性质决定其用途。下列物质的性质与其用途相匹配的是( )A、稀有气体化学性质不活泼,用作焊接金属的保护气 B、氧气有助燃性,用于医疗急救 C、石墨具有导电性,用于制铅笔芯 D、金刚石无色透明,用于切割玻璃4. 正确的实验操作是实验成功的保证。下列实验操作正确的是( )A、加入锌粒
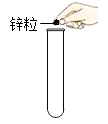 B、点燃酒精灯
B、点燃酒精灯 C、连接仪器
C、连接仪器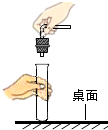 D、读取液体体积
D、读取液体体积 5. 科学家利用锗生产出世界上最灵活的晶体管,这种新型自适应晶体管可以在运行时动态切换,能执行不同的逻辑任务。锗在元素周期表中的部分信息及原子结构示意图如图所示,下列说法错误的是( )
5. 科学家利用锗生产出世界上最灵活的晶体管,这种新型自适应晶体管可以在运行时动态切换,能执行不同的逻辑任务。锗在元素周期表中的部分信息及原子结构示意图如图所示,下列说法错误的是( )
 A、锗属于金属元素 B、锗元素位于元素周期表第四周期 C、x的数值是2 D、锗原子的中子数是326. 下列关于灭火的方法及原理都正确的是( )A、吹灭蜡烛,原理是隔绝氧气 B、用高压水枪灭火,原理是降低可燃物的着火点 C、为防止森林大火蔓延可开辟隔离带,原理是清除可燃物 D、电器着火用水扑灭,原理是降低温度至可燃物的着火点以下7. 中国芯片蚀刻技术国际领先。NF3进行硅芯片蚀刻时的产物均为气体,在蚀刻物表面不留任何残留物。该反应的微观示意图如下,下列说法错误的是( )
A、锗属于金属元素 B、锗元素位于元素周期表第四周期 C、x的数值是2 D、锗原子的中子数是326. 下列关于灭火的方法及原理都正确的是( )A、吹灭蜡烛,原理是隔绝氧气 B、用高压水枪灭火,原理是降低可燃物的着火点 C、为防止森林大火蔓延可开辟隔离带,原理是清除可燃物 D、电器着火用水扑灭,原理是降低温度至可燃物的着火点以下7. 中国芯片蚀刻技术国际领先。NF3进行硅芯片蚀刻时的产物均为气体,在蚀刻物表面不留任何残留物。该反应的微观示意图如下,下列说法错误的是( ) A、该反应前后原子的数目不变 B、丙中硅、氟元素的质量比为7:19 C、空气中物质丁的体积分数约为78% D、该反应后生成的丙和丁的微粒数之比为1:18. 下列实验设计不能达到其对应实验目的的是( )
A、该反应前后原子的数目不变 B、丙中硅、氟元素的质量比为7:19 C、空气中物质丁的体积分数约为78% D、该反应后生成的丙和丁的微粒数之比为1:18. 下列实验设计不能达到其对应实验目的的是( )选项
A
B
C
D
实验设计




实验目的
测定空气里氧气的含量
验证甲烷中含有氢元素
验证面粉在一定条件下能爆炸
验证质量守恒定律
A、A B、B C、C D、D9. 化学兴趣小组为了探究微粒的性质,按图示进行实验,并借助传感设备测得U形管a、b中氨气浓度随时间变化的曲线(氨气极易溶于水)。下列关于该实验的说法中正确的是( ) A、曲线X对应的U形管为b B、湿棉花的作用是吸收氨气,减少氨气对空气的污染 C、0~1min,氨气浓度为零是因为微粒静止不动 D、该实验不能证明微粒运动速率与温度有关
A、曲线X对应的U形管为b B、湿棉花的作用是吸收氨气,减少氨气对空气的污染 C、0~1min,氨气浓度为零是因为微粒静止不动 D、该实验不能证明微粒运动速率与温度有关二、填空题
-
10. 2022年6月5日是第51个世界环境日,中国的主题为“共建清洁美丽世界”。(1)、化石燃料是(选填“可”或“不可”)再生能源。(2)、实现碳中和的重要方式之一是升级能源消费方式,请写出一种新能源:。(3)、在汽油中加入适量乙醇作为汽车燃料,可减少汽车尾气污染。乙醇完全燃烧的化学方程式为。11. 化学与生产、生活密切相关。(1)、生活中常用的方法降低水的硬度,同时又可以杀菌消毒。(2)、煤作为传统燃料,生活中把煤制成蜂窝状,其目的是。(3)、肼-空气燃料电池有望应用于汽车工业,其原理是 , 则X的化学式为。12. 化学用语是学习化学的工具,请用化学用语填空。(1)、2个氢原子:。(2)、保持二氧化硫化学性质的最小粒子:。(3)、标出氯酸钠(NaClO3)中氯元素的化合价:。
三、综合题
-
13. 已知A~E是初中化学常见的5种物质,它们之间的转化关系如图所示(“→”表示反应可一步实现,“____”表示物质间能相互反应,部分物质和反应条件略去)。已知:A、B均为黑色固体,D是造成温室效应的主要气体,E溶液能使紫色石蕊溶液变红。
 (1)、E的化学式是。(2)、A-C反应的化学方程式为。(3)、B-D反应的过程会(选填“吸收”或“放出”)热量。14. “嫦娥五号”带回的月壤中含有大量的钛铁矿(主要成分为FeTiO3)。科学家设想的有关人类利用月壤资源的流程图如下。回答下列问题:
(1)、E的化学式是。(2)、A-C反应的化学方程式为。(3)、B-D反应的过程会(选填“吸收”或“放出”)热量。14. “嫦娥五号”带回的月壤中含有大量的钛铁矿(主要成分为FeTiO3)。科学家设想的有关人类利用月壤资源的流程图如下。回答下列问题: (1)、步骤I中获得的金属有Ti和。(2)、步骤II中发生反应的化学方程式为。(3)、步骤III中发生反应的基本反应类型是。(4)、上述流程中可循环使用的物质是。15. 学习小组的同学利用下图所示实验装置探究燃烧的条件。已知白磷的着火点为40℃。
(1)、步骤I中获得的金属有Ti和。(2)、步骤II中发生反应的化学方程式为。(3)、步骤III中发生反应的基本反应类型是。(4)、上述流程中可循环使用的物质是。15. 学习小组的同学利用下图所示实验装置探究燃烧的条件。已知白磷的着火点为40℃。 (1)、实验前,打开K1、关闭K2或者打开K2、关闭K1 , 分别向上拉动甲处、丁处注射器的活塞,均能出现的现象,说明装置气密性良好。(2)、将装有适量白磷的具支试管放入20℃的冷水中,打开K1、关闭K2 , 往甲处锥形瓶中注入适量的过氧化氢溶液,乙处白磷未燃烧的原因是。(3)、关闭K1、打开K2 , 往丁处锥形瓶中注入适量的稀盐酸,使乙处的白磷与二氧化碳充分接触;然后将乙处的冷水换成80℃的热水,白磷不燃烧,这样设计的目的是。(4)、打开K1 , 关闭K2 , 往甲处锥形瓶中注入适量过氧化氢溶液,一段时间后乙处白磷燃烧,白磷燃烧的现象是;此时再关闭K1、打开K2 , 往丁处锥形瓶中注入适量的稀盐酸,白磷熄灭,体现了二氧化碳的化学性质。16. 下图是实验室制取气体的常用装置。
(1)、实验前,打开K1、关闭K2或者打开K2、关闭K1 , 分别向上拉动甲处、丁处注射器的活塞,均能出现的现象,说明装置气密性良好。(2)、将装有适量白磷的具支试管放入20℃的冷水中,打开K1、关闭K2 , 往甲处锥形瓶中注入适量的过氧化氢溶液,乙处白磷未燃烧的原因是。(3)、关闭K1、打开K2 , 往丁处锥形瓶中注入适量的稀盐酸,使乙处的白磷与二氧化碳充分接触;然后将乙处的冷水换成80℃的热水,白磷不燃烧,这样设计的目的是。(4)、打开K1 , 关闭K2 , 往甲处锥形瓶中注入适量过氧化氢溶液,一段时间后乙处白磷燃烧,白磷燃烧的现象是;此时再关闭K1、打开K2 , 往丁处锥形瓶中注入适量的稀盐酸,白磷熄灭,体现了二氧化碳的化学性质。16. 下图是实验室制取气体的常用装置。 (1)、写出标有字母a的仪器名称:。(2)、实验室用高锰酸钾制取并收集一瓶较干燥的氧气,应选择的装置组合是(填字母),发生反应的化学方程式为。(3)、装置F中集气瓶内放入少量水的目的是;能证明铁丝燃烧是化学变化的现象是。17. 学习小组的同学在学习了二氧化碳制取的研究课题后,拓展学习与探究了二氧化碳的收集方法。(1)、【知识回顾】实验室制取二氧化碳的化学方程式为。(2)、【提出问题】对于二氧化碳的收集方法,学习小组的甲同学认为只能用向上排空气法收集,乙同学认为还可以采用排水法收集。
(1)、写出标有字母a的仪器名称:。(2)、实验室用高锰酸钾制取并收集一瓶较干燥的氧气,应选择的装置组合是(填字母),发生反应的化学方程式为。(3)、装置F中集气瓶内放入少量水的目的是;能证明铁丝燃烧是化学变化的现象是。17. 学习小组的同学在学习了二氧化碳制取的研究课题后,拓展学习与探究了二氧化碳的收集方法。(1)、【知识回顾】实验室制取二氧化碳的化学方程式为。(2)、【提出问题】对于二氧化碳的收集方法,学习小组的甲同学认为只能用向上排空气法收集,乙同学认为还可以采用排水法收集。【查阅资料】氢氧化钠溶液能与二氧化碳反应,能有效吸收二氧化碳。
【实验探究】步骤I:小组同学利用右图所示装置制取二氧化碳,以锥形瓶作收集装置,并采用以下三种方法收集。

方法一:当反应装置开始产生二氧化碳15s后,用排水法收集二氧化碳备用。
方法二:当反应装置开始产生二氧化碳15s后,用向上排空气法收集二氧化碳备用。
方法三:当反应装置开始产生二氧化碳15s后,用向上排空气法收集二氧化碳,将燃着的木条放在锥形瓶口,待木条熄灭(视二氧化碳收集满)立即盖上玻璃片备用。
步骤Ⅱ:将一定浓度的足量氢氧化钠溶液分别滴入以上锥形瓶中,用压强传感器测得瓶内压强变化情况如下图所示,用二氧化碳传感器测得瓶内二氧化碳的纯度如下表。

方法
一
二
三
CO2纯度/%
91.1
69.5
61.9
【实验结论】根据数据可知(选填“甲”或“乙”)同学的说法不正确。
(3)、【反思交流】①收集二氧化碳时,15s以后再收集的目的是。
②根据实验数据分析,用燃着的木条检验二氧化碳收集满(选填“准确”或“不准确”),理由是。
(4)、【拓展延伸】结合上图和表中数据分析,除了上述结论外,还可以得到的结论是(写一条即可)。四、计算题
-
18. 氯酸钾在二氧化锰作催化剂并加热的条件下,能较快地分解生成氯化钾和氧气,下图是某次实验中固体的质量变化。
 (1)、实验后生成氧气的质量为g。(2)、计算参加反应的氯酸钾的质量。
(1)、实验后生成氧气的质量为g。(2)、计算参加反应的氯酸钾的质量。