2022--2023人教版九年级化学第八单元 金属和金属材料 单元测试提高训练
试卷更新日期:2023-03-14 类型:单元试卷
一、单选题
-
1. 生活生产中用到各种各样的材料。下列生活用品中由金属材料制成的是( )A、玻璃水杯 B、不锈钢菜刀 C、陶瓷碗 D、塑料桶2. 北斗系统的全面建成彰显了中国航天的力量。在航天科技中运用了大量金属材料,下列有关金属材料的说法错误的是A、纯金属和合金都是金属材料 B、生铁的主要成分是碳 C、金制成金箔是利用了金具有良好的延展性 D、一般来说,合金比组成它的纯金属硬度大3. 下列有关合金的说法错误的是( )A、合金中不一定含有非金属 B、武德合金熔点高做保险丝 C、人类最早使用的合金是青铜 D、合金是具有特殊性能的“新型金属”4. 下列化学方程式中书写正确且属于置换反应的是( )A、氢气还原氧化铜:H2+CuOCu+H2O B、甲烷燃烧:CH4+2O2CO2+2H2O C、生石灰与水的反应:CaO+H2O=Ca(OH)2 D、用氯酸钾制取氧气:2KClO32KCl+ 3O2↑5. 王同学想比较两种未知金属M、N和金属铝的活动性大小关系。他将M、N、铝三种金属粉末分别投入6.3%稀盐酸中,观察到金属M、铝粉表面有气泡产生,金属N无明显现象。另取一小块金属M投入硫酸铝溶液中,没有明显现象。据此判断三种金属的活动性顺序由强到弱的是( )A、铝>N>M B、N>M>铝 C、M>铝>N D、铝>M>N6. 金属材料的广泛应用,极大地促进了社会的发展。下列关于金属材料的说法中,错误的是( )A、纯金属的硬度一般比它们的合金硬度更高 B、地壳中含量最多的金属元素是铝元素 C、钢铁表面刷油漆可以防止钢铁生锈 D、生铁和钢是含碳量不同的两种铁合金7. 探究Zn、Fe、Ag三种金属的活动性顺序,下列试剂的选择方案可行的是( )A、Zn、Ag、FeSO4溶液 B、ZnSO4溶液、FeSO4溶液、Ag C、Fe、Ag、ZnSO4溶液 D、FeSO4溶液、AgNO3溶液、Zn8. 银汞合金是目前广泛使用的一种补牙材料。银汞合金中除了银、汞外,还含有锌、锡、铜等金属。请判断下列有关银汞合金的推测正确的是( )
①银汞合金是一种新型化合物
②银汞合金是一种金属材料
③银汞合金的硬度比锡的大
④银汞合金的毒性一定远低于汞的毒性
⑤组成银汞合金的各成分之间发生了化学反应
A、①②③ B、②③④ C、①②③④ D、②③④⑤9. 现有等质量的甲、乙两种金属,分别放入溶质质量分数相同的足量稀硫酸中,产生氢气的质量与时间的关系如图(已知甲、乙在生成物中的化合价均为+2 价).则下列说法错误的是( )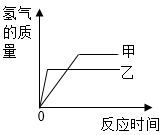 A、生成氢气的质量:甲>乙 B、相对原子质量:甲>乙 C、金属活泼性:乙>甲 D、消耗稀硫酸的质量:甲>乙10. 把一根洁净的铁钉放在稀硫酸中,下列叙述错误的是( )A、铁钉的质量减轻 B、溶液的质量减轻 C、在铁钉表面产生气泡 D、溶液由无色逐渐变为浅绿色
A、生成氢气的质量:甲>乙 B、相对原子质量:甲>乙 C、金属活泼性:乙>甲 D、消耗稀硫酸的质量:甲>乙10. 把一根洁净的铁钉放在稀硫酸中,下列叙述错误的是( )A、铁钉的质量减轻 B、溶液的质量减轻 C、在铁钉表面产生气泡 D、溶液由无色逐渐变为浅绿色二、填空题
-
11. 化学知识渗透到社会方方面面。(1)、2021年12月9日,“天宫课堂"开讲,神舟十三号乘组航天员霍志刚、王亚平、叶光富在中国空间站进行了太空授课。
①王亚平说"水是生命之源,人类的生活离不开水"。"空间站里的每一滴水都会物尽其用”,写出一条在生活中让水物尽其用的做法;
②科学进步,空间站实现了水的再生。请写出一个有水生成的置换反应;
(2)、2022年2月7日,任子威以1分26秒768获得北京冬奥会短道速滑男子1000米冠军,实现了中国队在该项目上冬奥金牌零的突破。冰刀是装在冰鞋底下的钢制刀状物,冰刀接触的冰熔化成水,使冰刀与冰之间的摩擦力降得更低,更有利于冰鞋的滑动。①冰刀属于(选填“有机合成材料”、“金属材料”或“复合材料”)。
②钢比纯铁的硬度(填“大”或“小”)。
12. 纽扣电池是生活中常用的电源,下图是银锌纽扣电池的构造示意图,回答下列问题。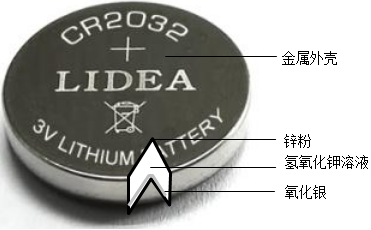 (1)、纽扣电池的外壳可以加工得很薄,说明金属具有性。(2)、氧化银加热分解可以得到两种单质,其化学反应方程式为。(3)、该电池中涉及的铁、锌、银三种金属,它们的金属活动性由强到弱的顺序是 , 为了验证该结论,某同学向质量、外形相同的铁片、锌片、银片中分别加入足量15%的稀盐酸,以下现象中不能成为该结论证据的是(填序号)。
(1)、纽扣电池的外壳可以加工得很薄,说明金属具有性。(2)、氧化银加热分解可以得到两种单质,其化学反应方程式为。(3)、该电池中涉及的铁、锌、银三种金属,它们的金属活动性由强到弱的顺序是 , 为了验证该结论,某同学向质量、外形相同的铁片、锌片、银片中分别加入足量15%的稀盐酸,以下现象中不能成为该结论证据的是(填序号)。A、表面没有气泡生成
B、铁表面最终生成气体的总量比锌多
C、铁表面产生气泡的速率比锌慢
13. 铝是大自然赐予人类的宝物,是现代文明不可缺少的物质基础。(1)、人类冶炼和使用金属铝的时间较晚。可能是因为(填字母)。a.地壳中铝元素含量少
b.冶炼铝的技术要求高
(2)、用铝锂合金制造“神舟号”航天飞船的一些部件,主要是利用其强度高、耐腐蚀和(写一条)等性质。高温下,铝与Li2O反应可置换出金属锂,写出该反应的化学方程式:。(3)、用砂纸去除铝片表面的氧化膜,将其浸人硫酸铜溶液中,一段时间后,观察到铝片表面有红色物质析出,并有气泡产生,经检验气体为氢气。①写出生成红色物质的化学方程式:。
②硫酸铜溶液中的阳离子有(填离子符号)。
(4)、原子簇是若干个原子的聚集体,有望开发成新材料。某铝原子簇由13个铝原子构成,其最外层电子数的总和为40时相对稳定。写出该稳定铝原子簇的微粒符号:。(铝原子的结构示意图为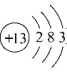 ) 14. 金属的用途很广,我们应该节约和保护金属资源,请用所学化学知识回答下列问题:(1)、铁制品长期裸露在室外易生锈,铁生锈实际上是铁与空气中的等发生化学反应的过程;(2)、为了预防铁制品生锈,我们常在其表面镀一层抗腐蚀的金属,但在镀金属之前,先要除去铁制品表面的铁锈。用稀盐酸除去铁锈的化学反应方程式是。(3)、将X、Z、Y三种金属片分别放入稀硫酸中,Y、Z表面有气泡产生,X没有明显现象,再把Y、Z分别放入FeSO4溶液中,发现放入Y的FeSO4溶液逐渐变成无色,而放入Z的FeSO4溶液和Z表面都没有明显现象。根据上述实验判断,X、Y、Z三种金属的活动性由强到弱的顺序是。15. 金属材料在生活中被广泛应用,回答下列问题。(1)、下列说法正确的是___(填序号)A、武德合金做保险丝是利用了合金熔点变低 B、“银粉漆”(铝粉)可涂在铁栏杆上防锈,这是因为铝化学性质稳定 C、生铁和钢的性能不同是由于它们的含碳量不同 D、铝制品表面应常用钢刷擦洗(2)、某同学用如下药品探究铝、镁的活动性,能否达到实验目的(填能或不能)。
) 14. 金属的用途很广,我们应该节约和保护金属资源,请用所学化学知识回答下列问题:(1)、铁制品长期裸露在室外易生锈,铁生锈实际上是铁与空气中的等发生化学反应的过程;(2)、为了预防铁制品生锈,我们常在其表面镀一层抗腐蚀的金属,但在镀金属之前,先要除去铁制品表面的铁锈。用稀盐酸除去铁锈的化学反应方程式是。(3)、将X、Z、Y三种金属片分别放入稀硫酸中,Y、Z表面有气泡产生,X没有明显现象,再把Y、Z分别放入FeSO4溶液中,发现放入Y的FeSO4溶液逐渐变成无色,而放入Z的FeSO4溶液和Z表面都没有明显现象。根据上述实验判断,X、Y、Z三种金属的活动性由强到弱的顺序是。15. 金属材料在生活中被广泛应用,回答下列问题。(1)、下列说法正确的是___(填序号)A、武德合金做保险丝是利用了合金熔点变低 B、“银粉漆”(铝粉)可涂在铁栏杆上防锈,这是因为铝化学性质稳定 C、生铁和钢的性能不同是由于它们的含碳量不同 D、铝制品表面应常用钢刷擦洗(2)、某同学用如下药品探究铝、镁的活动性,能否达到实验目的(填能或不能)。金属种类
金属质量
酸
铝片
1g
10mL5%稀盐酸
镁片
1g
10mL5%稀硫酸
(3)、写出铜和硝酸银溶液反应的化学方程式。(4)、向Zn(NO3)2、AgNO3、Cu(NO3)2混合溶液中加入一些铁粉,完全反应后过滤.取滤渣于试管中,加稀盐酸,有气体生成.则滤渣的成分是。三、简答题
-
16. 校园里的单双杠、篮球架、广场内的健身器材等铁制品由于表面的油漆或涂层脱落易产生铁锈,请你根据所学知识,指出铁生锈的条件是什么?17. 铝、铁、铜是人类广泛使用的三种金属,与我们的生活息息相关。(1)、在空气中铝制品更耐腐蚀,其原因是;(2)、用下列试剂验证这三种金属的活动性顺序,能一次实验达到目的的是___________________________________;A、硫酸铝溶液 B、硫酸亚铁溶液 C、硫酸铜溶液(3)、生铁与钢是两种常用的合金,二者性能不同的原因是。
四、综合题
-
18. 金属材料在生产、生活中具有广泛的应用。(1)、铁锅用来炒菜,主要是利用铁的性。(2)、铝合金是目前使用比较广泛的金属材料,街道上的垃圾桶的内胆更合适用铝合金的原因是。(用化学方程式表示)(3)、目前科学家正在研究以“氢能炼钢”替代“焦炭炼钢”。这两种工艺相比,“氢能炼钢”的主要优点有。(4)、防止钢铁制品的锈蚀可避免财产损失,写一条防止钢铁制品腐蚀的措施:。
五、实验探究题
-
19. 某兴趣小组想通过实验对铁、铜、锌三种金属的活动性强弱进行探究,现提供的药品有:铁粉、铜丝、锌粒、20%稀硫酸、CuSO4溶液、ZnSO4溶液、FeSO4溶液。(1)、甲同学设计用铁粉、铜丝、锌粒分别与等质量20%稀硫酸进行实验,立刻有同学提出反对,理由。(2)、乙同学设计如下方案进行实验:
实验步骤

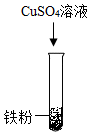
实验现象
无明显变化
。
实验结论
。
(3)、发生反应的化学方程式为。(4)、丙同学将两支试管中的物质倒在一个洁净的烧杯中,发现烧杯内的红色固体明显增多。充分反应后过滤,同学们分别对滤渣和滤液的成分展开了探究。【作出猜想】猜想一:滤渣中一定有铜,猜想二:。
(5)、【进行实验】实验步骤
实验现象
实验结论
向滤渣中加入20%稀硫酸
有气泡产生
猜想二正确
【交流讨论】
滤液中一定含有的溶质是(填化学式)。
(6)、丁同学掌握了比较金属活动性的正确方法后,他选择了另组试剂 , 进一步验证了三种金属的活动性强弱。20. 1949 年 10 月 1 日中华人民共和国成立,在开国大典上首次实现了电动升国旗。(1)、为保证国旗不被卷入,要求旗杆上的“阻断球”要足够结实,不易被撞裂。在“阻断球” 的制作过程中不仅使用了铁,还熔入了一定比例的铬(Cr)等金属,这是利用了合金的性质。在常见金属活动性顺序中没有铬,同学们决定对铬与常见金属镁和铜的活动性强弱进行探究。(2)、(查阅资料)铬(Cr)是一种银白色金属,其化合物硫酸亚铬(CrSO4)的水溶液呈蓝色。硫酸亚铬中铬元素的化合价为。(3)、(提出猜想)三种金属的活动性强弱为:猜想一:Cr>Mg>Cu; 猜想二:;猜想三:Mg>Cu>Cr
(4)、(进行实验)实验步骤
实验现象
实验结论
①分别向盛有 Cr 和 Cu 两种金属片的试管中加入同体积同浓度的稀硫酸
只有盛的试管中有气泡产生,并得到蓝色溶液
猜想三不正确
②向盛有硫酸镁溶液的试管中加入金属Cr
无明显现象
猜想正确
(5)、(交流与讨论)①实验前所用的金属片都需用砂纸打磨,目的是。
②实验①中发生反应的化学方程式为。
③结合探究结论,有同学提出上述三个实验可进行优化,只需选择三种药品,即可判断金属的活动性强弱。合理的选择是(选填序号)。
①硫酸镁溶液;②硫酸亚铬溶液;③硫酸铜溶液;④镁片;⑤铬片;⑥铜片
(6)、(拓展延伸)若将实验步骤①和②中反应后的混合物倒入同一烧杯中,搅拌、过滤, 得到固体 x 和溶液 y,则:①溶液 y 中溶质的成分(选填序号)。
A 一定有 MgSO4 B 一定有CrSO4
C 可能有 H2SO4 D 可能有CuSO4
②过滤过程中,用到的玻璃仪器有烧杯、玻璃棒和 , 其中玻璃棒的作用是。
-