广东省广州市荔湾区2022-2023学年九年级上学期期末化学试题
试卷更新日期:2023-03-14 类型:期末考试
一、单选题
-
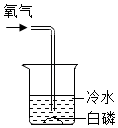
1. 我国古代的四大发明,是中国人智慧和辛勤劳动的成果。下列与四大发明相关的应用中,涉及化学变化的是( )A、指南针一海上导航 B、火药一鞭炮鸣放 C、印刷术一书籍出版 D、造纸术一文字书写2. 空气是人类生活生产活动中的重要资源。下列用到的气体不是来自空气的是( )A、用于飞艇的氦气 B、用于磁悬浮列车的氮气 C、用于氢氧燃料电池的氢气 D、用于医疗急救的氧气3. 紫花前胡醇(C14H14O4)可从中药材当归和白芷中提取,能提高人体免疫力。关于紫花前胡醇,下列说法正确的是( )A、相对分子质量为 (12×14+1×14+16×4) g B、C,H,O三种元素的质量比为 12︰1︰16 C、C,H,O三种原子的个数比为7︰7︰2 D、碳元素的质量分数为=4. 用下图装置可验证空气中O2的含量。下列现象能表明O2含量的是( )
 A、集气瓶中产生大量白烟 B、红磷燃烧一段时间后熄灭 C、烧杯中的水倒吸进入集气瓶 D、集气瓶中水面最终上升至1处5. 下列实验操作错误的是( )A、熄灭酒精灯时,用灯帽盖灭火焰 B、进行过滤时,用玻璃棒在过滤器中不断搅拌 C、倾倒液体时,试剂瓶瓶口紧挨着试管口 D、用试管夹持试管时,应由试管底部套上、取下6. 下列物质的性质与用途表述没有直接联系的是( )
A、集气瓶中产生大量白烟 B、红磷燃烧一段时间后熄灭 C、烧杯中的水倒吸进入集气瓶 D、集气瓶中水面最终上升至1处5. 下列实验操作错误的是( )A、熄灭酒精灯时,用灯帽盖灭火焰 B、进行过滤时,用玻璃棒在过滤器中不断搅拌 C、倾倒液体时,试剂瓶瓶口紧挨着试管口 D、用试管夹持试管时,应由试管底部套上、取下6. 下列物质的性质与用途表述没有直接联系的是( )选项
性 质
用 途
A
CO2水溶液显酸性
CO2用作大棚蔬菜的气体肥料
B
活性炭有吸附性
红糖脱色制白糖
C
CO具有还原性
冶金工业炼铁
D
常温下碳的化学性质不活泼
用墨绘制字画
A、A B、B C、C D、D7. 关于水的净化,下列说法正确的是( )A、家用自来水是纯净物 B、明矾能促进水中悬浮杂质沉降 C、活性炭可以使硬水转化为软水 D、过滤可使海水转化为饮用水8. 下列说法错误的是( )A、煤中主要含有碳元素,还含有氢、硫等元素,煤是清洁燃料 B、煤作为燃料主要是利用碳元素和氧反应所放出的热量 C、煤燃烧产生的NO2和SO2都是形成酸雨的污染物 D、减少煤的使用有利于防止温室效应进一步增强9. 我国科研团队借助一种固体催化剂,在常温常压和可见光条件下合成了氨气,其过程如图所示。下列说法错误的是( ) A、氮气在一定条件下能发生化学反应 B、该反应前后有元素的化合价发生了变化 C、太阳能的利用能缓解化石能源耗尽的问题 D、该反应的化学方程式为N2 + H2ONH3 + O210. 中国锶光钟是由中国计量科学研究院研制的锶原子光晶格钟。下图为锶(Sr)原子的结构示意图,下列说法错误的是( )
A、氮气在一定条件下能发生化学反应 B、该反应前后有元素的化合价发生了变化 C、太阳能的利用能缓解化石能源耗尽的问题 D、该反应的化学方程式为N2 + H2ONH3 + O210. 中国锶光钟是由中国计量科学研究院研制的锶原子光晶格钟。下图为锶(Sr)原子的结构示意图,下列说法错误的是( ) A、锶原子核内的质子数为38 B、锶离子的离子符号为Sr2+ C、氯化锶的化学式为Sr2Cl D、锶原子的核外电子分5层排布11. 甲醇(CH3OH)是一种重要的化工原料,在生活生产中有广泛的应用价值。下图是利用CO2为原料制备甲醇的微观示意图。下列说法正确的是( )
A、锶原子核内的质子数为38 B、锶离子的离子符号为Sr2+ C、氯化锶的化学式为Sr2Cl D、锶原子的核外电子分5层排布11. 甲醇(CH3OH)是一种重要的化工原料,在生活生产中有广泛的应用价值。下图是利用CO2为原料制备甲醇的微观示意图。下列说法正确的是( ) A、该反应的反应物和生成物均为化合物 B、该反应另一种反应物的化学式是O2 C、反应中
A、该反应的反应物和生成物均为化合物 B、该反应另一种反应物的化学式是O2 C、反应中 和
和 按分子个数比1︰4进行反应
D、反应中生成
按分子个数比1︰4进行反应
D、反应中生成  与
与 的质量比为16︰9
12. 下列实验方案中,能达到目的的是( )
的质量比为16︰9
12. 下列实验方案中,能达到目的的是( )选项
实验目的
实验方案
A
鉴别生石灰和石灰石粉末
取样,分别加入少量水,触碰试管外壁
B
除去氧化铜中的少量碳粉
取样,加入适量水,过滤
C
除去CO2中含有的少量CO
将混合气体通入过量的氧气,点燃
D
除去H2中含有的少量CO
将混合气体通过灼热CuO
A、A B、B C、C D、D13. 用下图所示实验探究燃烧的条件,下列说法正确的是( )①
②
③
④



白磷不燃烧
白磷不燃烧
白磷不燃烧
白磷燃烧
A、对比①③说明燃烧的条件之一是可燃物接触氧气 B、对比①④说明燃烧的条件之一是需要有可燃物 C、对比①②说明燃烧的条件之一是温度达到可燃物的着火点 D、对比③④说明燃烧的条件之一是温度达到可燃物的着火点14. 下列实验操作、现象与结论均正确的是( )选项
实验操作
现象
结论
A
在甲烷火焰上方罩一个
冷而干燥的烧杯
烧杯内壁有无色液滴产生
甲烷含有碳元素和氢元素
B
用拇指堵住收集了H2的
试管口,靠近火焰,移开
拇指点火
发出尖锐爆鸣声
试管中H2不纯
C
将燃着的木条插入某瓶
无色气体中
木条熄灭
该瓶中气体是
CO2
D
常温下,将硫放入氧气中
剧烈燃烧,发出蓝紫色火焰
硫能与氧气反应
A、A B、B C、C D、D二、填空题
-
15. 中国航天事业取得了一系列辉煌的成就,标志着我国已跻身于世界航天强国。请回答下列问题:(1)、“嫦娥五号”探测器从月球采样返回。
经分析发现,“嫦娥五号”探测器带回的月球土壤与地球土壤的构成类似。月壤中含钛铁矿(主要成分为FeTiO3)、辉石(主要成分为CaAl2Si2O8)、橄榄石(主要成分为MgFeSiO4)等物质。
① FeTiO3中钛(Ti)元素的化合价为+4,则铁元素的化合价为。
② CaAl2Si2O8的氧化物形式可表示为CaO·Al2O3·2SiO2 , 则MgFeSiO4的氧化物形式可表示为。
(2)、“天问一号”探测器成功抵达火星。①“天问一号”是利用砷化镓(GaAs)太阳能电池作为动力。制取砷化镓的化学原理为:(CH3)3Ga + AsH3GaAs + 3X,则X的化学式为。
②火星表面呈黄褐色,是由于火星表面土壤中含有氧化铁等物质引起的。氧化铁中氧元素的质量分数为。
③火星拥有丰富的金属矿物和二氧化碳等资源。火星低层大气的主要成分
如下表:
气体成分
CO2
N2
Ar
O2
其他
体积分数/ %
95.32
2.7
1.6
0.13
0.25
若为满足人类未来在火星上生活,下列研究设想不合理的是(填字母)。
A.将CO2转化为O2 , 提高O2含量
B.将CO2分解转化为N2 , 提高N2含量
C.寻找水的存在和开发水循环技术
D.利用火星上的金属矿物冶炼金属
16. 水是一种重要的自然资源,是生活、生产必不可少的物质。实验甲是水的沸腾装置,实验乙是水的电解装置。
回答下列问题:
(1)、从微观角度分析,实验甲中A和B处的不同点是。(2)、实验乙发生了(填“化合”或“分解”)反应。请依照图中水的组成的微观示意图,画出实验乙的试管①和试管②中气体组成的微观示意图。三、综合题
-
17. 生活中常用草酸溶液除铁锈和瓷砖上的污渍。草酸晶体加热会发生如下 反应:H2C2O4·2H2OCO2↑+ CO↑+ 3H2O↑。实验小组的同学设计如下实验检验草酸分解后的产物。

已知:① 白色的无水硫酸铜遇水变蓝;② CO2能与NaOH溶液反应,CO不能与NaOH溶液反应
回答下列问题:
(1)、实验中证明有水生成的现象是。(2)、乙中澄清石灰水的作用是 , 该反应的化学方程式为。(3)、要证明有CO生成,在不连接其他装置的情况下,可进行的操作是。18. 根据下列装置回答下列问题:
已知:浓硫酸具有吸水性,可做干燥剂。
(1)、实验室加热KMnO4制取一瓶氧气用于性质实验。①可选用与(填字母)装置组合。首先检查装置的气密性,方法是:把导管口放入水中,然后 , 观察到导管口有气泡冒出,说明装置气密性良好。
②实验室用KMnO4制备O2的化学方程式是。若需制备1.6 g O2 , 至少需要消耗g KMnO4。
③ 如图所示,铁丝在氧气中燃烧,产生的现象是 , 装置中水的作用是。
 (2)、①实验室用金属锌与稀硫酸制取并收集干燥的H2 , 反应的化学方程式为 , 从A~F中选用装置的连接顺序为(填字母)。
(2)、①实验室用金属锌与稀硫酸制取并收集干燥的H2 , 反应的化学方程式为 , 从A~F中选用装置的连接顺序为(填字母)。②氢气的生产方法是制约其作为清洁能源广泛使用的原因之一,科学家根据生产方法提出“绿色”氢气和“有污染”的氢气的概念,下列方法可获得 “绿色”氢气的是(填字母)。
A.利用煤燃烧发电,再电解水
B.用矿石生产锌和硫酸,再相互反应
C.在催化剂作用下,利用太阳能光解水
D.利用风能、水力发电,再电解水
(3)、若用装置G收集甲烷(CH4),气体应从(填“a”或“b”)端进入。19. 我国提出2060年前实现碳中和,彰显了负责任大国的作为与担当。实现碳中和有多种途径。(1)、矿物质碳化封存:其反应之一是氧化镁与CO2反应生成碳酸镁,该反应的化学方程式为。(2)、海洋封存:原理是利用CO2在水等溶剂中的溶解性来吸收CO2。某实验小组利用下图装置探究CO2在水和食盐水(模拟海水)中的溶解情况:在相同条件下,分别用排水法、排食盐水法收集CO2 , 待收集100 mL CO2后,移出导管,每隔一段时间观察并记录量筒内CO2体积。

重复实验,所测数据平均值如下表:
时间/h
0
0.5
6
12
24
48
排水法时CO2体积/mL
100
98.5
85.5
77
66
59
排食盐水法时CO2体积/mL
100
99
93
90.5
89
88
①发生装置中反应的化学方程式为。
②由上表数据分析:
a.相同条件下,等体积的水和食盐水吸收CO2更多的是(填“水”或“食盐水”)。
b.能用排水法收集CO2的理由是。
20. 某化学兴趣小组研究影响过氧化氢分解快慢的因素,设计以下实验装置(夹持仪器略去,气密性良好)进行实验,在锥形瓶内放入MnO2 , 一次性加入10mL的H2O2溶液,测定并记录收集10 mL O2所用时间。
序号
温度
催化剂
H2O2溶液
浓度/ %
H2O2溶液
体积/ mL
10mLO2
所用时间/s
1
20℃
0.1 g MnO2
5
10
76
2
20℃
0.1 g MnO2
15
10
33
3
20℃
0
15
10
t3
4
50℃
0.1 g MnO2
5
10
62
5
50℃
0.1 g MnO2
15
10
t5
6
80℃
0.1 g MnO2
5
10
40
7
80℃
0.1 g MnO2
15
10
16
8
20℃
①
②
10
t8
(1)、MnO2催化过氧化氢分解的化学方程式是。(2)、该小组研究了哪些因素影响过氧化氢分解的快慢?。(3)、为了分析浓度对反应快慢的影响,可对比表中实验(填字母)。A.2和3 B.4和5 C.6和7 D.1和6(4)、根据实验数据反映出的规律,表中数值t5的合理范围是:< t5<。(5)、实验结束,若要将MnO2从混合物中分离出来,可采取的方法是。(6)、为了探究MnO2、Fe2O3两种不同催化剂对过氧化氢分解的催化效果,在实验1~7的基础上进行实验8,请补充完整实验8的有关数据:①;②。