广东省广州市番禺区2022-2023学年九年级上学期期末化学试题
试卷更新日期:2023-03-14 类型:期末考试
一、单选题
-
1. 中华文化博大精深,下列成语中一定包含化学变化的是( )A、木已成舟 B、水滴石穿 C、冰雪消融 D、钻木取火2. 空气是人类生产活动的重要资源。下列生活生产中用到的气体不是来自空气的是( )A、炼钢过程用到的氧气 B、磁悬浮列车用到的氮气 C、用于生产氮肥的氨气 D、制作电光源的稀有气体3. 下列操作中,能鉴别空气、氧气和二氧化碳三瓶气体的是( )A、观察气体颜色 B、插入燃着的木条 C、闻气体的气味 D、倒入澄清石灰水4. 某兴趣小组模拟自来水厂对浑浊的有色河水进行如下处理,下列说法正确的是( )
 A、明矾的作用是吸附杂质 B、①中液体无色澄清 C、②中液体一定为纯净物 D、若③中出现大量泡沫,则②中液体为硬水5. 锶(Sr)和氧(O)的原子结构示意图如图所示。下列推断正确的是( )
A、明矾的作用是吸附杂质 B、①中液体无色澄清 C、②中液体一定为纯净物 D、若③中出现大量泡沫,则②中液体为硬水5. 锶(Sr)和氧(O)的原子结构示意图如图所示。下列推断正确的是( ) A、Sr离子核外共有五个电子层 B、O原子在化学反应中易失去6个电子 C、Sr和O可形成化合物SrO D、Sr和O均属于非金属元素6. 金刚石和石墨是常见的碳单质,其结构如图所示。下列说法正确的是( )
A、Sr离子核外共有五个电子层 B、O原子在化学反应中易失去6个电子 C、Sr和O可形成化合物SrO D、Sr和O均属于非金属元素6. 金刚石和石墨是常见的碳单质,其结构如图所示。下列说法正确的是( )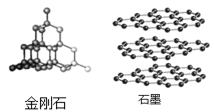 A、构成金刚石和石墨的原子结构不同 B、金刚石和石墨都有吸附性 C、1 g金刚石和1 g石墨所含原子数相同 D、石墨在氧气中能燃烧,但金刚石不能燃烧7. “长征5号”的助推器是用液氧、煤油作推进剂的,航空煤油可由优质石油分馏而来,十二烷(C12H26)是航空煤油中的成分之一,关于C12H26的说法正确的是( )A、十二烷分子由碳、氢两种元素组成 B、十二烷由12个碳原子和26个氢原子构成 C、十二烷中碳元素的质量分数计算式为 D、十二烷中碳元素与氢元素的质量比为12:268. 下列符号中,对“2”含义的理解正确的是( )A、2Ag:2个银元素 B、Ca2+:每个钙离子带有2个单位的正电荷 C、H2S:1个硫化氢分子中含有2个硫原子 D、中化学式上方的“-2”表示硫元素为-2价9. 我国古代典籍记载的“银针验毒”,涉及到反应 , 生成物X的化学式是( )A、AgHS B、Ag2S C、SO2 D、Ag2O10. 下列现象的微观解释中,错误的是A、“酒香不怕巷子深”--分子在不断的运动 B、1 滴水中水分子个数:--水分子很小 C、水烧开后易把壶盖冲起--温度升高,分子变大 D、天然气能被压入钢瓶中--气体分子间的间隔大,容易被压缩11. 某小组用如图所示装置探究二氧化碳的性质。下列说法正确的是( )
A、构成金刚石和石墨的原子结构不同 B、金刚石和石墨都有吸附性 C、1 g金刚石和1 g石墨所含原子数相同 D、石墨在氧气中能燃烧,但金刚石不能燃烧7. “长征5号”的助推器是用液氧、煤油作推进剂的,航空煤油可由优质石油分馏而来,十二烷(C12H26)是航空煤油中的成分之一,关于C12H26的说法正确的是( )A、十二烷分子由碳、氢两种元素组成 B、十二烷由12个碳原子和26个氢原子构成 C、十二烷中碳元素的质量分数计算式为 D、十二烷中碳元素与氢元素的质量比为12:268. 下列符号中,对“2”含义的理解正确的是( )A、2Ag:2个银元素 B、Ca2+:每个钙离子带有2个单位的正电荷 C、H2S:1个硫化氢分子中含有2个硫原子 D、中化学式上方的“-2”表示硫元素为-2价9. 我国古代典籍记载的“银针验毒”,涉及到反应 , 生成物X的化学式是( )A、AgHS B、Ag2S C、SO2 D、Ag2O10. 下列现象的微观解释中,错误的是A、“酒香不怕巷子深”--分子在不断的运动 B、1 滴水中水分子个数:--水分子很小 C、水烧开后易把壶盖冲起--温度升高,分子变大 D、天然气能被压入钢瓶中--气体分子间的间隔大,容易被压缩11. 某小组用如图所示装置探究二氧化碳的性质。下列说法正确的是( ) A、图1、图2实验中都是短的蜡烛先熄灭 B、“釜底抽薪”灭火的原理和图2实验中蜡烛熄灭的原理相同 C、图3实验证明二氧化碳与水反应生成了碳酸 D、图3实验中观察到试管内液面上升、紫色石蕊溶液变红12. 科学家最新发现,通过简单的化学反应,可以将树木纤维素转变为超级储能装置,该反应的微观示意图如图,下列说法正确的是( )
A、图1、图2实验中都是短的蜡烛先熄灭 B、“釜底抽薪”灭火的原理和图2实验中蜡烛熄灭的原理相同 C、图3实验证明二氧化碳与水反应生成了碳酸 D、图3实验中观察到试管内液面上升、紫色石蕊溶液变红12. 科学家最新发现,通过简单的化学反应,可以将树木纤维素转变为超级储能装置,该反应的微观示意图如图,下列说法正确的是( )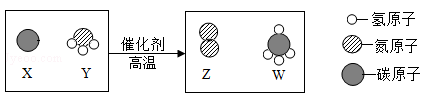 A、参加反应的Y中氮元素的质量一定等于生成Z的质量 B、该反应中使用催化剂增大产物质量 C、Y是由四种元素组成的化合物 D、该反应中生成的Z和W两物质的分子个数比为1:113. 化学用语是学好化学的工具。下列有关化学用语的说法正确的是( )A、H2O和H2O2中O的化合价相同 B、KMnO4和K2MnO4中有相同的原子团 C、Fe2+和Fe3+都属于铁元素,核外电子数不同 D、
A、参加反应的Y中氮元素的质量一定等于生成Z的质量 B、该反应中使用催化剂增大产物质量 C、Y是由四种元素组成的化合物 D、该反应中生成的Z和W两物质的分子个数比为1:113. 化学用语是学好化学的工具。下列有关化学用语的说法正确的是( )A、H2O和H2O2中O的化合价相同 B、KMnO4和K2MnO4中有相同的原子团 C、Fe2+和Fe3+都属于铁元素,核外电子数不同 D、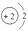 和
和  化学性质相同
14. 为了除去下列物质中的少量杂质(括号内为杂质),下列燥作方法不可行的是( )
化学性质相同
14. 为了除去下列物质中的少量杂质(括号内为杂质),下列燥作方法不可行的是( )选项
物质(杂质)
操作方法
A
N2(O2)
通过灼热的铜粉
B
N2(CO2)
将气体通过足量的澄清石灰水
C
CaO(CaCO3)
高温煅烧
D
CO2(CO)
将气体点燃
A、A B、B C、C D、D二、综合题
-
15. 化学实验是科学探究的基础。
 (1)、实验A,观察到的现象是。(2)、实验B,目的是探究铁生锈与有关。(3)、实验C,反应结束后,观察到天平的指针(填“不变”、偏左”或”偏右”)。(4)、实验D,用酒精灯在铜片中间位置加热一段时间。
(1)、实验A,观察到的现象是。(2)、实验B,目的是探究铁生锈与有关。(3)、实验C,反应结束后,观察到天平的指针(填“不变”、偏左”或”偏右”)。(4)、实验D,用酒精灯在铜片中间位置加热一段时间。①白磷先燃烧,a处红磷后燃烧,原因是。
②b处红磷拨开细沙后才燃烧,证明了燃烧的一个条件为。
16. 空气和水是维持生命的重要物质,下列实验可用于研究空气和水的组成。 (1)、利用实验A测定空气中氧气的含量。实验中用到的红磷属于。(填“单质”或“化合物”)(2)、为测定空气中氧气的含量,下列操作正确的是____(双选,填字母编号)A、检查装置的气密性 B、点燃红磷后,先让红磷在瓶内燃烧一会儿,再塞紧橡胶塞 C、点燃红磷前,不用弹簧夹夹紧橡胶导管 D、实验时取用稍过量的红磷 E、红磷熄灭后,立刻打开弹簧夹 F、实验中可以用硫代替红磷进行实验(3)、在实验B中,试管(填“a”或“b”)中的气体可以燃烧。试管a,b中产生气体的质量比为(填最简整数比)。电解水的化学方程式为 , 结合下面的电解水示意图,从微观角度补充填完成图A和图B .
(1)、利用实验A测定空气中氧气的含量。实验中用到的红磷属于。(填“单质”或“化合物”)(2)、为测定空气中氧气的含量,下列操作正确的是____(双选,填字母编号)A、检查装置的气密性 B、点燃红磷后,先让红磷在瓶内燃烧一会儿,再塞紧橡胶塞 C、点燃红磷前,不用弹簧夹夹紧橡胶导管 D、实验时取用稍过量的红磷 E、红磷熄灭后,立刻打开弹簧夹 F、实验中可以用硫代替红磷进行实验(3)、在实验B中,试管(填“a”或“b”)中的气体可以燃烧。试管a,b中产生气体的质量比为(填最简整数比)。电解水的化学方程式为 , 结合下面的电解水示意图,从微观角度补充填完成图A和图B .宏观变化
微观解释


三、综合题
-
17. 利用空气制取氮肥的流程如图所示:
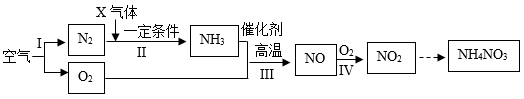
已知:硝酸铵(NH4NO3)溶于水后电离出和
(1)、I中是利用氧气和氮气的沸点不同分离液态空气,发生的是(填“物理变化”或“化学变化”)。(2)、请写出硝酸钙的化学式。(3)、单质X是一种常见气体,其化学式是 , 反应Ⅱ的基本反应类型是(填“化合反应”或“分解反应”)。(4)、写出反应IV的化学方程式。(5)、上述流程图中氮元素共有种不同的化合价。(6)、“雷雨发庄橡,一场雷雨一场肥”,自然界中的雷雨能使植物生长茂盛、叶色浓绿,雷雨给植物施加了氮肥。其原理为:雷雨天气时,空气中的氧气和氮气在雷电作用下可以直接反应生成NO,NO经过转化后,可生成氮肥。请写出该过程中氧气和氮气反应生成NO的化学方程式。18. 阅读下面的短文并回答问题。我国提出争取2030年前达到碳达峰,2060年实现碳中和的目标。现阶段我国的能源结构以化石燃料为主,其燃烧释放出大量的CO2。通过植树造林、海洋封存、综合利用等途径可降低大气中CO2浓度。
综合利用:工业上可以将CO2转化成甲醇(CH3OH)等资源,CO2和H2在一定条件下生成甲醇(CH3OH)和一种常见的液体氧化物。一定条件下,该反应在有、无分子筛膜时甲醇的产率随温度的变化如图所示。
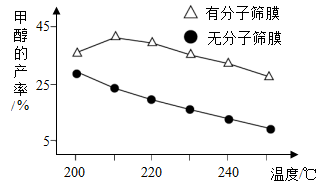 (1)、CO2可以封存在海洋里,但会引起海水酸化,体现出二氧化碳的性质是。(2)、写出利用CO2与H2合成甲醇的化学方程式 , 参加反应的CO2与H2的质量比为。(3)、由图可知,为提高甲醇的产率,合成甲醇应选择的最佳条件为、。(4)、煤(主要含碳元素,含有少量硫元素)燃烧时会产生SO2 , 从而形成酸雨。为防治酸雨,降低煤燃烧时向大气排放SO2工业上将生石灰(CaO)和含硫煤混合后使用:达到“固硫”的效果,有关“固硫”(不使硫化合物进入大气)的过程中发生了3个化合反应,最终生成CaSO4固体留在煤渣中、前2个分别是:、 , 则第3个反应的化学方程式为。(5)、实验室CO还原CuO的实验中,装有CuO的玻璃管中的现象为 , 写出该反应的化学方程式。19. 某化学兴趣小组同学设计以下实验,探究氢氧化钠与二氧化碳是否发生反应。
(1)、CO2可以封存在海洋里,但会引起海水酸化,体现出二氧化碳的性质是。(2)、写出利用CO2与H2合成甲醇的化学方程式 , 参加反应的CO2与H2的质量比为。(3)、由图可知,为提高甲醇的产率,合成甲醇应选择的最佳条件为、。(4)、煤(主要含碳元素,含有少量硫元素)燃烧时会产生SO2 , 从而形成酸雨。为防治酸雨,降低煤燃烧时向大气排放SO2工业上将生石灰(CaO)和含硫煤混合后使用:达到“固硫”的效果,有关“固硫”(不使硫化合物进入大气)的过程中发生了3个化合反应,最终生成CaSO4固体留在煤渣中、前2个分别是:、 , 则第3个反应的化学方程式为。(5)、实验室CO还原CuO的实验中,装有CuO的玻璃管中的现象为 , 写出该反应的化学方程式。19. 某化学兴趣小组同学设计以下实验,探究氢氧化钠与二氧化碳是否发生反应。【查阅资料】
①氢氧化钠与氢氧化钙的化学性质机似;
②碳酸钠与碳酸钙的化学性质相似;

该兴趣小组同学从反应物角度探究氢氧化钠与二氧化碳是否发生反应
(1)、小鹏同学按如图ABC进行实验,观察到软塑料瓶变形,认为NaOH与CO2发生了化学反应,反应的化学方程式为。(2)、小爽同学认为此现象不足以证明氢氧化钠与二氧化碳发生了反应,她的理由是。(3)、小静同学进一步思考后,设计了图D的改进装置进行实验:用注射器分别向烧瓶(已收集满CO2气体)中加入等体积的 , 通过传感器测得瓶中气压变化的曲线(如图E所示)①刚开始压强增大的原因是。
②800s时,曲线a表示的溶液显(填“酸”或“碱”)性。
③通过对比曲线a和曲线b(填“不能”或“能”)证明NaOH与CO2发生了化学反应,理由是。
(4)、CO和CO2的混合气体共0.72g,通过足量氢氧化钠溶液,充分反应后,得到气体的质量为0.28g,则原混合气体中碳元素和氧元素的质量比是。20. 根据下列实验装置图,回答有关问题。 (1)、写出装置图中标号仪器的名称:①。(2)、实验室用高锰酸钾制取氧气的化学方程式为;选用AF装置制取氧气结束时,为防止水槽里的水倒流,应采取的操作是。(3)、若用H2O2分解可制取O2 , 实验室通过测定收集一定体积O2所用的时间,来研究不同条件对H2O2分解速率的影响。
(1)、写出装置图中标号仪器的名称:①。(2)、实验室用高锰酸钾制取氧气的化学方程式为;选用AF装置制取氧气结束时,为防止水槽里的水倒流,应采取的操作是。(3)、若用H2O2分解可制取O2 , 实验室通过测定收集一定体积O2所用的时间,来研究不同条件对H2O2分解速率的影响。实验
温度/℃
H2O2溶液浓度
H2O2溶液体积/mL
lg催化剂
时间/s
1
20
5%
40
二氧化锰
37
2
20
10%
40
二氧化锰
14
3
20
a
40
氧化铜
b
①上表中实验1、2探究对分解速率的影响,实验2、3探究不同催化剂对分解速率的影响,则浓度a为。
②H2O2分解可制取O2 , 该小组在反应开始后立即连接装置G(注:G图中的集气瓶上方有少量空气)中的导管口,从而测定收集一定体积O2所用的时间。你认为该做法(填:“是”与“否”)合理。说出你的观点并闻述理由:。
(4)、实验室用大理石和稀盐酸制取二氧化碳的化学方程式为;若用碳酸钠粉末和稀盐酸反应来制取二氧化碳,为了得到平稳的气流,应选用的发生装置是。(5)、某兴趣小组用D装置制取二氧化碳时,用压强传感器测得试管内某段时间压强的变化如图所示,下列说法正确的是____(填字母)。 A、a点对应的操作是关闭弹簧夹 B、ab段试管中液面逐渐上升 C、bc段大理石与稀盐酸脱离接触 D、c点的对应操作是打开弹簧夹
A、a点对应的操作是关闭弹簧夹 B、ab段试管中液面逐渐上升 C、bc段大理石与稀盐酸脱离接触 D、c点的对应操作是打开弹簧夹