黑龙江省齐齐哈尔市龙沙区2022-2023学年九年级上学期期末化学试题
试卷更新日期:2023-03-14 类型:期末考试
一、选择题
-
1. 下列变化属于化学变化的是( )A、铁矿石粉碎 B、蓝莓酿红酒 C、纯铜丝导电 D、浓盐酸挥发2. 下列图示实验操作中,正确的是( )A、
 引燃镁条
B、
引燃镁条
B、 放置滴管
C、
放置滴管
C、 液体的量取
D、
液体的量取
D、 取用固体粉末
3. 下列与消防安全有关的做法正确的是A、家用电器着火用水浇灭 B、燃气泄露立刻打开排气扇 C、高层住宅失火时乘电梯逃生 D、逃离火场时,用湿毛巾捂住口鼻弯腰前行4. 下列有关部分实验现象的描述正确的是( )A、甲烷在空气中燃烧发出淡蓝色火焰 B、将打磨光亮的铝丝插入到硫酸铜溶液中,铝丝表面有铜析出 C、一氧化碳与氧化铁反应,固体由红(棕)色变为黑色 D、碘放到水中溶解,形成棕色溶液5. 鱼油中富含的DHA(C22H32O2)是大脑细胞形成和发育不可缺少的物质,下列关于DHA的叙述中正确的是( )A、DHA由碳、氢、氧三种元素组成 B、DHA属于氧化物 C、DHA由56个原子构成 D、DHA中氢元素的质量分数的最大6. 下列有关物质的用途错误的是( )A、
取用固体粉末
3. 下列与消防安全有关的做法正确的是A、家用电器着火用水浇灭 B、燃气泄露立刻打开排气扇 C、高层住宅失火时乘电梯逃生 D、逃离火场时,用湿毛巾捂住口鼻弯腰前行4. 下列有关部分实验现象的描述正确的是( )A、甲烷在空气中燃烧发出淡蓝色火焰 B、将打磨光亮的铝丝插入到硫酸铜溶液中,铝丝表面有铜析出 C、一氧化碳与氧化铁反应,固体由红(棕)色变为黑色 D、碘放到水中溶解,形成棕色溶液5. 鱼油中富含的DHA(C22H32O2)是大脑细胞形成和发育不可缺少的物质,下列关于DHA的叙述中正确的是( )A、DHA由碳、氢、氧三种元素组成 B、DHA属于氧化物 C、DHA由56个原子构成 D、DHA中氢元素的质量分数的最大6. 下列有关物质的用途错误的是( )A、 支架刷漆主要是美观
B、
支架刷漆主要是美观
B、 石墨做电极
C、
石墨做电极
C、 钛合金制造人造骨
D、
钛合金制造人造骨
D、 干冰用于血液制品的运输
7. 为探究二氧化碳能否和水反应,用四朵石蕊溶液染成紫色的干燥小花完成如下图四个实验。实验I、IV中小花变红,实验II、III中小花不变色。下列说法错误的是( )
干冰用于血液制品的运输
7. 为探究二氧化碳能否和水反应,用四朵石蕊溶液染成紫色的干燥小花完成如下图四个实验。实验I、IV中小花变红,实验II、III中小花不变色。下列说法错误的是( ) A、实验I、II说明醋酸可以使小花变红 B、实验III说明二氧化碳不能使小花变红 C、上述实验说明二氧化碳和稀醋酸具有相似的化学性质 D、该实验设计是多种因素对比实验8. 镍(Ni)和锰(Mn)都是重要金属,将Ni丝插入MnCl2溶液中,无明显现象;插入CuCl2溶液中,Ni丝表面有红色固体析出,则这三种金属活动性由强到弱的顺序是( )A、Cu、Mn、Ni B、Mn、Ni、Cu C、Ni、Mn、Cu D、Mn、Cu、Ni9. 下列有关溶液的说法中正确的是( )A、将40%的氢氧化钠溶液均分成两份,每份溶液的溶质质量分数都为20% B、降低饱和溶液的温度一定有晶体析出 C、与乳化作用相比,溶解能使物质混合得更均匀 D、溶液都是无色透明的液体10. 推理是化学学习过程中一种重要的思维方法,下列推理正确的是( )A、可燃性气体点燃前要检验纯度,所以点燃甲烷气体前一定要先检验其纯度 B、物质与氧气发生的反应属于氧化反应,所以氧化反应一定有氧气参加 C、溶液具有均一性、稳定性,所以具有均一性、稳定性的物质一定是溶液 D、活泼金属能与稀盐酸反应生成氢气,所以能与稀盐酸反应生成气体的物质一定是活泼金属11. 关于下列实验的分析与结论正确的是( )A、
A、实验I、II说明醋酸可以使小花变红 B、实验III说明二氧化碳不能使小花变红 C、上述实验说明二氧化碳和稀醋酸具有相似的化学性质 D、该实验设计是多种因素对比实验8. 镍(Ni)和锰(Mn)都是重要金属,将Ni丝插入MnCl2溶液中,无明显现象;插入CuCl2溶液中,Ni丝表面有红色固体析出,则这三种金属活动性由强到弱的顺序是( )A、Cu、Mn、Ni B、Mn、Ni、Cu C、Ni、Mn、Cu D、Mn、Cu、Ni9. 下列有关溶液的说法中正确的是( )A、将40%的氢氧化钠溶液均分成两份,每份溶液的溶质质量分数都为20% B、降低饱和溶液的温度一定有晶体析出 C、与乳化作用相比,溶解能使物质混合得更均匀 D、溶液都是无色透明的液体10. 推理是化学学习过程中一种重要的思维方法,下列推理正确的是( )A、可燃性气体点燃前要检验纯度,所以点燃甲烷气体前一定要先检验其纯度 B、物质与氧气发生的反应属于氧化反应,所以氧化反应一定有氧气参加 C、溶液具有均一性、稳定性,所以具有均一性、稳定性的物质一定是溶液 D、活泼金属能与稀盐酸反应生成氢气,所以能与稀盐酸反应生成气体的物质一定是活泼金属11. 关于下列实验的分析与结论正确的是( )A、 由酚酞溶液变红可知,分子是不断运动的
B、
由酚酞溶液变红可知,分子是不断运动的
B、 红磷量不足会使测量空气中氧气的体积分数偏大
C、
红磷量不足会使测量空气中氧气的体积分数偏大
C、 对照实验可得出铁生锈需要水和氧气
D、
对照实验可得出铁生锈需要水和氧气
D、 黄铜和纯铜相互刻画,黄铜上有划痕
12. 我国古代将炉甘石(ZnCO3)、赤铜和木炭粉混合后加热到约800℃,有如下反应发生① ②。下列有关说法错误的( )A、X的化学式为CO2 B、反应前后锌元素质量不变 C、②反应中ZnO发生了还原反应 D、②反应前后锌元素化合价升高13. 下列图像能正确表示对应关系的是( )A、
黄铜和纯铜相互刻画,黄铜上有划痕
12. 我国古代将炉甘石(ZnCO3)、赤铜和木炭粉混合后加热到约800℃,有如下反应发生① ②。下列有关说法错误的( )A、X的化学式为CO2 B、反应前后锌元素质量不变 C、②反应中ZnO发生了还原反应 D、②反应前后锌元素化合价升高13. 下列图像能正确表示对应关系的是( )A、 加热一定质量木炭粉和氧化铜混合物
B、
加热一定质量木炭粉和氧化铜混合物
B、 向饱和的氯化钠溶液中不断加入氯化钾固体
C、
向饱和的氯化钠溶液中不断加入氯化钾固体
C、 氢气燃烧生成水的质量
D、
氢气燃烧生成水的质量
D、 分别向等质量的镁和锌中滴加溶质质量分数相等的稀盐酸
14. 下列实验方案中,能达到目的的是( )
分别向等质量的镁和锌中滴加溶质质量分数相等的稀盐酸
14. 下列实验方案中,能达到目的的是( )选项
实验目的
实验方案
A
分离铜粉和锌粉的混合物
加入足量的稀硫酸,过滤、洗涤、干燥
B
除去氮气中混有的少量氧气
通入灼热的铜网
C
鉴别氢氧化钠固体和硝酸铵固体
分别取样,加适量的水,测量温度变化
D
提纯含有少量硝酸钾的氯化钠固体
加水溶解,加热浓缩,冷却结晶
A、A B、B C、C D、D15. 取6.5gZn放入Cu(NO3)2和AgNO3的混合溶液中,充分反应后,过滤。下列分析正确的是( )A、若滤液为蓝色,滤渣中一定有Ag,可能有Cu B、若滤液为无色,滤液中一定有Zn(NO3)2 , 可能有AgNO3 C、若滤液为无色,原溶液中AgNO3的质量可能为34g D、若滤渣质量为20g,滤液中一定有Zn(NO3)2 , 一定没有AgNO3二、填空题
-
16. 用适当的元素符号与数字的组合填空:(1)、2个氢原子。(2)、人体中含量最多的金属元素。(3)、菱铁矿的主要成分。17. 暑期实践活动中,同学们走进工厂,在实践中认识化学、体验化学、感悟化学。(1)、去工厂的途中,同学们看见路边鱼塘中用水泵把水喷向空中,这样做可以增大 , 达到目的。(2)、在工厂里,同学们看到车间里备有水基型灭火器,灭火时水基型灭火器产生的泡沫喷射到燃料的表面,泡沫层析出的水在燃料表面形成一层水膜,此过程中体现的灭火原理是。(3)、同学们取锅炉用水的水样,滴加肥皂水,搅拌,观察到产生大量泡沫,验证了锅炉用水是 , 同学们还参观了工厂循环用水和污水处理的流程,提升了爱护水资源的意识。(4)、工厂设有可回收和不可回收垃圾箱,小明自觉响应垃圾分类回收的倡导,将饮用完的金属易拉罐投放到垃圾箱。18. 能源与环境问题是社会关注的焦点。如图是某太阳能路灯的示意图,请回答下面的问题:
 (1)、图中所标示的路灯各主要部件中,属于金属材料的是(填序号)。(2)、常温下铝的化学性质活泼,但铝制品耐腐蚀的原因是。(3)、太阳能路灯中多处使用合金,合金与纯金属相比,有许多优良的性能,写出一条合金的优良性能。(4)、目前人们利用最多的能源是化石燃料。化石燃料属于(“可再生能源”或“不可再生能源”)天然气的主要成分是CH4 , CH4完全燃烧的化学方程式为。19. 如图是a、b、c三种物质的溶解度曲线,a与c溶解度曲线交于P点,据图回答问题:
(1)、图中所标示的路灯各主要部件中,属于金属材料的是(填序号)。(2)、常温下铝的化学性质活泼,但铝制品耐腐蚀的原因是。(3)、太阳能路灯中多处使用合金,合金与纯金属相比,有许多优良的性能,写出一条合金的优良性能。(4)、目前人们利用最多的能源是化石燃料。化石燃料属于(“可再生能源”或“不可再生能源”)天然气的主要成分是CH4 , CH4完全燃烧的化学方程式为。19. 如图是a、b、c三种物质的溶解度曲线,a与c溶解度曲线交于P点,据图回答问题: (1)、P点的含义是。(2)、t2℃时40ga物质加到50g水中不断搅拌,形成溶液的质量为g。(3)、除去固体a中混有的少量固体b的方法是(填“蒸发结晶”或“降温结晶”)。(4)、t2℃时,等质量的a、b、c三种物质的饱和溶液降温至t1℃时所含溶剂由多到少的顺序为。(5)、将t2℃时a、b、c三种物质的饱和溶液温度降到t1℃时,三种溶液中溶质的质量分数由大到小的排列顺序是。
(1)、P点的含义是。(2)、t2℃时40ga物质加到50g水中不断搅拌,形成溶液的质量为g。(3)、除去固体a中混有的少量固体b的方法是(填“蒸发结晶”或“降温结晶”)。(4)、t2℃时,等质量的a、b、c三种物质的饱和溶液降温至t1℃时所含溶剂由多到少的顺序为。(5)、将t2℃时a、b、c三种物质的饱和溶液温度降到t1℃时,三种溶液中溶质的质量分数由大到小的排列顺序是。三、综合题
-
20. A一F均为初中化学常见的物质,它们之间的关系如图所示(“→”表示转化关系,所涉及反应均为初中常见的化学反应),其中A俗称生石灰,C是最常用的溶剂,C与F元素组成相同。
 (1)、C的化学式是。(2)、A→B反应的化学方程式为。(3)、F→E反应的化学方程式为。21. “保护环境、保护自然就是保护我们人类自己”。请回答下列问题:(1)、请写出废旧电池随意丢弃造成的危害。(2)、请写出一种汽车尾气的污染物及减少汽车尾气的一条措施。22. 化学就在我们身边,生活中蕴含着丰富的化学知识。请回答下列问题:(1)、铅笔芯是用不同比率的石墨粉末和黏土混合而制成的。当家中的锁头因上锈而不易打开时,可以用铅笔芯粉末放入锁孔,就很容易打开了,为什么?(2)、当家中燃气灶中的火焰呈现黄色或橙色,锅底出现黑色,这时就需要调大一下灶具的进风口了,为什么?(3)、被汗水浸湿的衣服晾干后,常出现白色的斑迹,为什么?23. “宏观世界多姿多彩、微观世界魅力无穷”,利用所学微观知识解释下列宏观现象:(1)、金刚石与石墨物理性质差异很大的原因。(2)、体温计中的金属汞随体温升高,汞柱上升。(3)、固体物质配成溶液能加快化学反应速率。24. 某学生练习配制50g溶质质量分数为15%的氯化钠溶液。如图是该同学的操作过程中的示意图。试回答:
(1)、C的化学式是。(2)、A→B反应的化学方程式为。(3)、F→E反应的化学方程式为。21. “保护环境、保护自然就是保护我们人类自己”。请回答下列问题:(1)、请写出废旧电池随意丢弃造成的危害。(2)、请写出一种汽车尾气的污染物及减少汽车尾气的一条措施。22. 化学就在我们身边,生活中蕴含着丰富的化学知识。请回答下列问题:(1)、铅笔芯是用不同比率的石墨粉末和黏土混合而制成的。当家中的锁头因上锈而不易打开时,可以用铅笔芯粉末放入锁孔,就很容易打开了,为什么?(2)、当家中燃气灶中的火焰呈现黄色或橙色,锅底出现黑色,这时就需要调大一下灶具的进风口了,为什么?(3)、被汗水浸湿的衣服晾干后,常出现白色的斑迹,为什么?23. “宏观世界多姿多彩、微观世界魅力无穷”,利用所学微观知识解释下列宏观现象:(1)、金刚石与石墨物理性质差异很大的原因。(2)、体温计中的金属汞随体温升高,汞柱上升。(3)、固体物质配成溶液能加快化学反应速率。24. 某学生练习配制50g溶质质量分数为15%的氯化钠溶液。如图是该同学的操作过程中的示意图。试回答: (1)、配制一定溶质质量分数的氯化钠溶液的一些操作步骤见图,正确的操作顺序是(填序号)。(2)、③操作中应称量NaCl的质量是g,称量氯化钠时,在往左盘慢慢加入氯化钠的过程中,指针偏左,接下来的操作是。25. 对比实验是实验探究的重要方法。结合下图请回答问题:
(1)、配制一定溶质质量分数的氯化钠溶液的一些操作步骤见图,正确的操作顺序是(填序号)。(2)、③操作中应称量NaCl的质量是g,称量氯化钠时,在往左盘慢慢加入氯化钠的过程中,指针偏左,接下来的操作是。25. 对比实验是实验探究的重要方法。结合下图请回答问题: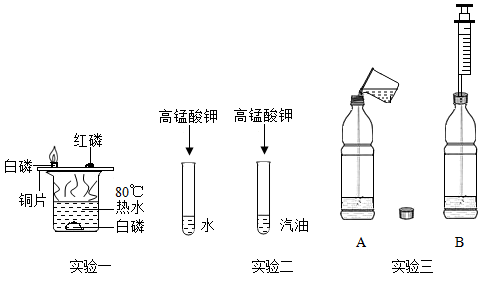 (1)、实验一,铜片上的白磷燃烧而红磷不燃烧说明可燃物燃烧需要的条件之一是 , 若实验过程中铜片上的红磷燃烧了原因是。(2)、实验二,根据两只试管中的现象得出的结论是。(3)、实验三,A和B的软塑料瓶体积相同且充满CO2 , 将A瓶盖打开,加入体积约为塑料瓶容积1/3的蒸馏水,旋紧瓶盖后充分振荡;向B中注入等体积的蒸馏水,充分振荡,观察到A瓶的实验现象是 , B瓶无明显变化,其原因是。26. 实验室现有大理石、高锰酸钾、稀盐酸等药品及相关仪器和用品,请结合下列装置回答问题:
(1)、实验一,铜片上的白磷燃烧而红磷不燃烧说明可燃物燃烧需要的条件之一是 , 若实验过程中铜片上的红磷燃烧了原因是。(2)、实验二,根据两只试管中的现象得出的结论是。(3)、实验三,A和B的软塑料瓶体积相同且充满CO2 , 将A瓶盖打开,加入体积约为塑料瓶容积1/3的蒸馏水,旋紧瓶盖后充分振荡;向B中注入等体积的蒸馏水,充分振荡,观察到A瓶的实验现象是 , B瓶无明显变化,其原因是。26. 实验室现有大理石、高锰酸钾、稀盐酸等药品及相关仪器和用品,请结合下列装置回答问题: (1)、I.用高锰酸钾制取氧气:
(1)、I.用高锰酸钾制取氧气:仪器a的名称是。
(2)、制取氧气时发生反应的化学方程式为。(3)、制取氧气的过程有多步操作,其中的两步操作为:①将集气瓶盛满水,连同玻璃片一起倒立在盛水的水槽内;②让试管均匀受热,然后对药品所在部位加热。①在②(填“之前“或“之后”)相对合理。(4)、图E为用图D中的方法刚刚收集满的一瓶氧气,此时集气瓶内压强(填“大于”或“小于”)外界大气压。将红热的木炭伸入到图E的集气瓶中,观察到木炭燃烧发出、放热。(5)、 II.用大理石(大理石中的杂质不溶于水,且不参与反应)和稀盐酸制取二氧化碳:选用C装置收集二氧化碳的原因是:在相同条件下,二氧化碳的密度比空气的密度(填“大”或“小”)。
(6)、制取二氧化碳发生反应的化学方程式为 , B装置内碳酸钙的质量随时间变化的大致趋势如图所示,请结合图像分析,t0时B装置内的溶液中Ca2+与Cl-的个数比(填“等于”或“小于”)1:2。 27. 实验活动课上,老师为大家演示兴趣实验,振荡留有小孔的盒子,将里面的黑色粉末均匀地洒在酒精灯火焰的上方,观察到火星四射的灿烂烟花。老师揭秘黑色粉末是食品包装袋中的脱氧剂。为此兴趣小组展开了对该脱氧剂成分及原理的探究。(1)、实验活动一:探究脱氧剂中黑色粉末的成分。
27. 实验活动课上,老师为大家演示兴趣实验,振荡留有小孔的盒子,将里面的黑色粉末均匀地洒在酒精灯火焰的上方,观察到火星四射的灿烂烟花。老师揭秘黑色粉末是食品包装袋中的脱氧剂。为此兴趣小组展开了对该脱氧剂成分及原理的探究。(1)、实验活动一:探究脱氧剂中黑色粉末的成分。【作出猜想】黑色粉末含有铁粉和碳粉中的一种或两种。
【实验探究】小组同学设计实验方案并完成如下实验:
实验步骤
实验现象
实验结论
D取黑色粉末放入烧杯中,加入稀盐酸。
, 溶液变为浅绿色,有黑色不溶物。
黑色粉末中含有铁粉,反应的化学方程式为。
②将①中黑色不溶物滤出,洗涤、干燥后,放在陶土网上灼烧,上方放一蘸有澄清石灰水的玻璃片。
黑色粉末中含有碳粉。
(2)、【查阅资料】实验所用脱氧剂中还含有氯化钠实验活动二:探究脱氧剂中氯化钠的作用。
【实验探究】小组同学用控制变量法按如图装置进行实验:

一段时间后观察到烧杯内左侧导管液面右侧导管液面(填“高于”或“低于”)。
(3)、【表达交流】脱氧剂利用铁生锈的原理延长食品保质期。其中碳粉具有性,可以促进反应的发生,氯化钠可以加快铁生锈的反应速率。(4)、【反思评价】脱氧剂包装上应注明的注意事项是(请写出一条)。四、计算题