广西玉林市2022-2023学年九年级上学期期末化学试题
试卷更新日期:2023-03-14 类型:期末考试
一、单选题
-
1. 我们可以采用以下方法预防新冠病毒。其中主要利用化学变化的是( )A、酒精消毒 B、勤洗手 C、配戴口罩 D、测量体温2. 作为生活常识,我们应该知道一些特殊的符号。下列标志属于禁止吸烟的是( )A、
 B、
B、 C、
C、 D、
D、 3. 通过实验测定,空气的成分按体积计,约占78%的是( )A、氧气 B、氮气 C、二氧化碳 D、稀有气体4. 生活中“富硒苹果”“高钙牛奶”中的“硒”和“钙”是指( )A、元素 B、单质 C、原子 D、分子5. 下列实验基本操作,正确的是( )A、
3. 通过实验测定,空气的成分按体积计,约占78%的是( )A、氧气 B、氮气 C、二氧化碳 D、稀有气体4. 生活中“富硒苹果”“高钙牛奶”中的“硒”和“钙”是指( )A、元素 B、单质 C、原子 D、分子5. 下列实验基本操作,正确的是( )A、 滴加液体
B、
滴加液体
B、 加热氯酸钾粉末
C、
加热氯酸钾粉末
C、 闻气体气味
D、
闻气体气味
D、 读取液体体积
6. “一家炒菜十家香”,这句话说明分子具有的主要性质是( )A、分子的体积很小 B、分子间间隔很小 C、分子可以再分 D、分子不断运动7. “建设美丽中国”是新时代的目标,下列做法不符合这一理念的是( )A、垃圾分类处理 B、工业废气经处理达标后再排放 C、外出尽量步行或乘坐公交车 D、大量使用化肥,提高粮食产量8. 下列有关实验现象的描述正确的是( )A、石蜡在空气中燃烧生成使澄清石灰水变浑浊的二氧化碳气体 B、硫粉在氧气中燃烧时,产生蓝紫色火焰,生成有刺激性气味的无色气体 C、红磷在空气中燃烧,产生大量的白色烟雾 D、铁丝在空气中剧烈燃烧,火星四射,生成黑色固体9. 要提高全民的环保意识,保护我们的空气。下列不属于空气污染物的是( )A、CO B、SO2 C、CO2 D、NO210. 下列做法正确的是( )A、发现油锅起火,应立即使用冷水将其浇灭 B、进入久未开启的菜窖,可以做灯火实验检查 C、厨房里天然气泄漏后,应立即打开排气扇 D、遇到室内起火,迅速打开门窗通风11. 有关金刚石、石墨、C60的下列说法中,错误的是( )A、微粒观:金刚石、石墨和C60都由碳原子构成 B、能量观:C60在氧气中燃烧是放热反应 C、变化观:一定条件下可以将石墨转化为金刚石 D、结构观:碳原子排列方式不同,因此三种物质的物理性质存在差异12. 连花清瘟胶囊具有清瘟解毒,宣肺泄热的功效。其成分中含有一种名为绿原酸的物质,下列有关绿原酸(C16H18O9)的说法正确的是( )A、绿原酸的相对分子质量是354g B、绿原酸属于氧化物 C、绿原酸中碳元素和氧元素的质量比为4:3 D、绿原酸由16个碳原子、18个氢原子和9个氧原子构成13. 月球岩石中富含钛铁矿,其主要成分是FeTiO3 , 其中钛(Ti)元素的化合价为+4,则铁元素的化合价为( )A、0价 B、+2价 C、+3价 D、+4价14. 氢元素(H)与氦元素(He)的本质区别是()A、质子数不同 B、中子数不同 C、核外电子数不同 D、相对原子质量不同15. 用嘴吹灭生日蛋糕的蜡烛,利用的主要灭火原理是( )A、使可燃物温度降到着火点以下 B、降低可燃物的着火点 C、隔绝空气 D、清除可燃物16. 逻辑推理是一种重要的化学思维方法。下列推理正确的是( )A、单质由同种元素组成,由同种元素组成的物质一定是单质 B、含碳元素的物质充分燃烧会生成CO2 , 燃烧能生成CO2的物质一定含碳元素 C、氧化物中含有氧元素,则含氧元素的化合物一定是氧化物 D、离子是带电的粒子,则带电的粒子一定是离子17. 下列实验设计能达到目的的是( )A、
读取液体体积
6. “一家炒菜十家香”,这句话说明分子具有的主要性质是( )A、分子的体积很小 B、分子间间隔很小 C、分子可以再分 D、分子不断运动7. “建设美丽中国”是新时代的目标,下列做法不符合这一理念的是( )A、垃圾分类处理 B、工业废气经处理达标后再排放 C、外出尽量步行或乘坐公交车 D、大量使用化肥,提高粮食产量8. 下列有关实验现象的描述正确的是( )A、石蜡在空气中燃烧生成使澄清石灰水变浑浊的二氧化碳气体 B、硫粉在氧气中燃烧时,产生蓝紫色火焰,生成有刺激性气味的无色气体 C、红磷在空气中燃烧,产生大量的白色烟雾 D、铁丝在空气中剧烈燃烧,火星四射,生成黑色固体9. 要提高全民的环保意识,保护我们的空气。下列不属于空气污染物的是( )A、CO B、SO2 C、CO2 D、NO210. 下列做法正确的是( )A、发现油锅起火,应立即使用冷水将其浇灭 B、进入久未开启的菜窖,可以做灯火实验检查 C、厨房里天然气泄漏后,应立即打开排气扇 D、遇到室内起火,迅速打开门窗通风11. 有关金刚石、石墨、C60的下列说法中,错误的是( )A、微粒观:金刚石、石墨和C60都由碳原子构成 B、能量观:C60在氧气中燃烧是放热反应 C、变化观:一定条件下可以将石墨转化为金刚石 D、结构观:碳原子排列方式不同,因此三种物质的物理性质存在差异12. 连花清瘟胶囊具有清瘟解毒,宣肺泄热的功效。其成分中含有一种名为绿原酸的物质,下列有关绿原酸(C16H18O9)的说法正确的是( )A、绿原酸的相对分子质量是354g B、绿原酸属于氧化物 C、绿原酸中碳元素和氧元素的质量比为4:3 D、绿原酸由16个碳原子、18个氢原子和9个氧原子构成13. 月球岩石中富含钛铁矿,其主要成分是FeTiO3 , 其中钛(Ti)元素的化合价为+4,则铁元素的化合价为( )A、0价 B、+2价 C、+3价 D、+4价14. 氢元素(H)与氦元素(He)的本质区别是()A、质子数不同 B、中子数不同 C、核外电子数不同 D、相对原子质量不同15. 用嘴吹灭生日蛋糕的蜡烛,利用的主要灭火原理是( )A、使可燃物温度降到着火点以下 B、降低可燃物的着火点 C、隔绝空气 D、清除可燃物16. 逻辑推理是一种重要的化学思维方法。下列推理正确的是( )A、单质由同种元素组成,由同种元素组成的物质一定是单质 B、含碳元素的物质充分燃烧会生成CO2 , 燃烧能生成CO2的物质一定含碳元素 C、氧化物中含有氧元素,则含氧元素的化合物一定是氧化物 D、离子是带电的粒子,则带电的粒子一定是离子17. 下列实验设计能达到目的的是( )A、 探究空气与呼出的气体中CO2含量的高低
B、
探究空气与呼出的气体中CO2含量的高低
B、 验证质量守恒定律
C、
验证质量守恒定律
C、 测定空气中氧气的含量
D、
测定空气中氧气的含量
D、 探究二氧化碳与水发生反应
18. 在一个密闭容器中,有甲、乙、丙、丁、戊五种物质,在一定条件下发生反应,测得反应前后各物质的质量变化量如图所示(图中正数表示物质质量的增加量,负数表示物质质量的减少量,0表示物质质量不变),下列说法正确的是( )
探究二氧化碳与水发生反应
18. 在一个密闭容器中,有甲、乙、丙、丁、戊五种物质,在一定条件下发生反应,测得反应前后各物质的质量变化量如图所示(图中正数表示物质质量的增加量,负数表示物质质量的减少量,0表示物质质量不变),下列说法正确的是( )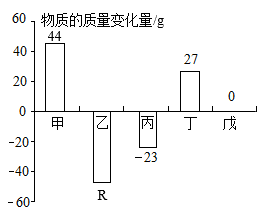 A、R=-38 B、戊一定是该反应的催化剂 C、反应后容器中一定含有5种物质 D、该反应中参加反应的乙与生成丁的质量比为16:919. 物质的检验、鉴别与除杂是重要的实验技能。下列依据实验目的所设计的实验方案中,试剂或方法错误的是( )
A、R=-38 B、戊一定是该反应的催化剂 C、反应后容器中一定含有5种物质 D、该反应中参加反应的乙与生成丁的质量比为16:919. 物质的检验、鉴别与除杂是重要的实验技能。下列依据实验目的所设计的实验方案中,试剂或方法错误的是( )选项
实验目的
用试剂或方法
A
除去CO2中混有的少量CO
通过灼热的氧化铜
B
鉴别白醋和白酒
闻气味
C
检验酒精中是否含有氧元素
在空气中点燃,检验生成物
D
除去CaO中的CaCO3
高温煅烧
A、A B、B C、C D、D20. 下列图像能正确反映对应变化关系的是( )A、 加热一定质量的高锰酸钾固体
B、
加热一定质量的高锰酸钾固体
B、 用等质量氯酸钾制取氧气
C、
用等质量氯酸钾制取氧气
C、 电解水一段时间
D、
电解水一段时间
D、 高温煅烧石灰石
高温煅烧石灰石
二、填空题
-
21. 化学就在我们身边。请用下列物质的序号填空。
①稀有气体 ②酒精 ③生石灰 ④石墨 ⑤明矾
(1)、具有导电性、可以做电极的是;(2)、可制成多种用途电光源的是;(3)、可用作干燥剂的是;(4)、实验室常用的燃料是;(5)、可用作净水剂的是。22. 水是生命之源,是人类宝贵的自然资源,我们每个人都要关心水、爱护水、节约用水。(1)、保持水的化学性质的最小微粒是。(2)、区别硬水和软水时,可用来检验,日常生活中可采取措施降低水的硬度。(3)、利用的吸附性去除水中异味。(4)、在下列净化水方法中,净化水程度最高的是____。A、过滤 B、煮沸 C、蒸馏 D、吸附 E、静置沉淀 F、吸附沉淀(5)、人类拥有的淡水资源紧缺,请写出一种生活中节约用水的方法:。23. 建立“宏观一微观一符号”之间的联系是化学学习的重要方法。 (1)、图1是部分微粒的结构示意图。
(1)、图1是部分微粒的结构示意图。①A~E共有种元素。
②D在化学反应中容易(填“得到”或“失去”)电子。
③C、E形成化合物的化学式为。
(2)、钕元素(Nd)是制造导弹的金属材料中的重要元素,钕元素部分信息如图2所示。钕原子的核外电子数为。(3)、汽车尾气催化转换器可减少有害气体排放,其反应过程的微观变化如图所示。
已知丁是一种单质,则丁是(写化学式)。
24. 我国提出2060年前实现碳中和,彰显了负责任大国的作为与担当。(1)、现阶段的能源结构仍以化石燃料为主,化石燃料包括煤、和天然气。(2)、“碳中和”的含义是产生的二氧化碳和消耗的二氧化碳相当,达到“零排放”实现“碳中和”有利于缓解的环境问题是。(3)、可燃冰被科学家誉为“21世纪能源”。可燃冰是(填“纯净物”和“混合物”)。(4)、为实现“碳中和”,达到“净零排放”,下列做法错误的是____。A、大力植树造林,严禁乱砍滥伐森林 B、开发氢能,更多利用太阳能等清洁能源 C、禁止使用化石燃料 D、露天焚烧垃圾三、综合题
-
25. A~F为初中化学的常见物质,它们由H、C、O、Ca、Cu元素中的一种、两种或三种组成,其中A、C、D在常温下的状态各不相同,且均为氧化物;F是大理石的主要成分。它们之间的关系如图所示(图中“一”表示能相互反应,“→”表示一步转化关系,部分反应物、生成物及反应条件已略去)。

回答下列问题:
(1)、C物质呈固态时叫做 , F的化学式是。(2)、D→E反应的化学方程式是 , 该反应为反应(填“吸热”或“放热”)。(3)、写出B的一种用途。26. 2022年11月30日神舟十五号载人飞船成功对接空间站,中国空间站首次迎来6人“在岗”。氧气、水、食物等是维持航天员驻留空间站的必要物质。为提高物质的利用率,目前空间站通过以下途径实现物质循环利用: (1)、“蒸发水汽”时,从微观角度分析,液态水与气态水的区别是。(2)、系统将从尿处理系统输送来的水进行电解产生氧气,供航天员呼吸。写出电解水的化学方程式。(3)、为实现氧的循环,目前空间站内利用氢气和航天员呼出的二氧化碳,在一定条件下转化为甲烷和另一种液态物质,写出该反应的化学方程式。(4)、在上述物质循环过程中循环利用的物质是(写化学式)。27. 工业上用石灰石为原料制备纳米CaCO3的一种流程如图所示。
(1)、“蒸发水汽”时,从微观角度分析,液态水与气态水的区别是。(2)、系统将从尿处理系统输送来的水进行电解产生氧气,供航天员呼吸。写出电解水的化学方程式。(3)、为实现氧的循环,目前空间站内利用氢气和航天员呼出的二氧化碳,在一定条件下转化为甲烷和另一种液态物质,写出该反应的化学方程式。(4)、在上述物质循环过程中循环利用的物质是(写化学式)。27. 工业上用石灰石为原料制备纳米CaCO3的一种流程如图所示。
已知:SiO2不与盐酸反应。
(1)、设备Ⅰ中需不断搅拌,其目的是。(2)、设备Ⅰ中发生反应的化学方程式为。(3)、设备Ⅳ中的分离操作是 , 该操作用到的玻璃仪器有烧杯、漏斗、。(4)、设备Ⅲ中参加反应的物质除水和CaCl2外,还有。28. 某研究性学习小组欲利用下列装置进行相关气体制取的探究,请回答下列问题: (1)、仪器①的名称为。(2)、实验室若要制取并收集一瓶较纯净的氢气,合适的装置组合是 , 反应的化学方程式是。(3)、实验室若用装置D收集CO2 , 检验其是否收集满的方法为。若用G收集二氧化碳,二氧化碳应从(选“a”或“b”)进,装置C与装置B相比,其主要优点是。29. 同学们为了研究氧化铁能否在氯酸钾制取氧气的实验中起催化作用,进行了以下实验:
(1)、仪器①的名称为。(2)、实验室若要制取并收集一瓶较纯净的氢气,合适的装置组合是 , 反应的化学方程式是。(3)、实验室若用装置D收集CO2 , 检验其是否收集满的方法为。若用G收集二氧化碳,二氧化碳应从(选“a”或“b”)进,装置C与装置B相比,其主要优点是。29. 同学们为了研究氧化铁能否在氯酸钾制取氧气的实验中起催化作用,进行了以下实验:【资料】氯酸钾和氯化钾均能溶于水。
【实验一】氧化铁能否在氯酸钾制取氧气实验中加快反应速率?
实验编号
KClO3/g
氧化物
产生气体的体积(mL)
耗时(s)
①
0.6
/
67
1800
②
0.6
0.2g二氧化锰
67
36.5
③
0.6
____g氧化铁
67
89.5
(1)、实验③中氧化铁的质量为g。(2)、实验①③对比得到的结论是。(3)、【交流讨论】经过讨论,有的同学认为只有上述证据,不能证明氧化铁能作氯酸钾分解的催化剂。还要补充一个探究实验:【实验二】在实验③反应后的混合物中加足量的水溶解,过滤得到固体,洗涤干燥并用电子天平称量,质量0.2g。说明氧化铁在反应前后质量不变。
【交流反思】有的同学认为要证明氧化铁能作氯酸钾分解的催化剂,上述实验还不足够,还需要再增加一个实验:探究。
(4)、【实验结论】氧化铁能在氯酸钾制取氧气反应中作催化剂。写出该反应的化学方程式。(5)、【拓展实验】同学们还想探究氧化铁的其他性质,将一定量的CO通入滤出的固体(氧化铁),按如图进行实验:
回答下面问题:
①实验过程中,观察到装置B中的现象是。
②实验开始时,是先给氧化铁加热,还是先通入一氧化碳? , 这样做的目的是。
洒实验中酒精灯的目的是。
四、计算题
-
30. 某补钙剂的有效成分是碳酸钙,其说明书中表明碳酸钙含量是80%,其他成分不含钙且不与盐酸反应。现取15g补钙剂进行如图所示实验。试分析并计算:
 (1)、反应生成气体的总质量为g。(2)、通过计算判断该补钙剂中碳酸钙含量与说明书是否相符?(结果精确到0.1%)
(1)、反应生成气体的总质量为g。(2)、通过计算判断该补钙剂中碳酸钙含量与说明书是否相符?(结果精确到0.1%)