2022-2023人教版九年级化学第九单元溶液 课题3溶液的浓度 课时提高训练
试卷更新日期:2023-03-06 类型:同步测试
一、单选题
-
1. 向20%NaCl溶液中,再加入1.5 gNaCl和6 g水,所得溶液溶质质量分数( )A、等于20% B、大于20% C、小于20% D、无法判断2. 在20 ℃时向100 g质量分数为5%的氯化钠溶液中加入5 g氯化钾,充分搅拌后全部溶解,则所得溶液中NaCl的质量分数( )A、大于5% B、小于5% C、仍为5% D、不确定3. 将25g氯酸钠加入25g水中,升高温度并充分搅拌,不同温度时所得溶液的质量如表所示。下列说法正确的是( )
温度/℃
20
30
60
70
80
溶液质量/g
32.9
36.4
50
50
50
A、20℃时,氯酸钠的溶解度为31.6g B、30℃时,所得溶液为不饱和溶液 C、由60℃升温到70℃过程中,氯酸钠溶解度保持不变 D、80℃时,向该溶液中加入25g水,溶质的质量分数为50%4. 如图是甲、乙两种固体物质(均不含结晶水)的溶解度曲线,下列说法错误的是( ) A、甲中含有少量乙,可用冷却热饱和溶液的方法提纯甲 B、t3℃时,甲的溶液溶质质量分数不一定大于乙的溶液溶质质量分数 C、t1℃时,乙的不饱和溶液通过蒸发溶剂的方法可以转变成饱和溶液 D、t3℃时,将等质量的甲、乙两种物质的溶液分别降温至t2℃,析出晶体的质量甲一定大于乙5. 20℃时,向盛有72g水的烧杯中加入18g固体M,充分溶解(如甲所示),进行如图所示实验(不考虑水分蒸发)。下列说法正确的是( )
A、甲中含有少量乙,可用冷却热饱和溶液的方法提纯甲 B、t3℃时,甲的溶液溶质质量分数不一定大于乙的溶液溶质质量分数 C、t1℃时,乙的不饱和溶液通过蒸发溶剂的方法可以转变成饱和溶液 D、t3℃时,将等质量的甲、乙两种物质的溶液分别降温至t2℃,析出晶体的质量甲一定大于乙5. 20℃时,向盛有72g水的烧杯中加入18g固体M,充分溶解(如甲所示),进行如图所示实验(不考虑水分蒸发)。下列说法正确的是( )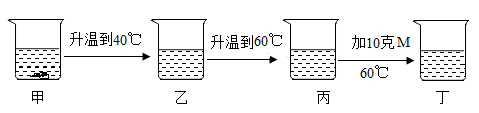 A、甲是饱和溶液,乙是不饱和溶液 B、丙和丁都是不饱和溶液 C、丁中溶液溶质的质量分数为28% D、M的溶解度随温度的升高而减小6. 如图为甲、乙两种固体物质的溶解度曲线。下列说法错误的是( )
A、甲是饱和溶液,乙是不饱和溶液 B、丙和丁都是不饱和溶液 C、丁中溶液溶质的质量分数为28% D、M的溶解度随温度的升高而减小6. 如图为甲、乙两种固体物质的溶解度曲线。下列说法错误的是( )
 A、要使甲从溶液中析出,只能用冷却热饱和溶液的方法 B、b 点所代表的的甲溶液可通过降低温度的方式变成饱和溶液 C、t1℃时,甲、乙两物质饱和溶液中溶质的质量分数相等 D、乙物质的溶解度随温度的升高而增大7. 20℃时,向100g质量分数为26.5%的饱和氯化钠溶液中加入3.5g氯化钠,此时溶液中溶质的质量分数为( )A、2.5% B、29.1% C、26.5% D、40%8. t℃时,向一支盛有0.1g熟石灰的试管内加入10mL水,充分振荡后,静置,试管底部仍有未溶解的白色固体。对于试管内上层澄清液体的叙述正确的是( )A、溶液t℃时的饱和溶液 B、升高温度溶液变为不饱和溶液 C、溶液中溶质的质量等于0.1g D、溶液中溶质的质量分数等于1%9. 在温度不变的条件下,下列欲使10%的硝酸钾溶液的溶质质量分数变为20%的方法中,一定能实现的是( )A、将20g10%的硝酸钾饱和溶液倒掉10g B、将20g10%的硝酸钾不饱和溶液蒸发掉10g水 C、在20g10%的硝酸钾溶液中,加入10g40%的硝酸钾溶液 D、将20g10%的硝酸钾不饱和溶液中加入20g硝酸钾固体10. 甲、乙两物质的溶解度曲线如下图所示。下列叙述中正确的是()
A、要使甲从溶液中析出,只能用冷却热饱和溶液的方法 B、b 点所代表的的甲溶液可通过降低温度的方式变成饱和溶液 C、t1℃时,甲、乙两物质饱和溶液中溶质的质量分数相等 D、乙物质的溶解度随温度的升高而增大7. 20℃时,向100g质量分数为26.5%的饱和氯化钠溶液中加入3.5g氯化钠,此时溶液中溶质的质量分数为( )A、2.5% B、29.1% C、26.5% D、40%8. t℃时,向一支盛有0.1g熟石灰的试管内加入10mL水,充分振荡后,静置,试管底部仍有未溶解的白色固体。对于试管内上层澄清液体的叙述正确的是( )A、溶液t℃时的饱和溶液 B、升高温度溶液变为不饱和溶液 C、溶液中溶质的质量等于0.1g D、溶液中溶质的质量分数等于1%9. 在温度不变的条件下,下列欲使10%的硝酸钾溶液的溶质质量分数变为20%的方法中,一定能实现的是( )A、将20g10%的硝酸钾饱和溶液倒掉10g B、将20g10%的硝酸钾不饱和溶液蒸发掉10g水 C、在20g10%的硝酸钾溶液中,加入10g40%的硝酸钾溶液 D、将20g10%的硝酸钾不饱和溶液中加入20g硝酸钾固体10. 甲、乙两物质的溶解度曲线如下图所示。下列叙述中正确的是()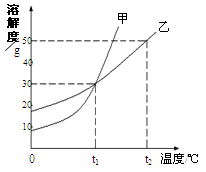 A、t1℃时,甲和乙的溶解度均为30 B、t1℃时,甲和乙的饱和溶液中溶质质量一定相等 C、t2℃时,分别在100g水中各溶解20g甲、乙,降温后,乙溶液的溶质质量分数可能会大于甲溶液的溶质质量分数 D、t2℃时,在100g水中放入60g乙,其溶质的质量分数为37.5%
A、t1℃时,甲和乙的溶解度均为30 B、t1℃时,甲和乙的饱和溶液中溶质质量一定相等 C、t2℃时,分别在100g水中各溶解20g甲、乙,降温后,乙溶液的溶质质量分数可能会大于甲溶液的溶质质量分数 D、t2℃时,在100g水中放入60g乙,其溶质的质量分数为37.5%二、填空题
-
11. 20℃时,将33g氯化钠放人100g水中,氯化钠全部溶解,再向此溶液中加入3g氯化钠又恰好全部溶解,则溶质为g,现在溶液恰好饱和,再向此溶液中加入3g氯化钠,溶质的质量分数为。12. 现有100g溶质质量分数为5%的KNO3溶液,若要使其溶质质量分数变为10%,则可加入g KNO3。13. 80克质量分数为15%的硝酸钠溶液里有硝酸钠克,在这种硝酸钠溶液中加入20克水后,所得溶液中溶质的质量分数为 .14. 在农业科研上,有时用10%~20%的氯化钠溶液来选种.现需用30Kg 16%的氯化钠溶液,可用下述两种方法配制.
(1)若用氯化钠固体和水配制上述溶液,需用氯化钠的质量 Kg;
(2)若用25%的氯化钠溶液和水配制上述溶液,需用25%氯化钠溶液的质量是 Kg.
15.图是A、B、C三种固体物质(固体组成与溶质相同)的溶解度曲线.在t1℃时,将质量为a g的A、B、C三种物质分别加入100g水中,根据图示回答下列问题:
(1)三种物质中,随温度升高溶解度减小的物质是 ;
(2)t1℃时,所得三种物质的溶液中为不饱溶液的是 ;
(3)若使这三种溶液溶质的质量分数相等,则温度应由t1℃升至 ℃;
(4)若将温度由t1℃升至t4℃时,三种溶液中溶质质量分数的大小关系为 .

三、简答题
-
16. 如果用a%表示饱和溶液中溶质的质量分数,用s表示该溶液中溶质的溶解度,请你比较a值和s值的大小,并说明为什么?17. 在20℃时,食盐的溶解度为36克,在此温度下,你能配制出40%的食盐溶液吗?为什么?(写出计算过程)
四、综合题
-
18. A、B、C三种物质的溶解度曲线如丙图所示。
 (1)、图中P点的含义:。(2)、t1℃时,将等质量的A和B分别加入到各盛有50g水的两个烧杯中,充分搅拌后现象如图烧杯甲和烧杯乙所示。烧杯乙中的溶质是(填“A”或“B”),为使烧杯乙中固体完全溶解可采取的方法为。(3)、将t2℃时A、B、C三种物质的饱和溶液分别降温到t1℃时,所得溶液溶质的质量分数由大到小的顺序为。
(1)、图中P点的含义:。(2)、t1℃时,将等质量的A和B分别加入到各盛有50g水的两个烧杯中,充分搅拌后现象如图烧杯甲和烧杯乙所示。烧杯乙中的溶质是(填“A”或“B”),为使烧杯乙中固体完全溶解可采取的方法为。(3)、将t2℃时A、B、C三种物质的饱和溶液分别降温到t1℃时,所得溶液溶质的质量分数由大到小的顺序为。五、实验探究题
-
19. 如图是 A,B,C 三种固体物质的溶解度曲线,请回答下列问题。
 (1)、P 点的含义是。(2)、t1℃时,A,B,C三种固体物质的溶解度由大到小依次是。(3)、t2℃时,分别向 100g 的水中加入 30gA、30gB 和 30gC, 形成不饱和溶液的是。(4)、当 B 中混有少量的 A 时,可用的方法提纯 B。(5)、将 t2℃时等质量的 A,B,C 的饱和溶液降温到 t1℃,则下列说法正确的是(填序号)。
(1)、P 点的含义是。(2)、t1℃时,A,B,C三种固体物质的溶解度由大到小依次是。(3)、t2℃时,分别向 100g 的水中加入 30gA、30gB 和 30gC, 形成不饱和溶液的是。(4)、当 B 中混有少量的 A 时,可用的方法提纯 B。(5)、将 t2℃时等质量的 A,B,C 的饱和溶液降温到 t1℃,则下列说法正确的是(填序号)。A 溶质质量分数:A<C
B 溶剂质量:A>B
C 溶质质量:A>C
D 溶液质量:B>C
20. 实验室常用下列装置制取气体,请你根据所学知识回答下列问题. (1)、写出编号所指仪器的名称:① .(2)、A装置图中有一处明显的错误,请你找出错误的地方并把改正的结果填在下列横线上: .
(1)、写出编号所指仪器的名称:① .(2)、A装置图中有一处明显的错误,请你找出错误的地方并把改正的结果填在下列横线上: .上述装置改进后,请继续回答下列问题.
(3)、小李在实验室中用氯酸钾和另一种固体制取较纯净的氧气,他选择上述装置中的A和(填字母)进行组装,请你写出小李制取氧气的化学反应方程式 . 小红用上述装置制取二氧化碳应选用的发生装置和收集装置是(填写装置的字母代号),请写出该反应的化学方程式 . B 装置的优点是可随时控制反应的发生和停止.若打开旋钮,固体与液体接触,反应便能发生,请简述使B装置中反应停止的原理 .(4)、实验室常用一定质量分数的过氧化氢溶液制取氧气.某同学取少量二氧化锰于锥形瓶中,然后慢慢滴入34g过氧化氢溶液,完全反应后,生成氧气1.6g;求该同学所用过氧化氢溶液中溶质质量分数.
-