江苏省宿迁市宿豫区2021-2022学年九年级下学期期中化学试题
试卷更新日期:2023-03-01 类型:期中考试
一、单选题
-
1. 下列物质的用途与化学性质无关的是( )A、氧气用于医疗急救 B、用铝制作导线 C、用氦气充探空气球 D、二氧化碳灭火2. 2022年3月22日是第三十届世界水日,我国纪念2022年“世界水日”和“中国水周”活动的宣传主题为“推进地下水超采综合治理,复苏河湖生态环境”。下列关于水的说法正确的是( )A、使用无磷洗涤剂减少水体污染 B、淡水资源是取之不尽的 C、海水是纯净物 D、生活污水可以随意排放3. 下列有关粗盐提纯实验中的相关装置和操作,正确的是( )A、溶解粗盐

B、过滤食盐水
B、过滤食盐水 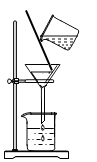
C、蒸发食盐水
C、蒸发食盐水 
D、冷却蒸发皿
D、冷却蒸发皿 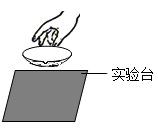
4. 掌握物质的性质和用途,可以为人类开启智慧之旅。下列说法错误的是( )A、用灼烧闻气味的方法可以鉴别蚕丝和合成纤维 B、糖类和维生素都能为人体提供能量 C、研制、生产可降解塑料可以缓解“白色污染”问题 D、包装食品的聚乙烯塑料袋可用加热的方法封口5. 下列说法错误的是( )A、同种元素的原子和离子具有相同的质子数 B、稀硫酸、盐酸中都含有大量H+ , 所以具有相似的化学性质 C、称取5.0g熟石灰,加入95.0mL水充分搅拌,得到5.0%的Ca(OH)2溶液 D、向盐酸与氢氧化钠充分反应后的溶液中滴入酚酞试液,不变色,则可能是酸过量6. 根据下列实验方案进行实验,能达到相应实验目的的是( )
4. 掌握物质的性质和用途,可以为人类开启智慧之旅。下列说法错误的是( )A、用灼烧闻气味的方法可以鉴别蚕丝和合成纤维 B、糖类和维生素都能为人体提供能量 C、研制、生产可降解塑料可以缓解“白色污染”问题 D、包装食品的聚乙烯塑料袋可用加热的方法封口5. 下列说法错误的是( )A、同种元素的原子和离子具有相同的质子数 B、稀硫酸、盐酸中都含有大量H+ , 所以具有相似的化学性质 C、称取5.0g熟石灰,加入95.0mL水充分搅拌,得到5.0%的Ca(OH)2溶液 D、向盐酸与氢氧化钠充分反应后的溶液中滴入酚酞试液,不变色,则可能是酸过量6. 根据下列实验方案进行实验,能达到相应实验目的的是( )编号
A
B
C
D
实验
方案



实验
目的
验证质量守恒定律
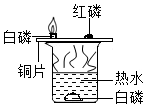
探究燃烧条件之一需要可燃物
探究铁钉生锈时O2是否参与反应
比较Zn和Fe的金属活动性强弱
A、A B、B C、C D、D7. 有X、Y、Z三种金属,为判断其活动性顺序,某兴趣小组的同学做了如下实验:①将X、Y、Z分别置于稀盐酸中,X有气体产生,Y、Z无明显现象;②将Y金属放入Z的盐溶液中,无现象。则X、Y、Z的活动性顺序为( )A、Y>Z>X B、X>Y>Z C、Y>X>Z D、X>Z>Y8. 将足量NH3和CO2依次通入饱和食盐水,发生反应:① ;② 。下列说法正确的是( )A、总的化学方程式为 B、上述反应过程中观察不到明显现象 C、反应②是有沉淀生成的复分解反应 D、上述反应中有元素化合价发生变化9. 提纯含少量NaCl杂质的KNO3 , 部分实验过程如下。相关物质的溶解度曲线如图所示。下列说法正确的是( )

 A、①→②,KNO3的溶解度不变 B、①→②,溶液中KNO3的质量分数不变 C、②→③,溶液中NaCl的质量增大 D、②→③,溶液中KNO3的质量减小10. 下列图像不能正确反映其对应变化关系的是( )A、
A、①→②,KNO3的溶解度不变 B、①→②,溶液中KNO3的质量分数不变 C、②→③,溶液中NaCl的质量增大 D、②→③,溶液中KNO3的质量减小10. 下列图像不能正确反映其对应变化关系的是( )A、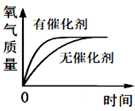 用等质量、等浓度的过氧化氢溶液在有无催化剂条件下制氧气
B、
用等质量、等浓度的过氧化氢溶液在有无催化剂条件下制氧气
B、 向HCl和MgCl2的混合溶液中加入NaOH溶液
C、
向HCl和MgCl2的混合溶液中加入NaOH溶液
C、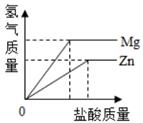 分别向相同质量的镁粉和锌粉中加入过量的稀盐酸
D、
分别向相同质量的镁粉和锌粉中加入过量的稀盐酸
D、 向饱和氢氧化钙溶液中加少量CaO
向饱和氢氧化钙溶液中加少量CaO
二、填空题
-
11. 用化学用语填空:
2个铁离子。氦气的化学式。K2MnO4中Mn的化合价。3个甲烷分子。
12. 中国古代四大发明之一的“黑火药”是由木炭(C)、硫粉(S)和硝酸钾(KNO3)按一定比例混合而成。(1)、分类。下列关于“黑火药”说法正确的是。a.“黑火药”由“黑火药分子”构成
b.“黑火药”中的KNO3属于复合肥料
c.“黑火药”中C,S不再保持各自的化学性质
(2)、变化。“黑火药”爆炸时发生的主要反应是:。①依据质量守恒定律,空格上缺少的物质是(填化学式)。
②“黑火药”爆炸时能闻到刺鼻的火药味,是因为爆炸时除了有硫化物,还有硫的氧化物生成。硫在空气中燃烧的化学方程式为。
(3)、制备。古代曾用硝土(主要成分Ca(NO3)2 , 其它不参加反应)和草木灰(含有K2CO3)作原料制取KNO3.某化学兴趣小组设计了如下实验流程: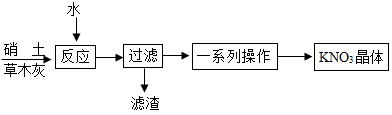
①“反应”过程中的化学方程式为。
②“过滤”操作必须用到的玻璃仪器有烧杯、玻璃棒和。
(4)、发展。现代国防、开矿等使用的烈性炸药,主要成分为硝化甘油(C3H5O9N3)。①硝化甘油在人体内能缓慢氧化生成一种氮的氧化物,用于治疗心绞痛。该氧化物中氮为+2价,其化学式为。
②硝化甘油中C、H、O、N四种元素的质量比为。
三、综合题
-
13. 实验是科学探究的重要方式,请结合图示回答下列问题:

 (1)、装置1常用于实验室测定空气中氧气含量。请写出红磷燃烧的化学方程式。(2)、装置2中的活性炭有性,可用于净化水;可以用鉴别软水和硬水,生活中常用的方法降低水的硬度。(3)、装置3常用于实验室电解水,与电源正极相连的玻璃管中收集的气体是;此实验可以证明水是由组成的。(4)、装置4可用于研究CO2与NaOH溶液的反应。关闭弹簧夹K,将NaOH溶液全部挤入烧瓶,振荡;然后打开弹簧夹K。观察到的实验现象: , 烧瓶中溶液变 , 写出该反应的化学方程式。14. 请结合如图回答问题。
(1)、装置1常用于实验室测定空气中氧气含量。请写出红磷燃烧的化学方程式。(2)、装置2中的活性炭有性,可用于净化水;可以用鉴别软水和硬水,生活中常用的方法降低水的硬度。(3)、装置3常用于实验室电解水,与电源正极相连的玻璃管中收集的气体是;此实验可以证明水是由组成的。(4)、装置4可用于研究CO2与NaOH溶液的反应。关闭弹簧夹K,将NaOH溶液全部挤入烧瓶,振荡;然后打开弹簧夹K。观察到的实验现象: , 烧瓶中溶液变 , 写出该反应的化学方程式。14. 请结合如图回答问题。 (1)、仪器名称:① , ②。(2)、用双氧水制取氧气可选用装置B和(填字母)组合,反应的化学方程式为。(3)、实验室制取CO2的化学方程式为 , 选用装置C相对B的优点是。(4)、已知CaCl2的水溶液呈中性。用图1装置探究制取CO2的实验。实验开始时,向锥形瓶中加入一定量的盐酸,图2表示实验过程中装置G和I中的溶液pH变化曲线。
(1)、仪器名称:① , ②。(2)、用双氧水制取氧气可选用装置B和(填字母)组合,反应的化学方程式为。(3)、实验室制取CO2的化学方程式为 , 选用装置C相对B的优点是。(4)、已知CaCl2的水溶液呈中性。用图1装置探究制取CO2的实验。实验开始时,向锥形瓶中加入一定量的盐酸,图2表示实验过程中装置G和I中的溶液pH变化曲线。

①装置H的作用为。
②t1时,锥形瓶中石灰石有剩余,无气泡产生。请判断t2时,锥形瓶中(填“有”或“无”)盐酸剩余。
③t1后,显示器B中曲线几乎无变化,其原因是。
15. 兴趣小组的同学为探究在空气中久置的某氢氧化钠样品是否变质,设计了如下图所示的A、B、C、D四组探究实验。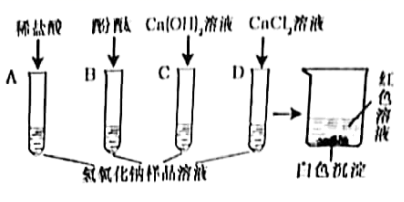
(查阅资料)氯化钙、氯化钡溶液都呈中性。
(实验探究)取适量该氢氧化钠样品,加足量的水溶解,将得到的溶液分别加入到四支试管中,再向四支试管中分别加入稀盐酸(足量)、酚酞试液、氢氧化钙溶液、氯化钙溶液,如图所示:
(1)、(分析与结论)上述四组实验中不能达到实验目的的是(填字母序号)。(2)、实验A中,观察到的现象,说明该氢氧化钠样品已经变质。(3)、实验D中,证明该氢氧化钠样品已经变质的反应的化学方程式是。(4)、(继续探究)实验结束后,同学们将四支试管中反应后的混合物全部倒入一个洁净的大烧杯中(如上图),充分搅拌、静置,观察到烧杯内上层清液呈红色,下层有白色沉淀。(提出问题)上层清液呈红色,说明溶液呈碱性。上层清液中呈碱性的物质是什么?
(猜想与假设)上层清液中呈碱性的物质可能是碳酸钠、氢氧化钙和三种物质中的一种或两种。
(5)、(设计实验)取少量烧杯中的上层清液于试管中,加入过量的氯化钡溶液,观察现象。(现象与结论)
预测现象
结论
①若有白色沉淀生成溶液呈红色
上层清液中呈碱性的物质是
②若无沉淀生成溶液呈红色
上层清液中呈碱性的物质是氢氧化钙
(6)、(实验反思)同学们认为上述预测现象②所得结论不严密,原因是。四、计算题
-
16. 某化学兴趣小组的同学在社会实践中,对废品回收站中废弃电器零部件黄铜(铜、锌合金)中铜的含量产生了兴趣,为了测定该黄铜中铜的含量,小组同学将黄铜带入化学实验室,称取该黄铜样品50克放入指定容器中,然后分四次加入稀硫酸,实验数据记录如下:
加入次数
第1次
第2次
第3次
第4次
加入稀硫酸质量(g)
100
100
100
100
充分反应后剩余固体质量(g)
43.5
37
35
n
请回答下列问题:
(1)、根据实验数据分析,n的数值应该为;(2)、黄铜样品中铜的质量分数为;(3)、所用稀硫酸溶质的质量分数。(写出计算过程)