高考化学真题重组卷 7+4专题冲刺 专题7 水溶液中的离子平衡及pH计算
试卷更新日期:2023-02-21 类型:三轮冲刺
一、单选题
-
1. 下图是亚砷酸As(OH)3和酒石酸混合体系中部分物种的c-pH图(浓度:总As为 , 总T为)。下列说法错误的是( )
 A、的为 B、的酸性比的强 C、时,的浓度比的高 D、时,溶液中浓度最高的物种为2. 常温下,一元酸的。在某体系中,与离子不能穿过隔膜,未电离的可自由穿过该膜(如图所示)。
A、的为 B、的酸性比的强 C、时,的浓度比的高 D、时,溶液中浓度最高的物种为2. 常温下,一元酸的。在某体系中,与离子不能穿过隔膜,未电离的可自由穿过该膜(如图所示)。
设溶液中 , 当达到平衡时,下列叙述正确的是( )
A、溶液Ⅰ中 B、溶液Ⅱ中的的电离度为 C、溶液Ⅰ和Ⅱ中的不相等 D、溶液Ⅰ和Ⅱ中的之比为3. 常温下,已知H3PO3溶液中含磷物种的浓度之和为0.1mol·L-1 , 溶液中各含磷物种的pc—pOH关系如图所示。图中pc表示各含磷物种的浓度负对数(pc=-lgc),pOH表示OH-的浓度负对数[pOH=-lgc(OH-)];x、y、z三点的坐标:x(7.3,1.3),y(10.0,3.6),z(12.6,1.3)。下列说法正确的是( ) A、曲线①表示pc(H3PO3)随pOH的变化 B、H3PO3的结构简式为
A、曲线①表示pc(H3PO3)随pOH的变化 B、H3PO3的结构简式为 C、pH=4的溶液中:c(H2PO )<0.1mol·L-1-2c(HPO )
D、H3PO3+HPO 2H2PO 的平衡常数K>1.0×105
4. 二氧化碳的过量排放可对海洋生物的生存环境造成很大影响,其原理如下图所示。下列叙述错误的是
C、pH=4的溶液中:c(H2PO )<0.1mol·L-1-2c(HPO )
D、H3PO3+HPO 2H2PO 的平衡常数K>1.0×105
4. 二氧化碳的过量排放可对海洋生物的生存环境造成很大影响,其原理如下图所示。下列叙述错误的是 A、海水酸化能引起 浓度增大、 浓度减小 B、海水酸化能促进CaCO3的溶解,导致珊瑚礁减少 C、CO2能引起海水酸化,其原理为
A、海水酸化能引起 浓度增大、 浓度减小 B、海水酸化能促进CaCO3的溶解,导致珊瑚礁减少 C、CO2能引起海水酸化,其原理为 H++
D、使用太阳能、氢能等新能源可改善珊瑚的生存环境
5. 以酚酞为指示剂,用0.1000 mol·L−1的NaOH溶液滴定20.00 mL未知浓度的二元酸H2A溶液。溶液中,pH、分布系数 随滴加NaOH溶液体积VNaOH的变化关系如图所示。[比如A2−的分布系数: ]
H++
D、使用太阳能、氢能等新能源可改善珊瑚的生存环境
5. 以酚酞为指示剂,用0.1000 mol·L−1的NaOH溶液滴定20.00 mL未知浓度的二元酸H2A溶液。溶液中,pH、分布系数 随滴加NaOH溶液体积VNaOH的变化关系如图所示。[比如A2−的分布系数: ]
下列叙述正确的是( )
A、曲线①代表 ,曲线②代表 B、H2A溶液的浓度为0.2000 mol·L−1 C、HA−的电离常数Ka=1.0×10−2 D、滴定终点时,溶液中6. 室温下进行下列实验,根据实验操作和现象所得到的结论正确的是( )选项
实验操作和现象
结论
A
向X溶液中滴加几滴新制氯水,振荡,再加入少量KSCN溶液,溶液变为红色
X溶液中一定含有Fe2+
B
向浓度均为0.05 mol·L−1的NaI、NaCl混合溶液中滴加少量AgNO3溶液,有黄色沉淀生成
Ksp(AgI)> Ksp(AgCl)
C
向3 mL KI溶液中滴加几滴溴水,振荡,再滴加1mL淀粉溶液,溶液显蓝色
Br2的氧化性比I2的强
D
用pH试纸测得:CH3COONa溶液的pH约为
9,NaNO2溶液的pH约为8
HNO2电离出H+的能力比CH3COOH的强
A、A B、B C、C D、D7. 某温度下, 和 的电离常数分别为 和 。将 和体积均相同的两种酸溶液分别稀释,其 随加水体积的变化如图所示。下列叙述正确的是( ) A、曲线Ⅰ代表 溶液 B、溶液中水的电离程度:b点>c点 C、从c点到d点,溶液中 保持不变(其中 、 分别代表相应的酸和酸根离子) D、相同体积a点的两溶液分别与 恰好中和后,溶液中 相同
A、曲线Ⅰ代表 溶液 B、溶液中水的电离程度:b点>c点 C、从c点到d点,溶液中 保持不变(其中 、 分别代表相应的酸和酸根离子) D、相同体积a点的两溶液分别与 恰好中和后,溶液中 相同二、综合题
-
8. 吸收工厂烟气中的SO2 , 能有效减少SO2对空气的污染。氨水、ZnO水悬浊液吸收烟气中SO2后经O2催化氧化,可得到硫酸盐。
已知:室温下,ZnSO3微溶于水,Zn(HSO3)2易溶于水;溶液中H2SO3、HSO3-、SO32-的物质的量分数随pH的分布如图-1所示。
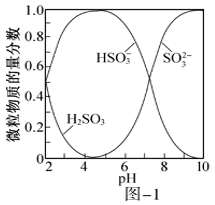 (1)、氨水吸收SO2。向氨水中通入少量SO2 , 主要反应的离子方程式为;当通入SO2至溶液pH=6时,溶液中浓度最大的阴离子是(填化学式)。(2)、ZnO水悬浊液吸收SO2。向ZnO水悬浊液中匀速缓慢通入SO2 , 在开始吸收的40mim内,SO2吸收率、溶液pH均经历了从几乎不变到迅速降低的变化(见图-2)。溶液pH几乎不变阶段,主要产物是(填化学式);SO2吸收率迅速降低阶段,主要反应的离子方程式为。
(1)、氨水吸收SO2。向氨水中通入少量SO2 , 主要反应的离子方程式为;当通入SO2至溶液pH=6时,溶液中浓度最大的阴离子是(填化学式)。(2)、ZnO水悬浊液吸收SO2。向ZnO水悬浊液中匀速缓慢通入SO2 , 在开始吸收的40mim内,SO2吸收率、溶液pH均经历了从几乎不变到迅速降低的变化(见图-2)。溶液pH几乎不变阶段,主要产物是(填化学式);SO2吸收率迅速降低阶段,主要反应的离子方程式为。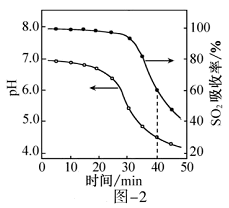 (3)、O2催化氧化。其他条件相同时,调节吸收SO2得到溶液的pH在4.5~6.5范围内,pH越低SO 生成速率越大,其主要原因是;随着氧化的进行,溶液的pH将(填“增大”、“减小”或“不变”)。9. 硼酸(H3BO3)是一种重要的化工原料,广泛应用于玻璃、医药、肥料等工艺。一种以硼镁矿(含Mg2B2O5·H2O、SiO2及少量Fe2O3、Al2O3)为原料生产硼酸及轻质氧化镁的工艺流程如下:
(3)、O2催化氧化。其他条件相同时,调节吸收SO2得到溶液的pH在4.5~6.5范围内,pH越低SO 生成速率越大,其主要原因是;随着氧化的进行,溶液的pH将(填“增大”、“减小”或“不变”)。9. 硼酸(H3BO3)是一种重要的化工原料,广泛应用于玻璃、医药、肥料等工艺。一种以硼镁矿(含Mg2B2O5·H2O、SiO2及少量Fe2O3、Al2O3)为原料生产硼酸及轻质氧化镁的工艺流程如下:
回答下列问题:
(1)、在95 ℃“溶侵”硼镁矿粉,产生的气体在“吸收”中反应的化学方程式为。(2)、“滤渣1”的主要成分有。为检验“过滤1”后的滤液中是否含有Fe3+离子,可选用的化学试剂是。(3)、根据H3BO3的解离反应:H3BO3+H2O H++B(OH)−4 , Ka=5.81×10−10 , 可判断H3BO3是酸;在“过滤2”前,将溶液pH调节至3.5,目的是。(4)、在“沉镁”中生成Mg(OH)2·MgCO3沉淀的离子方程式为 , 母液经加热后可返回工序循环使用。由碱式碳酸镁制备轻质氧化镁的方法是。10. (14分)H2S和SO2会对环境和人体健康带来极大的危害,工业上采取多种方法减少这些有害气体的排放,回答下列方法中的问题.Ⅰ.H2S的除去
方法1:生物脱H2S的原理为:
H2S+Fe2(SO4)3═S↓+2FeSO4+H2SO4
4FeSO4+O2+2H2SO4 2Fe2(SO4)3+2H2O
(1)、硫杆菌存在时,FeSO4被氧化的速率是无菌时的5×105倍,该菌的作用是 .(2)、由图1和图2判断使用硫杆菌的最佳条件为 . 若反应温度过高,反应速率下降,其原因是 .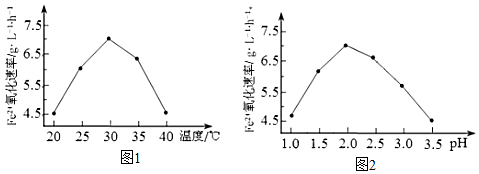 (3)、方法2:在一定条件下,用H2O2氧化H2S
(3)、方法2:在一定条件下,用H2O2氧化H2S随着参加反应的n(H2O2)/n(H2S)变化,氧化产物不同.当n(H2O2)/n(H2S)=4时,氧化产物的分子式为 .
(4)、Ⅱ.SO2的除去方法1(双碱法):用NaOH吸收SO2 , 并用CaO使NaOH再生
NaOH溶液 Na2SO3溶液
写出过程①的离子方程式:;CaO在水中存在如下转化:
CaO(s)+H2O (l)═Ca(OH)2(s)⇌Ca2+(aq)+2OH﹣(aq)
从平衡移动的角度,简述过程②NaOH再生的原理 .
(5)、方法2:用氨水除去SO2已知25℃,NH3•H2O的Kb=1.8×10﹣5 , H2SO3的Ka1=1.3×10﹣2 , Ka2=6.2×10﹣8 . 若氨水的浓度为2.0mol•L﹣1 , 溶液中的c(OH﹣)=mol•L﹣1 . 将SO2通入该氨水中,当c(OH﹣)降至1.0×10﹣7 mol•L﹣1时,溶液中的c(SO32﹣)/c(HSO3﹣)= .
11. (14分)(砷(As)是一些工厂和矿山废水中的污染元素,使用吸附剂是去除水中砷的有效措 施之一.(1)、将硫酸锰、硝酸钇与氢氧化钠溶液按一定比例混合,搅拌使其充分反应,可获得一种砷的高效吸附剂X,吸附剂X中含有CO32﹣ , 其原因是 .(2)、H3AsO3和H3AsO4水溶液中含砷的各物种的分布分数(平衡时某物种的浓度占各物种浓度之和的分数)与pH的关系分别如图﹣1和图﹣2所示.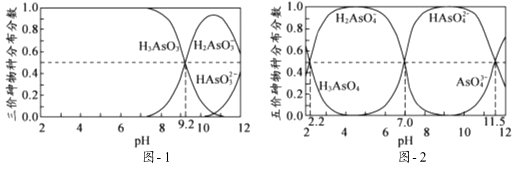
①以酚酞为指示剂(变色范围pH 8.0~10.0),将NaOH溶液逐滴加入到H3AsO3溶液中,当溶液由无色变为浅红色时停止滴加.该过程中主要反应的离子方程式为 .
②H3AsO4第一步电离方程式H3AsO4⇌H2AsO4﹣+H+的电离常数为Ka1 , 则pKa1=
(p Ka1=﹣lg Ka1 ).
(3)、溶液的pH对吸附剂X表面所带电荷有影响.pH=7.1时,吸附剂X表面不带电荷; pH>7.1时带负电荷,pH越高,表面所带负电荷越多;pH<7.1时带正电荷,pH越低,表面所带正电荷越多.pH不同时吸附剂X对三价砷和五价砷的平衡吸附量(吸附达平衡时单位质量吸附剂X吸附砷的质量)如图﹣3所示.
①在pH7~9之间,吸附剂X对五价砷的平衡吸附量随pH升高而迅速下降,其原因是 .
②在pH4~7之间,吸附剂X对水中三价砷的去除能力远比五价砷的弱,这是因为 . 提高吸附剂X对三价砷去除效果可采取的措施是 .