浙江省2018-2022年科学中考真题汇编20:酸和碱(基础)
试卷更新日期:2023-02-19 类型:二轮复习
一、单选题
-
1. 配制10%的稀硫酸并与碳酸钠粉末反应的部分操作如下,其中操作规范的是浓硫酸( )A、读取浓硫酸的体积
 B、稀释浓硫酸
B、稀释浓硫酸  C、加入碳酸钠
C、加入碳酸钠  D、倾倒稀硫酸
D、倾倒稀硫酸  2. 先秦时期,人们就知道在水中加入草木灰(含有K2CO3)来提高洗涤衣物的效果。下列物质与K2CO3溶液一样呈碱性的是( )
2. 先秦时期,人们就知道在水中加入草木灰(含有K2CO3)来提高洗涤衣物的效果。下列物质与K2CO3溶液一样呈碱性的是( )
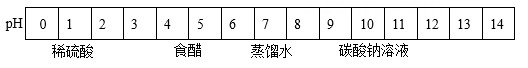 A、稀硫酸 B、食醋 C、蒸馏水 D、碳酸钠溶液3. 下列实验操作规范的是( )A、点燃酒精灯
A、稀硫酸 B、食醋 C、蒸馏水 D、碳酸钠溶液3. 下列实验操作规范的是( )A、点燃酒精灯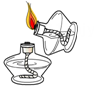 B、装固体粉末
B、装固体粉末  C、滴加液体
C、滴加液体  D、测溶液的pH
D、测溶液的pH  4. 物质的结构决定性质,性质决定用途。下列物质的结构、性质和用途之间匹配正确的是( )
4. 物质的结构决定性质,性质决定用途。下列物质的结构、性质和用途之间匹配正确的是( )选项
结构
性质
用途
A
稀盐酸中含有氢离子
具有酸性
具有酸性检验溶液中是否含有银离子
B
稀盐酸中含有氯离子
具有酸性
具有酸性检验溶液中是否含有银离子
C
氢氧化钠溶液中含有钠离子
具有碱性
具有碱性吸收二氧化硫气体
D
氢氧化钠溶液中含有氢氧根离子
具有碱性
具有碱性吸收二氧化硫气体
A、A B、B C、C D、D5. 科学以实验为基础,规范操作是科学实验取得成功的关键。下列实验操作规范的是( )A、加热液体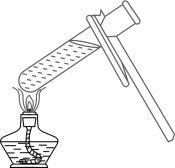 B、测溶液pH
B、测溶液pH 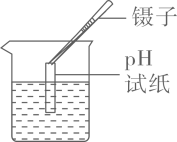 C、盖盖玻片
C、盖盖玻片 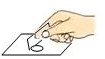 D、检查气密性
D、检查气密性  6. 在测定土壤酸碱性的实验中,下列操作规范的是( )A、装入土样粉末
6. 在测定土壤酸碱性的实验中,下列操作规范的是( )A、装入土样粉末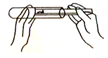 B、滴加蒸馏水
B、滴加蒸馏水 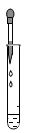 C、振荡土壤液
C、振荡土壤液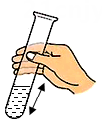 D、测定酸碱性
D、测定酸碱性 7. 如图是我们常见的水果及其近似pH,其中酸性最强的是( )A、西瓜pH=6.6
7. 如图是我们常见的水果及其近似pH,其中酸性最强的是( )A、西瓜pH=6.6 B、葡萄pH=5.1
B、葡萄pH=5.1  C、猕猴桃pH=3.3
C、猕猴桃pH=3.3  D、桔子pH=3.6
D、桔子pH=3.6  8. 台州气候适宜,盛产各种酸甜爽口的水果。深受市民喜爱,分析下表,酸性最强的水果是( )
8. 台州气候适宜,盛产各种酸甜爽口的水果。深受市民喜爱,分析下表,酸性最强的水果是( )水果名称
东魁杨梅
涌泉蜜桔
楚门文旦
玉麟西瓜
pH值
2.5~3.5
4.0-5.0
4.5~5.5
5.5-6.5
A、东魁杨梅 B、涌泉蜜桔 C、楚门文旦 D、玉麟西瓜9. 不同品牌的洗手液pH一般不同,25℃时四种洗手液的pH如图所示。下列说法错误的是( )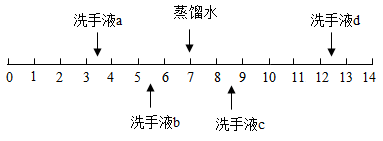 A、洗手液a用蒸馏水稀释后pH减小 B、洗手液b的酸性比a弱 C、洗手液c能使石蕊试液变蓝色 D、洗手液d和a混合液的pH可能等于710. 利用图形对概念间的关系进行归纳梳理,可以直观地反映两者的个性和共性。下列图形中左右两部分表示两个概念的个性,相交部分表示它们的共性,其中归纳梳理错误的是( )A、
A、洗手液a用蒸馏水稀释后pH减小 B、洗手液b的酸性比a弱 C、洗手液c能使石蕊试液变蓝色 D、洗手液d和a混合液的pH可能等于710. 利用图形对概念间的关系进行归纳梳理,可以直观地反映两者的个性和共性。下列图形中左右两部分表示两个概念的个性,相交部分表示它们的共性,其中归纳梳理错误的是( )A、 B、
B、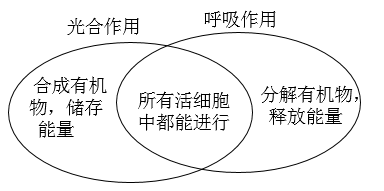 C、
C、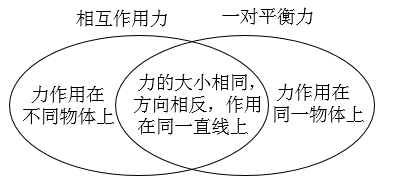 D、
D、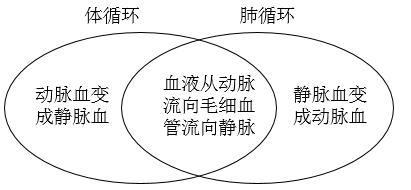 11. 将稀盐酸分别滴入NaOH溶液和NaCl溶液中,充分混合后均无明显现象。混合后相关变化的微观示意图如下,下列说法正确的是为( )
11. 将稀盐酸分别滴入NaOH溶液和NaCl溶液中,充分混合后均无明显现象。混合后相关变化的微观示意图如下,下列说法正确的是为( ) A、物质间均未发生化学反应 B、变化中都有新物质产生 C、混合后溶液酸碱性都不变 D、图甲可表示酸碱反应的实质12. 正确规范的操作是实验成功的关键,下列实验操作规范的是( )A、闻气味
A、物质间均未发生化学反应 B、变化中都有新物质产生 C、混合后溶液酸碱性都不变 D、图甲可表示酸碱反应的实质12. 正确规范的操作是实验成功的关键,下列实验操作规范的是( )A、闻气味 B、滴加液体
B、滴加液体  C、倾倒液体
C、倾倒液体  D、稀释浓硫酸
D、稀释浓硫酸  13. 新鲜果汁是常见的饮料,下列四种饮料呈弱碱性的是( )A、柠檬汁(pH:2~3)
13. 新鲜果汁是常见的饮料,下列四种饮料呈弱碱性的是( )A、柠檬汁(pH:2~3) B、苹果汁(pH:3~4)
B、苹果汁(pH:3~4)  C、西瓜汁(pH:5~6)
C、西瓜汁(pH:5~6)  D、玉米汁(pH:7~8)
D、玉米汁(pH:7~8)  14. 下列实验操作正确的是( )A、读取液体体积
14. 下列实验操作正确的是( )A、读取液体体积 B、闻气味
B、闻气味  C、测定溶液pH
C、测定溶液pH  D、稀释浓硫酸
D、稀释浓硫酸  15. 规范的操作是实验成功的基本保证,下列实验操作规范的是( )A、加热液体
15. 规范的操作是实验成功的基本保证,下列实验操作规范的是( )A、加热液体 B、测溶液pH
B、测溶液pH  C、气密性检查
C、气密性检查  D、稀释浓硫酸
D、稀释浓硫酸  16. 测量是一个把待测的量与公认的标准进行比较的过程。下列实验过程中没有用到这一科学原理的是( )A、用天平测出某物体的质量 B、用弹簧秤测出测出某物体的重力 C、用光学显微镜观察小鱼尾鳍内的血液流动 D、用pH试纸测出某溶液的pH17. 在科学实验和生活中,有许多涉及操作上的“先”“后”问题,如果顺序颠倒,就会影响实验效果或导致事故的发生。下列描述的操作中,先后顺序正确的是( )A、探究温度对唾液淀粉酶催化作用的影响时,先将唾液和淀粉溶液混合并等分为若干份,然后分别在不同温度下水浴 B、氢气还原氧化铜时,先对装有氧化铜的试管加热,然后通入氢气 C、稀释浓硫酸时,先在烧杯中倒入适量水,然后将浓硫酸沿烧杯壁缓缓倒入水中并用玻璃棒搅拌 D、发现有人接触漏电的家用电器而发生触电事故时,先用手迅速将触电者拉离电器,然后切断电源进行维修
16. 测量是一个把待测的量与公认的标准进行比较的过程。下列实验过程中没有用到这一科学原理的是( )A、用天平测出某物体的质量 B、用弹簧秤测出测出某物体的重力 C、用光学显微镜观察小鱼尾鳍内的血液流动 D、用pH试纸测出某溶液的pH17. 在科学实验和生活中,有许多涉及操作上的“先”“后”问题,如果顺序颠倒,就会影响实验效果或导致事故的发生。下列描述的操作中,先后顺序正确的是( )A、探究温度对唾液淀粉酶催化作用的影响时,先将唾液和淀粉溶液混合并等分为若干份,然后分别在不同温度下水浴 B、氢气还原氧化铜时,先对装有氧化铜的试管加热,然后通入氢气 C、稀释浓硫酸时,先在烧杯中倒入适量水,然后将浓硫酸沿烧杯壁缓缓倒入水中并用玻璃棒搅拌 D、发现有人接触漏电的家用电器而发生触电事故时,先用手迅速将触电者拉离电器,然后切断电源进行维修二、填空题
-
18. 洗衣机槽清洁剂的主要成分是过碳酸钠(Na2CO4),过碳酸钠是一种白色晶体,溶于水时会与水反应生成碳酸钠和过氧化氢(化学方程式为:Na2CO4+H2O=Na2CO3+H2O2)。现取少许过碳酸钠晶体,加入水形成溶液。(1)、取少量二氧化锰加入试管中,再加入适量该溶液,观察到有气泡产生,为了检验该气体,可用(2)、待不再产生气泡时,得到的溶液呈(选填“酸性”或“中性”或“碱性”)。(3)、生成的碳酸钠中碳元素的化合价为。19. 物质结构决定性质,性质决定用途,现象反映本质。如图是小科构建的硫酸部分知识网络,其中“一”表示相连物质能发生化学反应。
 (1)、石蕊试液在H2SO4溶液中显红色,该溶液中能使石蕊试液变红的离子是。(2)、在实验室中常用浓硫酸做干燥剂,这是利用它的。20. 物质结构决定性质,物质性质决定用途,反应本质决定变化现象。如图是小科构建的氢氧化钙部分知识网络,其中“一”表示相连物质能发生化学反应,X与图中所给物质的类别不同。请回答:
(1)、石蕊试液在H2SO4溶液中显红色,该溶液中能使石蕊试液变红的离子是。(2)、在实验室中常用浓硫酸做干燥剂,这是利用它的。20. 物质结构决定性质,物质性质决定用途,反应本质决定变化现象。如图是小科构建的氢氧化钙部分知识网络,其中“一”表示相连物质能发生化学反应,X与图中所给物质的类别不同。请回答: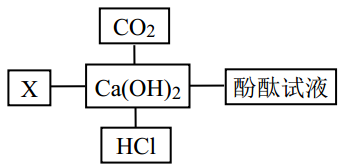 (1)、酚酞试液在Ca(OH)2溶液中显红色,能使酚酞试液变红的离子是(2)、列举熟石灰[Ca(OH)2]在工农业上的一种用途;(3)、X溶液能与Ca(OH)2溶液反应并产生蓝色絮状沉淀,写出产生该实验现象的一个化学方程式。21. 根据物质的特征反应进行物质的鉴别是一种常用的科学方法。现有两瓶失去标签的氯化钠溶液和碳酸钠溶液,分别标为A和B。鉴别试剂有无色酚酞试液、稀盐酸和硝酸银溶液。某同学选用无色酚酞试液进行鉴别,发现A溶液不变色,由此可确定A是溶液。他还可以选择上述试剂中的进行鉴别。22. 物质的酸碱性与我们的生活密切相关。(1)、酸性是因为物质能电离出 , 可以使紫色石蕊试液变色。(2)、酸碱性强弱可用pH表示,通常洗衣粉、香皂呈碱性,即pH7.
(1)、酚酞试液在Ca(OH)2溶液中显红色,能使酚酞试液变红的离子是(2)、列举熟石灰[Ca(OH)2]在工农业上的一种用途;(3)、X溶液能与Ca(OH)2溶液反应并产生蓝色絮状沉淀,写出产生该实验现象的一个化学方程式。21. 根据物质的特征反应进行物质的鉴别是一种常用的科学方法。现有两瓶失去标签的氯化钠溶液和碳酸钠溶液,分别标为A和B。鉴别试剂有无色酚酞试液、稀盐酸和硝酸银溶液。某同学选用无色酚酞试液进行鉴别,发现A溶液不变色,由此可确定A是溶液。他还可以选择上述试剂中的进行鉴别。22. 物质的酸碱性与我们的生活密切相关。(1)、酸性是因为物质能电离出 , 可以使紫色石蕊试液变色。(2)、酸碱性强弱可用pH表示,通常洗衣粉、香皂呈碱性,即pH7.三、实验探究题
-
23. 酸碱理论的发展如下:
 (1)、根据朴素的酸碱理论,Na2CO3属于(选填“酸”或“碱”)。(2)、根据酸碱电离理论理解酸碱反应的实质是: 。(3)、已知H2CO3→ +H+和 →CO32-+H+ , 由酸碱质子理论,H2CO3的共轭碱是 。(4)、随着认知水平的不断提高,人们对酸碱理论的描述也在不断完善。下列对不同酸碱理论的分析合理的是 。A、酸碱电离理论认为酸碱是两种不同的物质 B、酸碱电离理论认为氧元素是酸中必不可少的元素 C、酸碱质子理论认为酸和碱可以是分子,也可以是离子 D、酸碱质子理论扩大了酸和碱的范围,不再具有局限性24. 某同学要在一块空地上种植作物,于是对这块空地的土壤酸碱度进行测定。(1)、在空地上确定5~6个位置进行取样测定壤酸碱度。以下三种取样位置设定合理的是。
(1)、根据朴素的酸碱理论,Na2CO3属于(选填“酸”或“碱”)。(2)、根据酸碱电离理论理解酸碱反应的实质是: 。(3)、已知H2CO3→ +H+和 →CO32-+H+ , 由酸碱质子理论,H2CO3的共轭碱是 。(4)、随着认知水平的不断提高,人们对酸碱理论的描述也在不断完善。下列对不同酸碱理论的分析合理的是 。A、酸碱电离理论认为酸碱是两种不同的物质 B、酸碱电离理论认为氧元素是酸中必不可少的元素 C、酸碱质子理论认为酸和碱可以是分子,也可以是离子 D、酸碱质子理论扩大了酸和碱的范围,不再具有局限性24. 某同学要在一块空地上种植作物,于是对这块空地的土壤酸碱度进行测定。(1)、在空地上确定5~6个位置进行取样测定壤酸碱度。以下三种取样位置设定合理的是。 (2)、将采集到的土样进行处理后,用玻璃棒蘸取土壤浸出液,滴在上,将其呈现的颜色与标准比色卡比色.确定了空地土壤的pH约为7.查阅资料,常见作物最适宜生长的土壤pH范围如下表,则这块空地上适合种植的作物有。
(2)、将采集到的土样进行处理后,用玻璃棒蘸取土壤浸出液,滴在上,将其呈现的颜色与标准比色卡比色.确定了空地土壤的pH约为7.查阅资料,常见作物最适宜生长的土壤pH范围如下表,则这块空地上适合种植的作物有。作物
大蒜
丝瓜
茄子
沙枣
最适pH范围
5.6~6.0
6.0~6.5
6.8~7.3
8.0~8.7
25. 氯气(Cl2)是一种黄绿色气体,它可溶于水,得到黄绿色的氯水。它易与氢氧化钠反应,不与硫酸反应。(1)、小明对氯气溶于水的过程中所发生的变化提出了两种假设:假设1:氯气溶于水的过程中只有物理变化
假设2:氯气溶于水的过程中既有物理变化又有化学变化
小明向氯水中加入紫色石蕊试液,发现溶液先变红后褪色。由溶液变红可知氯水显 性,从而知道氯气溶于水的过程中发生了化学变化。假设2成立。
(2)、小明对褪色现象产生了兴趣,查阅资料后了解到氯水有漂白性。氯水中有氯气分子,还有氯气与水反应得到的盐酸和次氯酸(HClO)。他对氯水的漂白性提出了3种假设:A.盐酸有漂白性
B.氯气有漂白性
C.次氯酸有漂白性
经过认真思考,小明否定了假设A,请写出依据 。
实验室制备的氯气往往带有水蒸气和其他杂质。为了探究氯气是否具有漂白性,必须要用纯净、干燥的氯气。图甲是小明为了干燥氯气所设计的装置图。请在图甲中将广口瓶中的导管画完整,并在图中的处写出试剂名称。最后,将经过除杂后得到的干燥氯气通入装有有色布条的试管中(如图乙),布条颜色不变。得出结论:氯气不具有漂白性。
 (3)、次氯酸除有漂白性外还有不稳定性。小明设计了一套装置,收集到一试管次氯酸见光分解后生成的气体,将带火星的木条伸入试管,发现木条复燃,说明分解产物中含有。
(3)、次氯酸除有漂白性外还有不稳定性。小明设计了一套装置,收集到一试管次氯酸见光分解后生成的气体,将带火星的木条伸入试管,发现木条复燃,说明分解产物中含有。四、解答题
-
26. 黄铜(铜和锌的合金)因性能优良,被广泛用于制作钱币、饰品和生产中,铜的质量分数在59%~65%之间的黄铜性能优良。兴趣小组为了解某黄铜螺母的材料性能进行如下实验:取多个黄铜螺母放入烧杯中,另取80克l9.6%的稀硫酸,分四次等质量加入,每次均充分反应,实验过程数据记录如下表。
实验次数
1
2
3
4
稀硫酸的用量/克
20
20
20
20
剩余固体的质量/克
20.0
17.4
14.8
13.5
分析上述数据,请回答下列问题:
(1)、第4次实验结束后溶液的pH 7(选填”>”“=”或“<”)
(2)、配制80克溶质质量分数为19.6%的稀硫酸,需98%的浓硫酸(密度为1.84克/厘米3)多少毫升?(精确到小数点后一位)
(3)、通过计算说明该黄铜螺母的材料性能是否优良。
27. 小明取一包某食品包装袋内的“脱氧剂”,查阅资料发现其成分除铁粉外,可能含有碳粉、Na2CO3、NaCl、Fe2O3等。为确定其成分,进行了如下实验: (1)、过滤操作中除了需带铁圈的铁架台、滤纸、玻璃棒外,还需要用到的仪器有 。(2)、写出用pH试纸测定滤液pH的方法:。(3)、试剂X的名称是。
(1)、过滤操作中除了需带铁圈的铁架台、滤纸、玻璃棒外,还需要用到的仪器有 。(2)、写出用pH试纸测定滤液pH的方法:。(3)、试剂X的名称是。