湖南省岳阳市城区2019-2020学年九年级上学期期末化学试题
试卷更新日期:2023-02-10 类型:期末考试
一、单选题
-
1. 生活中会发生各种变化,下列变化属于化学变化的是( )A、干冰升华 B、蜡烛燃烧 C、活性炭吸附异味 D、用海水制蒸馏水2. 下列实验基本操作正确的是 ( )A、熄灭酒精灯
 B、倾倒液体
B、倾倒液体 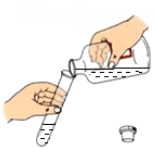 C、气体验满
C、气体验满  D、液体过滤
D、液体过滤 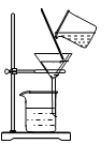 3. 下列有关空气的说法中,错误的是( )A、空气的成分按体积计算,含量最高的是氮气 B、植树造林有利于保护空气 C、二氧化碳是一种空气污染物 D、稀有气体可用作多种用途的电光源4. 有关电解水实验的下列叙述中,错误的是( )A、可证明水由氢、氧元素组成 B、与电源正极相连的一端产生氧气 C、正、负极产生的气体质量比是1∶2 D、在水中加氢氧化钠可增强水的导电性5. 2019年是“国际化学元素周期表年”。制出第一张元素周期表的科学家的是( )A、舍勒 B、道尔顿 C、门捷列夫 D、阿伏加德罗6. 金属钒被誉为“金属的维生素”,其化合物五氧化二钒是工业制硫酸的催化剂,五氧化二钒(V2O5)中钒元素的化合价是()A、﹣3 B、+1 C、+3 D、+57. 建立宏观和微观之间的联系对学习化学十分重要。下列宏观事实的微观解释错误的是( )A、品红在水中扩散——分子在不断运动 B、水蒸发由液态变成气态——水分子发生改变 C、NO与NO2化学性质不同——构成物质的分子不同 D、10mL 水与10mL 酒精混合后体积小于20mL——分子间有间隔8. 下列四种粒子的结构示意图中,说法正确的是( )
3. 下列有关空气的说法中,错误的是( )A、空气的成分按体积计算,含量最高的是氮气 B、植树造林有利于保护空气 C、二氧化碳是一种空气污染物 D、稀有气体可用作多种用途的电光源4. 有关电解水实验的下列叙述中,错误的是( )A、可证明水由氢、氧元素组成 B、与电源正极相连的一端产生氧气 C、正、负极产生的气体质量比是1∶2 D、在水中加氢氧化钠可增强水的导电性5. 2019年是“国际化学元素周期表年”。制出第一张元素周期表的科学家的是( )A、舍勒 B、道尔顿 C、门捷列夫 D、阿伏加德罗6. 金属钒被誉为“金属的维生素”,其化合物五氧化二钒是工业制硫酸的催化剂,五氧化二钒(V2O5)中钒元素的化合价是()A、﹣3 B、+1 C、+3 D、+57. 建立宏观和微观之间的联系对学习化学十分重要。下列宏观事实的微观解释错误的是( )A、品红在水中扩散——分子在不断运动 B、水蒸发由液态变成气态——水分子发生改变 C、NO与NO2化学性质不同——构成物质的分子不同 D、10mL 水与10mL 酒精混合后体积小于20mL——分子间有间隔8. 下列四种粒子的结构示意图中,说法正确的是( ) A、它们表示四种不同的元素 B、②表示的元素在化合物中通常显+2价 C、④表示的元素是非金属元素 D、①④表示的是阳离子9. 分类法是化学学习和研究中重要的方法之一,下列分类完全正确的是( )A、金属单质铁铜硅 B、稀有气体氦气氮气氖气 C、氧化物水二氧化碳氧化铁 D、清洁能源氢气酒精汽油10. 如图所示有关二氧化碳的实验中,只能证明二氧化碳物理性质的是()A、
A、它们表示四种不同的元素 B、②表示的元素在化合物中通常显+2价 C、④表示的元素是非金属元素 D、①④表示的是阳离子9. 分类法是化学学习和研究中重要的方法之一,下列分类完全正确的是( )A、金属单质铁铜硅 B、稀有气体氦气氮气氖气 C、氧化物水二氧化碳氧化铁 D、清洁能源氢气酒精汽油10. 如图所示有关二氧化碳的实验中,只能证明二氧化碳物理性质的是()A、 B、
B、 C、
C、 D、
D、 11. 锑是一种重要的稀土金属,湖南是锑的主要产地之一。下列关于锑的说法正确的是( )
11. 锑是一种重要的稀土金属,湖南是锑的主要产地之一。下列关于锑的说法正确的是( ) A、相对原子质量为51 B、元素符号为Sb C、原子的核外电子数为121.8 D、该元素为非金属元素12. 西班牙的瑞奥汀河是一条酸河,河水中含有硫酸和硫酸亚铁。经调查发现,酸河形成的原因是由于上游河床含有的某种物质R在水中氧的作用下发生反应所致,其反应的化学方程式为:2R+2H2O+7O2 =2FeSO4+2H2SO4 , 则R的化学式为( )A、FeS B、Fe2S3 C、FeS2 D、FeO13. 2019年5月12日是我国第11个“防灾减灾日”,了解防灾减灾的相关知识,有利保护人们的生命、财产安全。下列关于火灾、灭火与逃生的说法错误的是()A、严禁携带易燃、易爆物品乘坐火车 B、遭遇火灾,如果火势较大,立即拨打119电话报警 C、生活中常用水来灭火,其原理是降低可燃物着火点 D、从火场中逃生时,应有序撤离着火区域14. 肉毒碱(化学式为C7H15NO3)是一种具有多种生理功能的物质,被公认为人体必需的营养物质和最佳的减肥营养素。下列关于肉毒碱的叙述错误的是( )A、由四种元素组成 B、每个分子中含有26个原子 C、相对分子质量为161 D、碳、氢、氮、氧四种元素的质量比为7∶15∶1∶315. 在一个密闭容器中放入 M、N、Q、P 四种物质,在一定条件下发生化学反应,一段时间后,测得有关数据如下表,则关于此反应认识错误的是()
A、相对原子质量为51 B、元素符号为Sb C、原子的核外电子数为121.8 D、该元素为非金属元素12. 西班牙的瑞奥汀河是一条酸河,河水中含有硫酸和硫酸亚铁。经调查发现,酸河形成的原因是由于上游河床含有的某种物质R在水中氧的作用下发生反应所致,其反应的化学方程式为:2R+2H2O+7O2 =2FeSO4+2H2SO4 , 则R的化学式为( )A、FeS B、Fe2S3 C、FeS2 D、FeO13. 2019年5月12日是我国第11个“防灾减灾日”,了解防灾减灾的相关知识,有利保护人们的生命、财产安全。下列关于火灾、灭火与逃生的说法错误的是()A、严禁携带易燃、易爆物品乘坐火车 B、遭遇火灾,如果火势较大,立即拨打119电话报警 C、生活中常用水来灭火,其原理是降低可燃物着火点 D、从火场中逃生时,应有序撤离着火区域14. 肉毒碱(化学式为C7H15NO3)是一种具有多种生理功能的物质,被公认为人体必需的营养物质和最佳的减肥营养素。下列关于肉毒碱的叙述错误的是( )A、由四种元素组成 B、每个分子中含有26个原子 C、相对分子质量为161 D、碳、氢、氮、氧四种元素的质量比为7∶15∶1∶315. 在一个密闭容器中放入 M、N、Q、P 四种物质,在一定条件下发生化学反应,一段时间后,测得有关数据如下表,则关于此反应认识错误的是()物质
M
N
Q
P
反应前质量(g)
18
1
2
32
反应后质量(g)
x
26
2
12
A、该变化的基本反应类型是分解反应 B、反应后物质x的值为13 C、反应中 N、P 的质量比为5:4 D、物质Q可能是该反应的催化剂二、填空题
-
16. 用正确的化学符号填空:(1)、二个氮原子。(2)、镁离子。17. 请选择下列物质的正确序号填入适当空格中:
①石墨②金刚石③活性炭④一氧化碳⑤二氧化碳
(1)、有毒且易与血红蛋白结合的物质是;(2)、有良好的导电性可以用做干电池电极的是;18. 元素周期表是学习和研究化学的重要工具,它的内容十分丰富。下表是依据元素周期表画出的1~10号元素的原子结构示意图,对它进行研究: (1)、上述粒子中,化学性质相似的有(填该原子的原子序数);(2)、上面的粒子之间能形成AB4型分子的化学式。19. 根据如图微观示意图分析:
(1)、上述粒子中,化学性质相似的有(填该原子的原子序数);(2)、上面的粒子之间能形成AB4型分子的化学式。19. 根据如图微观示意图分析: (1)、图中甲是由构成的,物质丙CH3OH的相对分子质量为;(2)、通过观察可以得出微观角度化学反应的实质是;(3)、写出在一定条件下甲、乙反应的化学方程式。
(1)、图中甲是由构成的,物质丙CH3OH的相对分子质量为;(2)、通过观察可以得出微观角度化学反应的实质是;(3)、写出在一定条件下甲、乙反应的化学方程式。三、综合题
-
20. 甲、乙、丙是我们化学学习中常见的物质,它们之间有如图所示的转化关系(“→”表示反应一步实现,部分反应物和反应条件略去)。
 (1)、如果甲是固体单质,乙丙常温下是组成元素相同的气体,则甲可能是;(2)、如果甲丙常温下为液态,则乙可能是;写出甲转变为乙的化学方程式。
(1)、如果甲是固体单质,乙丙常温下是组成元素相同的气体,则甲可能是;(2)、如果甲丙常温下为液态,则乙可能是;写出甲转变为乙的化学方程式。四、综合题
-
21. Si是重要的半导体材料,半导体工业中有一句行话“从沙滩到用户”,指的是利用石英砂(主要成分SiO2)制取高纯度的Si。已知硅与碳有相似的化学性质,SiHCl3(三氯氢硅)能与水反应,其工艺流程和主要化学反应如图:

①2C+SiO2Si(不纯)+2CO↑②3HCl+Si(不纯)SiHCl3+H2
(1)、反应②中是还原剂;(2)、根据H2和SiHCl3性质推断整个制备过程除达到高温外,还必须注意条件;(3)、物质A循环利用(填能还是不能);(4)、试写出反应③的化学方程式。22. 根据下列实验装置图,回答问题: (1)、写出仪器a、b的名称:a;b;(2)、实验室常用B装置制取二氧化碳,反应物为稀盐酸和大理石,其反应化学方程式为。(3)、实验室用无水醋酸钠和碱石灰两种固体加热来制取甲烷气体,甲烷难溶于水且密度比空气小,制取甲烷可选用的发生装置是(填序号,下同),收集甲烷可选用的装置是。23. 某同学为了探究木炭和氧化铜在高温条件下生成的气体产物的成分,提出了如下猜想:
(1)、写出仪器a、b的名称:a;b;(2)、实验室常用B装置制取二氧化碳,反应物为稀盐酸和大理石,其反应化学方程式为。(3)、实验室用无水醋酸钠和碱石灰两种固体加热来制取甲烷气体,甲烷难溶于水且密度比空气小,制取甲烷可选用的发生装置是(填序号,下同),收集甲烷可选用的装置是。23. 某同学为了探究木炭和氧化铜在高温条件下生成的气体产物的成分,提出了如下猜想:
a、可能是二氧化碳;
b、可能是一氧化碳。
并设计如图所示装置进行实验,预期的实验现象及结论如下:
Ⅰ、若澄清的石灰水变浑浊。则气体为二氧化碳;
Ⅱ、若澄清的石灰水不变浑浊。则气体为一氧化碳。
请你分析并回答:
(1)、另一位同学认为该同学的猜想不严谨,提出了第三种猜想。这位同学的猜想是:;(2)、为验证这位同学的猜想,他设计了如下实验方案。实验方案
预期实验现象
预期实验结论
①先将气体通过澄清的石灰水
石灰水变浑浊
气体中有
②再通过足量的石灰水溶液
无明显现象
该过程的目的是
③然后气体通过灼热的氧化铜
气体中有一氧化碳
五、计算题
-
24. 某同学在实验室用氯酸钾和二氧化锰的混合物制取氧气,并对反应后固体剩余物进行回收、利用,实验操作流程及数据记录如下:

求:
(1)、该同学制得氧气的质量g。(2)、反应前固体中所含氯酸钾的质量。
-