湖南省郴州市2022-2023学年九年级上学期期末化学试题
试卷更新日期:2023-02-10 类型:期末考试
一、单选题
-
1. 下列是防控“新冠肺炎”的“三字经”,其中涉及化学变化的是( )A、带口罩 B、测体温 C、勤消毒 D、常通风2. 下列有关试管使用的实验操作中错误的是( )A、
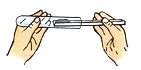 取用固体粉末
B、
取用固体粉末
B、 连接仪器
C、
连接仪器
C、 加热固体
D、
加热固体
D、 检查装置气密性
3. 空气和水是人类生活和生产不可缺少的自然资源。下列说法错误的是( )A、空气中的二氧化碳是植物进行光合作用必需的物质 B、空气中的氧气能供给生物呼吸,支持燃料燃烧 C、地球上的水总储量虽然很大,但淡水很少,我们要节约用水 D、用水浇灭燃烧的木材—降低可燃物的着火点4. 下列各组物质,按混合物、化合物、单质的顺序排列的是( )A、冰水共存物、干冰、氮气 B、石油、天然气、煤 C、洁净的空气、氯化钠、液态氧 D、石灰水、水银、铜5. 下列关于“化学与生活”的认识错误的是( )A、在家中准备一盆冷水,可防止煤气中毒 B、食品包装常用氮气冲气包装,利用氮气化学性质不活泼 C、饮用井水时先煮沸,既可降低水的硬度,又可杀死水中的细菌 D、把煤球做成蜂窝状,大大的增大了可燃物与氧气的接触面积6. 下列事实不能作为相应观点的证据的是( )
检查装置气密性
3. 空气和水是人类生活和生产不可缺少的自然资源。下列说法错误的是( )A、空气中的二氧化碳是植物进行光合作用必需的物质 B、空气中的氧气能供给生物呼吸,支持燃料燃烧 C、地球上的水总储量虽然很大,但淡水很少,我们要节约用水 D、用水浇灭燃烧的木材—降低可燃物的着火点4. 下列各组物质,按混合物、化合物、单质的顺序排列的是( )A、冰水共存物、干冰、氮气 B、石油、天然气、煤 C、洁净的空气、氯化钠、液态氧 D、石灰水、水银、铜5. 下列关于“化学与生活”的认识错误的是( )A、在家中准备一盆冷水,可防止煤气中毒 B、食品包装常用氮气冲气包装,利用氮气化学性质不活泼 C、饮用井水时先煮沸,既可降低水的硬度,又可杀死水中的细菌 D、把煤球做成蜂窝状,大大的增大了可燃物与氧气的接触面积6. 下列事实不能作为相应观点的证据的是( )选项
事实
观点
A
水分解成氢气和氧气
分子是可以再分的
B
一氧化碳能还原氧化铜,而二氧化碳不能
分子种类不同,化学性质不同
C
温度越高,蔗糖在水中溶解得越快
温度越高,分子的运动速率越快
D
干冰升华变为二氧化碳气体
化学变化中分子种类发生改变
A、A B、B C、C D、D7. 对于Cu、Cu2+、Cu+三种粒子的判断,正确的是( )①核电荷数相同②核外电子数相同③电子层结构完全相同④相对原子质量几乎相等
A、①②③④ B、①③ C、①④ D、②③8. 下列排序正确的是( )A、地壳中元素含量: B、空气中体积分数:
B、空气中体积分数: C、金属活动性顺序:
C、金属活动性顺序: D、氯元素的化合价:
D、氯元素的化合价: 9. 下列化学反应中不属于基本反应类型的是( )A、 B、 C、 D、10. 家居装修时,装饰材料会释放出一种叫甲醛【CH2O】的有害气体,下列关于甲醛的说法中正确的是( )A、甲醛是由碳原子和水分子构成的 B、甲醛中含4个原子 C、甲醛中碳、氢、氧三种元素的质量比是1:2:1 D、甲醛是由碳、氢、氧三种元素组成11. 人工光合固碳装置通过电化学手段将二氧化碳还原为甲酸(HCOOH)。该反应的微观示意图如下,有关该反应的说法错误的是( )
9. 下列化学反应中不属于基本反应类型的是( )A、 B、 C、 D、10. 家居装修时,装饰材料会释放出一种叫甲醛【CH2O】的有害气体,下列关于甲醛的说法中正确的是( )A、甲醛是由碳原子和水分子构成的 B、甲醛中含4个原子 C、甲醛中碳、氢、氧三种元素的质量比是1:2:1 D、甲醛是由碳、氢、氧三种元素组成11. 人工光合固碳装置通过电化学手段将二氧化碳还原为甲酸(HCOOH)。该反应的微观示意图如下,有关该反应的说法错误的是( ) A、从反应价值看:可减少CO2的排放 B、从粒子数量看:反应中生成物的分子个数比为1:1 C、从价态变化看:反应前后有元素化合价改变 D、从守恒关系看:反应前后原子的种类、数目不变12. 质量相等的两份氯酸钾a和b,向b中加入少量的高锰酸钾,完全反应后,下列图像能正确表示氧气的质量随时间变化关系的是( )
A、从反应价值看:可减少CO2的排放 B、从粒子数量看:反应中生成物的分子个数比为1:1 C、从价态变化看:反应前后有元素化合价改变 D、从守恒关系看:反应前后原子的种类、数目不变12. 质量相等的两份氯酸钾a和b,向b中加入少量的高锰酸钾,完全反应后,下列图像能正确表示氧气的质量随时间变化关系的是( )



A
B
C
D
A、A B、B C、C D、D13. 下列实验方案设计错误的是( )选项
实验目的
实验方案
A
检验某种无色气体是否为CH4
点燃,并通入澄清石灰水,观察现象
B
验证Zn、Cu、Ag三种金属的活动性强弱
将Zn、Ag分别加入CuSO4溶液中,观察现象
C
区别过氧化氢溶液和水
加入少量二氧化锰,观察现象
D
除去FeCl2溶液中混有的CuCl2
加入过量的Fe粉,过滤
A、A B、B C、C D、D14. 密闭容器中有甲、乙、丙、丁四种物质,在一定条件下反应,测得其反应前后各物质在密闭容器中所占的质量分数如下、下列说法正确的是( )物质
甲
乙
丙
丁
反应前质量百分比
15%
m
60%
20%
反应后质量百分比
n
5%
0
70%
A、乙物质是该反应的催化剂 B、该反应是化合反应 C、反应中甲和丙的质量比是15:60 D、丙物质一定是化合物15. 工业甲醇是一种有毒液体,略有酒精的气味,误饮会使人中毒,当氧气不足时,甲醇(CH3OH)燃烧会生成CO2、CO和H2O,若12g甲醇燃烧生成CO2和CO的质量比为22:7,则参加反应的O2的质量为( )A、8g B、16g C、18g D、32g二、填空题
-
16. 用化学符号填空。(1)、氧化铁;(2)、两个硫原子;(3)、硬水中含有较多的钙离子和;(4)、画出铝的原子结构示意图;(5)、标出KIO3中碘元素的化合价。17. 用符合要求物质的序号填空:
①氮气;②干冰;③石墨;④氧气;⑤酒精。
(1)、常用于电池电极的是;(2)、常用作火箭助燃剂的是;(3)、属于绿色能源的是;(4)、用于人工降雨的是;(5)、常用作制氮肥的原料的是。18. 在宏观、微观和符号之间建立联系是化学学科的重要思维方式。请根据图中信息回答下列问题。

 (1)、在A,B,C,D,E中容易失电子的是(填字母),表示阳离子的是(写离子符号),属于稳定结构的原子是(填字母)。(2)、镍是第周期的元素,镍的相对原子质量是。19. 第24届冬奥会于2022年2月4日在北京隆重举行,本届冬奥会体现了绿色环保理念。(1)、冬奥会速滑馆“冰丝带”制冰采用了世界上最先进的二氧化碳跨临界直冷制冰技术。制冰过程中,二氧化碳发生了物理变化,从微粒的角度分析,变化的原因是发生了改变。(2)、冬奥会用氢能源汽车作为交通工具。专家研究出一种新型的催化剂,在光照下实现水的高效分解制氢气,其中部分过程的微观示意图如图所示:
(1)、在A,B,C,D,E中容易失电子的是(填字母),表示阳离子的是(写离子符号),属于稳定结构的原子是(填字母)。(2)、镍是第周期的元素,镍的相对原子质量是。19. 第24届冬奥会于2022年2月4日在北京隆重举行,本届冬奥会体现了绿色环保理念。(1)、冬奥会速滑馆“冰丝带”制冰采用了世界上最先进的二氧化碳跨临界直冷制冰技术。制冰过程中,二氧化碳发生了物理变化,从微粒的角度分析,变化的原因是发生了改变。(2)、冬奥会用氢能源汽车作为交通工具。专家研究出一种新型的催化剂,在光照下实现水的高效分解制氢气,其中部分过程的微观示意图如图所示:
请写出反应Ⅰ的化学方程式。
(3)、化学助力防疫:过氧乙酸常用于教室消毒,其化学性质不稳定,分解的化学方程式为: , 则X的化学式为。(4)、2022年“世界水日”的主题是“珍惜地下水,珍惜隐藏的资源”,生活、生产中我们都离不开水。郴州某地井水中有异味,可利用活性炭的性除去异味。20. 金属材料在生产、生活中具有广泛的应用。(1)、铁锅用来炒菜,主要是利用铁的性。(2)、铝合金是目前使用比较广泛的金属材料,街道上的垃圾桶的内胆更合适用铝合金的原因是。(用化学方程式表示)(3)、目前科学家正在研究以“氢能炼钢”替代“焦炭炼钢”。这两种工艺相比,“氢能炼钢”的主要优点有。(4)、防止钢铁制品的锈蚀可避免财产损失,写一条防止钢铁制品腐蚀的措施:。三、综合题
-
21. A、B、C和D是初中化学中常见的四种不同物质,都含有一种相同的元素,其中D为大理石的主要成分,其转化关系如图所示:
 (1)、A,B,C,D所含相同的元素名称是。(2)、说出C的一种用途:。(3)、若由A→C的反应中生成物有铜,该反应发生时观察到的现象为。(4)、写出由D→C的反应中属于分解反应的化学方程式。22. 下图是初中化学实验室制取气体的常用装置,请回答下列问题:
(1)、A,B,C,D所含相同的元素名称是。(2)、说出C的一种用途:。(3)、若由A→C的反应中生成物有铜,该反应发生时观察到的现象为。(4)、写出由D→C的反应中属于分解反应的化学方程式。22. 下图是初中化学实验室制取气体的常用装置,请回答下列问题: (1)、写出标号仪器名称:②。(2)、实验室若用A装置制取并收集一瓶较纯净的O2时,选用的收集装置是:(填字母),写出该反应的化学方程式:。(3)、若用B、C装置制取并收集另一种无色气体,则B中加入的液体药品液面高度应该在(填B装置中的“a”或“b”)处,请写出检验该气体的化学方程式。(4)、用图G的装置进行铁丝在O2中燃烧的实验,容易导致集气瓶炸裂,为了避免这种情况,应采取的措施是。(5)、实验室常用加热无水醋酸钠和碱石灰固体的方法制取甲烷气体。则制备并收集一瓶甲烷气体的装置组合是(填字母,任写一种即可)。23. 回答问题(1)、某研究性学习小组为验证铜、铁、锌三种金属的活动性,进行了如图所示实验:
(1)、写出标号仪器名称:②。(2)、实验室若用A装置制取并收集一瓶较纯净的O2时,选用的收集装置是:(填字母),写出该反应的化学方程式:。(3)、若用B、C装置制取并收集另一种无色气体,则B中加入的液体药品液面高度应该在(填B装置中的“a”或“b”)处,请写出检验该气体的化学方程式。(4)、用图G的装置进行铁丝在O2中燃烧的实验,容易导致集气瓶炸裂,为了避免这种情况,应采取的措施是。(5)、实验室常用加热无水醋酸钠和碱石灰固体的方法制取甲烷气体。则制备并收集一瓶甲烷气体的装置组合是(填字母,任写一种即可)。23. 回答问题(1)、某研究性学习小组为验证铜、铁、锌三种金属的活动性,进行了如图所示实验:
研究性学习小组根据气球膨胀的快慢得出的结论是:铁>锌>铜,结论与我们学习的知识不符,你认为要使实验成功,除了用砂纸打磨外还应该怎样改正: , 改正后的实验中气球膨胀最快的是。(选填“A、B或C”)
(2)、用如图所示的装置进行实验,验证可燃物燃烧的条件并测定空气中氧气含量(已知白磷的着火点为40℃,红磷的着火点为240℃)。
①验证可燃物燃烧的条件:向Y型管中放入足量红磷和白磷,塞好橡胶塞,关闭弹簧夹。然后将Y型管放入80℃的热水中,观察到红磷不燃烧,白磷燃烧,说明可燃物燃烧的条件之一是 , 写出该反应的化学方程式。
②测定空气中氧气含量:已知Y型管的容积是60mL,待白磷熄灭,装置冷却至室温后,打开弹簧夹,会观察到量筒中的水约减少了mL。
四、计算题
-
24. 牛奶是我们日常生活中一种营养丰富的饮品,每天饮用可补充我们对钙等营养物质的需求。其中营养成分的具体含量如下表所示。
项目
能量
蛋白质
脂肪
碳水化合物
钠
钙
非脂乳固体
每100mL
272kJ
3.2g
3.8g
4.5g
60mg
110mg
≥8.1%
请根据资料回答下列问题:
(1)、通常中学生每天需从牛奶中补充550mg的钙,若一盒牛奶为250mL,则理论上每天应喝盒牛奶。(2)、牛奶中的钙主要以磷酸钙[Ca3(PO4)2]的形式存在,①磷酸钙的相对分子质量=;②钙元素的质量分数约为(结果保留至0.1%)。25. 长期使用的热水壶底部有一层水垢,水垢的主要成分是碳酸钙。某化学兴趣小组为测定水垢中碳酸钙的含量,将过量的稀盐酸加入到20g水垢中(其它成分反应不生成CO2或不与盐酸反应),再将产生的CO2气体用足量的澄清石灰水吸收,石灰水增加的质量随时间的变化如下表所示。时间/s
0
20
40
60
80
100
增加的质量/g
0
3.0
5.0
5.5
5.5
5.5
(1)、20g该水垢与过量的稀盐酸反应生成的二氧化碳的总质量是g。(2)、水垢中碳酸钙的质量分数是多少?