河南省信阳市光山县2022-2023学年九年级上学期期末化学试题
试卷更新日期:2023-02-10 类型:期末考试
一、单选题
-
1. 下列变化属于化学变化的是( )A、干冰升华 B、食物腐烂 C、石油分馏 D、汽油挥发2. 2019年环境日的主题是“美丽中国,我是行动者”。下列行为与主题不符合的是( )A、垃圾分类回收处理 B、使用共享单车绿色出行 C、提倡使用清洁能源 D、倡导使用一次性筷子3. 下列各图所表示的化学实验操作正确的是( )A、
 闻气体气味
B、
闻气体气味
B、 倾倒液体
C、
倾倒液体
C、 添加药品
D、
添加药品
D、 检查气密性
4. 为相对原子质量的测定作出了贡献的中国科学家是( )A、杨振宁 B、屠呦呦 C、张青莲 D、袁隆平5. 下列有关化学实验操作的先后顺序正确的是( )A、实验室制取二氧化碳时,先加稀盐酸,后加石灰石 B、实验室制取二氧化碳时,先装药品,后检查装置的气密性 C、组装制取氧气的实验装置时,先左后右、先下后上 D、用氯酸钾制取氧气实验结束时,先熄灭酒精灯,后从水中移出导管6. 下列关于电解水实验的说法错误的是( )A、证明了水是由氢元素和氧元素组成的 B、负极产生的气体可以使带火星的木条复燃 C、相关反应可表示为 2H2O2H2↑+O2↑ D、反应前后元素种类没变但物质种类发生了改变7. 下列对实验现象的描述正确的是( )A、木炭在空气中燃烧,发出白光 B、铁丝在空气中燃烧,火星四射 C、硫在空气中燃烧,产生蓝紫色火焰 D、氢气在空气中燃烧,产生淡蓝色火焰8. 尿素是一种高效氮肥,其化学成分为 CO(NH2)2 , 下列有关尿素的叙述正确的是( )A、尿素中碳、氢元素的个数比为 1:4 B、尿素由碳、氢、氧、氮四种原子构成 C、尿素是由 CO(NH2)2 分子构成 D、尿素中氮元素的质量分数为×100%9. 构成下列物质的微粒与构成干冰的微粒属于同一类别的是( )A、金刚石 B、C60 C、硫酸铜 D、铜10. 利用天平及下列物品(必要时还可用燃着的酒精灯),能够直接用于验证质量守恒定律的是( )A、
检查气密性
4. 为相对原子质量的测定作出了贡献的中国科学家是( )A、杨振宁 B、屠呦呦 C、张青莲 D、袁隆平5. 下列有关化学实验操作的先后顺序正确的是( )A、实验室制取二氧化碳时,先加稀盐酸,后加石灰石 B、实验室制取二氧化碳时,先装药品,后检查装置的气密性 C、组装制取氧气的实验装置时,先左后右、先下后上 D、用氯酸钾制取氧气实验结束时,先熄灭酒精灯,后从水中移出导管6. 下列关于电解水实验的说法错误的是( )A、证明了水是由氢元素和氧元素组成的 B、负极产生的气体可以使带火星的木条复燃 C、相关反应可表示为 2H2O2H2↑+O2↑ D、反应前后元素种类没变但物质种类发生了改变7. 下列对实验现象的描述正确的是( )A、木炭在空气中燃烧,发出白光 B、铁丝在空气中燃烧,火星四射 C、硫在空气中燃烧,产生蓝紫色火焰 D、氢气在空气中燃烧,产生淡蓝色火焰8. 尿素是一种高效氮肥,其化学成分为 CO(NH2)2 , 下列有关尿素的叙述正确的是( )A、尿素中碳、氢元素的个数比为 1:4 B、尿素由碳、氢、氧、氮四种原子构成 C、尿素是由 CO(NH2)2 分子构成 D、尿素中氮元素的质量分数为×100%9. 构成下列物质的微粒与构成干冰的微粒属于同一类别的是( )A、金刚石 B、C60 C、硫酸铜 D、铜10. 利用天平及下列物品(必要时还可用燃着的酒精灯),能够直接用于验证质量守恒定律的是( )A、 B、
B、 C、
C、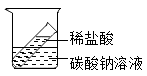 D、
D、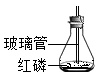 11. 下列化学方程式中书写正确且属于置换反应的是( )A、氢气还原氧化铜:H2+CuOCu+H2O B、甲烷燃烧:CH4+2O2CO2+2H2O C、生石灰与水的反应:CaO+H2O=Ca(OH)2 D、用氯酸钾制取氧气:2KClO32KCl+ 3O2↑12. 闭容器内,有甲、乙、丙、丁四种物质在一定条件下充分混合反应,测得反应前后各物质的质量分数如图所示。下列说法正确的是( )
11. 下列化学方程式中书写正确且属于置换反应的是( )A、氢气还原氧化铜:H2+CuOCu+H2O B、甲烷燃烧:CH4+2O2CO2+2H2O C、生石灰与水的反应:CaO+H2O=Ca(OH)2 D、用氯酸钾制取氧气:2KClO32KCl+ 3O2↑12. 闭容器内,有甲、乙、丙、丁四种物质在一定条件下充分混合反应,测得反应前后各物质的质量分数如图所示。下列说法正确的是( ) A、丁一定是化合物 B、反应生成甲和丙的质量比为8:1 C、该反应是化合反应 D、乙一定是该反应的催化剂13. 下列图象能正确反映对应关系的是( )A、
A、丁一定是化合物 B、反应生成甲和丙的质量比为8:1 C、该反应是化合反应 D、乙一定是该反应的催化剂13. 下列图象能正确反映对应关系的是( )A、 用相等质量的氯酸钾制取氧气
B、
用相等质量的氯酸钾制取氧气
B、 将水通电一段时间
C、
将水通电一段时间
C、 足量的锌、铁放入一定量的盐酸溶液中
D、
足量的锌、铁放入一定量的盐酸溶液中
D、 加热一定质量的高锰酸钾制氧气
14. 氧化钙和碳酸钙的固体混合物质量为100g,将其高温煅烧至碳酸钙完全分解,称得剩余固体的质量为70g。则原固体混合物中钙元素的质量分数为( )A、20% B、40% C、50% D、70%
加热一定质量的高锰酸钾制氧气
14. 氧化钙和碳酸钙的固体混合物质量为100g,将其高温煅烧至碳酸钙完全分解,称得剩余固体的质量为70g。则原固体混合物中钙元素的质量分数为( )A、20% B、40% C、50% D、70%二、填空题
-
15. 空气中体积分数约为78%的气体是 , 天然气的主要成分是。16. 开封市的“一渠六河”工程以绿为骨,将构建“河畅、水清,岸绿、景美”的水生态体系。在河道上设置拦污网拦截漂浮垃圾,其原理类似于化学实验操作中的;还可以利用活性炭的性除去水中的色素和异味;水分解可制取氢气,氢气作为新能源其主要优点是(答一点即可)。17. 我国“高分五号”企谱段高光谱卫星,其天线是用钛镍形状记忆合金制成的。如图是镍在元素周期表中的部分信息及原子结构示意图,则镍的相对原子质量为;图中x=;镍元素在元素周期表中处在第周期。
 18. 港珠澳大桥是世界最长的跨海钢桥,施工中用了大量的钢材并采用了先进的防锈技术。(1)、钢铁制品在空气中容易与等物质接触而生锈。(2)、利用下图所示的微型实验装置模拟赤铁矿炼铁。
18. 港珠澳大桥是世界最长的跨海钢桥,施工中用了大量的钢材并采用了先进的防锈技术。(1)、钢铁制品在空气中容易与等物质接触而生锈。(2)、利用下图所示的微型实验装置模拟赤铁矿炼铁。
①写出a处反应的化学方程式。
②从环保角度考虑,写出一种尾气处理方法。
19. 老师利用图甲装置测定空气中氧气的含量并结合现代传感器技术,测得过程中容器内气体压强、温度、氧气浓度的变化趋势如图乙所示。 (1)、t2时打开止水夹,最终水面大约上升至集气瓶刻度处。(2)、结合乙图曲线,BC段气体压强发生变化的原因是。20. 能源是人类生存和发展的基础。(1)、探究燃烧条件的实验装置如图所示,能够得出燃烧条件之一为“与氧气接触”的实验现象是什么?
(1)、t2时打开止水夹,最终水面大约上升至集气瓶刻度处。(2)、结合乙图曲线,BC段气体压强发生变化的原因是。20. 能源是人类生存和发展的基础。(1)、探究燃烧条件的实验装置如图所示,能够得出燃烧条件之一为“与氧气接触”的实验现象是什么? (2)、为节约能源,使燃料充分燃烧,应采取哪些措施?(写出一条即可)21. “宏观辨识与微观探析"是化学核心素养之一。
(2)、为节约能源,使燃料充分燃烧,应采取哪些措施?(写出一条即可)21. “宏观辨识与微观探析"是化学核心素养之一。工业上用甲和乙两种物质在一定条件下反应生成丙和丁,反应的微观示意图如下所示。
 (1)、反应前后化合价没有变化的元素是什么?(2)、写出该反应的化学方程式。22. 一氧化碳不仅可作燃料,还可用于冶炼金属,如图是实验室利用 CO 还原氧化铁的装置示意图,请完成以下问题。
(1)、反应前后化合价没有变化的元素是什么?(2)、写出该反应的化学方程式。22. 一氧化碳不仅可作燃料,还可用于冶炼金属,如图是实验室利用 CO 还原氧化铁的装置示意图,请完成以下问题。 (1)、写出 A 装置中的实验现象:。(2)、写出 B 试管中发生反应的化学方程式:。(3)、请从微观角度分析CO 和CO2性质不同的原因:。
(1)、写出 A 装置中的实验现象:。(2)、写出 B 试管中发生反应的化学方程式:。(3)、请从微观角度分析CO 和CO2性质不同的原因:。三、综合题
-
23. A~F 均为初中化学常见的物质,它们之间的关系如图所示(部分物质已略去),其中 D 是石灰石的主要成分,C 为最常见的液体,且 C 与 E 元素组成相同,请回答下列问题:
 (1)、E 的化学式为。(2)、写出 B 和 C 反应的化学方程式:。(3)、写出 E→F 的化学方程式:。24. 请结合图示回答下列问题。
(1)、E 的化学式为。(2)、写出 B 和 C 反应的化学方程式:。(3)、写出 E→F 的化学方程式:。24. 请结合图示回答下列问题。 (1)、用高锰酸钾制取较为纯净的氧气,应选用的发生装置和收集装置是(填序号),该反应的化学方程式为。(2)、在实验室,既能用来制取氧气,又能用来制取二氧化碳的发生装置是(填序号)。25. 金属及其化合物是中学化学学习的重要内容。(1)、《梦溪笔谈》中记载:“古人以剂刚为刃,柔铁为茎干,不尔则多断折。”剂刚、柔铁均为铁的合金,这主要是因为合金比纯金属____。(填序号)A、硬度大、耐腐蚀 B、硬度小、熔点高 C、熔点高、耐腐蚀(2)、某兴趣小组为探究 Zn、Fe、Cu、Ag 四种金属的活动性,进行如图中甲、乙、丙三个实验。
(1)、用高锰酸钾制取较为纯净的氧气,应选用的发生装置和收集装置是(填序号),该反应的化学方程式为。(2)、在实验室,既能用来制取氧气,又能用来制取二氧化碳的发生装置是(填序号)。25. 金属及其化合物是中学化学学习的重要内容。(1)、《梦溪笔谈》中记载:“古人以剂刚为刃,柔铁为茎干,不尔则多断折。”剂刚、柔铁均为铁的合金,这主要是因为合金比纯金属____。(填序号)A、硬度大、耐腐蚀 B、硬度小、熔点高 C、熔点高、耐腐蚀(2)、某兴趣小组为探究 Zn、Fe、Cu、Ag 四种金属的活动性,进行如图中甲、乙、丙三个实验。
①请写出丙实验中的化学方程式:。
②小组同学随后发现该实验无法得出四种金属的活动性顺序,于是补充图丁实验,最终得出四种金属活动性:Zn>Fe >Cu>Ag,则图丁中的试剂 A、B 分别为。(写出一组即可)。
(3)、某化学实验室从含少量硝酸锌的硝酸银废液中提取金属 Ag,其主要操作流程如图:
①固体 A 的成分有;
②步骤Ⅰ、Ⅱ共同的实验操作中,玻璃棒的作用是;
③请写出步骤Ⅱ中加入过量稀硫酸的原因:;若往溶液 D 中加入适量的铁粉,则发生反应的化学方程式为。
(4)、2019 年诺贝尔化学奖授予三位化学家,以表彰他们在锂离子电池领域的研发工作。利用锂与水的反应可制成锂水电池,作为潜艇的储备电源。已知锂与水反应生成氢氧化锂(LiOH)和一种具有可燃性的单质气体,若消耗 21g 锂,则生成的单质气体质量为多少克?