北京市西城区2022-2023学年九年级上学期期末化学试题
试卷更新日期:2023-02-08 类型:期末考试
一、单选题
-
1. 地壳中含量最多的元素是( )A、硅 B、氧 C、铁 D、铝2. 下列新年活动中,主要利用了化学变化的是A、敲钟迎新 B、燃放礼花 C、制作冰雕 D、张贴对联3. 下列图标中表示禁止吸烟的是( )A、
 B、
B、 C、
C、 D、
D、 4. “补钙剂”中的“钙”指的是A、单质 B、元素 C、分子 D、原子5. 下列气体中,有毒的是( )A、N2 B、O2 C、CO D、CO26. 下列物质在O2中燃烧,火星四射,生成黑色固体的是( )A、木炭 B、镁条 C、蜡烛 D、铁丝7. 下列元素符号书写错误的是A、镁Mg B、氮N C、银AG D、氯Cl8. 下列仪器中,不能加热的是A、量筒 B、烧杯 C、燃烧匙 D、试管9. 下列物质中含有氧分子的是A、O2 B、KMnO4 C、H2O2 D、CO210. 室温下收集一瓶氢气,其中约含有3×1021个氢分子,这说明A、分子的体积很小 B、分子间有间隔 C、分子在不断运动 D、分子是保持物质化学性质的最小粒子11. 下列物质的化学式书写错误的是A、氢氧化钠NaOH B、硫酸铜CuSO4 C、氯化亚铁FeCl2 D、氧化钠NaO12. 下列实验操作正确的是A、
4. “补钙剂”中的“钙”指的是A、单质 B、元素 C、分子 D、原子5. 下列气体中,有毒的是( )A、N2 B、O2 C、CO D、CO26. 下列物质在O2中燃烧,火星四射,生成黑色固体的是( )A、木炭 B、镁条 C、蜡烛 D、铁丝7. 下列元素符号书写错误的是A、镁Mg B、氮N C、银AG D、氯Cl8. 下列仪器中,不能加热的是A、量筒 B、烧杯 C、燃烧匙 D、试管9. 下列物质中含有氧分子的是A、O2 B、KMnO4 C、H2O2 D、CO210. 室温下收集一瓶氢气,其中约含有3×1021个氢分子,这说明A、分子的体积很小 B、分子间有间隔 C、分子在不断运动 D、分子是保持物质化学性质的最小粒子11. 下列物质的化学式书写错误的是A、氢氧化钠NaOH B、硫酸铜CuSO4 C、氯化亚铁FeCl2 D、氧化钠NaO12. 下列实验操作正确的是A、 点燃酒精灯
B、
点燃酒精灯
B、 量取液体
C、
量取液体
C、 滴加液体
D、
滴加液体
D、 取块状固体
13. 下列节水措施不恰当的是( )A、工厂废水处理后循环使用 B、推广使用节水龙头 C、用洗菜水冲洗马桶 D、生活污水任意排放14. 北京冬奥会火种灯中的燃料为丙烷(C3H8),其燃烧的化学方程式为。下列说法错误的是A、丙烷和氧气在点燃条件下反应生成水和二氧化碳 B、反应前后分子的数目不变 C、反应后的产物均属于氧化物 D、丙烷燃烧放出热量15. 下列灭火方法所用原理与其他三个不同的是A、用砂子盖灭燃着的木柴 B、用灯帽盖灭酒精灯 C、油锅中的油着火用锅盖盖灭 D、森林火灾时将火场周围树木砍伐掉16. 下列化学方程式书写正确的是A、 B、 C、 D、17. 下列实验操作不能达到实验目的的是
取块状固体
13. 下列节水措施不恰当的是( )A、工厂废水处理后循环使用 B、推广使用节水龙头 C、用洗菜水冲洗马桶 D、生活污水任意排放14. 北京冬奥会火种灯中的燃料为丙烷(C3H8),其燃烧的化学方程式为。下列说法错误的是A、丙烷和氧气在点燃条件下反应生成水和二氧化碳 B、反应前后分子的数目不变 C、反应后的产物均属于氧化物 D、丙烷燃烧放出热量15. 下列灭火方法所用原理与其他三个不同的是A、用砂子盖灭燃着的木柴 B、用灯帽盖灭酒精灯 C、油锅中的油着火用锅盖盖灭 D、森林火灾时将火场周围树木砍伐掉16. 下列化学方程式书写正确的是A、 B、 C、 D、17. 下列实验操作不能达到实验目的的是实验目的
实验操作
A
除去河水中的泥沙
过滤
B
除去CO2中的少量CO
点燃气体
C
鉴别硬水和软水
取等量水样,分别滴加等量肥皂水,振荡
D
鉴别CO和CH4
分别点燃,在火焰上方罩干冷烧杯
A、A B、B C、C D、D18. 某小组利用图1装置研究25℃时二氧化碳的溶解性。打开止水夹,向3个充满二氧化碳的100mL烧瓶中,分别注入20mL、40mL、60mL蒸馏水,关闭止水夹,振荡前后压强的变化如图2.下列说法错误的是 A、曲线①中ab段对应的操作是迅速注入蒸馏水 B、曲线①中c点和e点可能进行了振荡 C、曲线③对应的实验是注入60mL蒸馏水 D、终点气压高于初始的原因可能是在25℃时,1体积水中最多吸收的二氧化碳的量小于1体积
A、曲线①中ab段对应的操作是迅速注入蒸馏水 B、曲线①中c点和e点可能进行了振荡 C、曲线③对应的实验是注入60mL蒸馏水 D、终点气压高于初始的原因可能是在25℃时,1体积水中最多吸收的二氧化碳的量小于1体积二、选择题组
-
19. 2022年5月,中国科学家推导出可控核聚变燃料极限的新定律,在解决能源危机的道路上迈出了重要一步。完成下面小题。(1)、核聚变的原料氘原子()和氚原子()统称氢元素,它们之间的不同之处可能是A、质子数不同 B、中子数不同 C、核外电子数不同 D、最外层电子数不同(2)、下列符号中,表示两个氢原子的是A、2H B、2H+ C、H2 D、2H2(3)、生产重水时,需对天然水进行净化。下列净水方法中,净化程度最高的是A、沉降 B、吸附 C、过滤 D、蒸馏20. 2021年4月,毅力号火星车成功利用火星大气富含的二氧化碳制出氧气,这是人类首次在地外行星制氧。完成下面小题。(1)、氧气属于( )A、单质 B、化合物 C、氧化物 D、混合物(2)、火星制氧的主要反应的微观示意图如下,下列说法正确的是( )
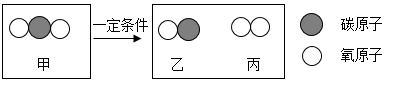 A、甲中碳、氧元素质量比为1:2 B、生成乙和丙的分子个数比为1:1 C、反应后氧原子个数增加 D、属于分解反应21. 二氧化碳与生产生活息息相关。完成下面小题。(1)、下列方法能鉴别空气、氧气和二氧化碳3瓶气体的是A、闻气味 B、倒入适量的水 C、观察颜色 D、伸入燃着的木条(2)、二氧化碳的下列用途中,主要利用其物理性质的是A、灭火 B、人工降雨 C、生产纯碱(Na2CO3) D、光合作用(3)、下列做法不利于控制二氧化碳排放的是A、提倡公共出行 B、植树造林 C、推广燃油汽车 D、利用二氧化碳制氧气22. 中国口腔专家发现钛酸钡(BaTiO3)可美白牙齿。生产BaTiO3的反应为;钛元素在元素周期表中的信息如下图。完成下面小题。
A、甲中碳、氧元素质量比为1:2 B、生成乙和丙的分子个数比为1:1 C、反应后氧原子个数增加 D、属于分解反应21. 二氧化碳与生产生活息息相关。完成下面小题。(1)、下列方法能鉴别空气、氧气和二氧化碳3瓶气体的是A、闻气味 B、倒入适量的水 C、观察颜色 D、伸入燃着的木条(2)、二氧化碳的下列用途中,主要利用其物理性质的是A、灭火 B、人工降雨 C、生产纯碱(Na2CO3) D、光合作用(3)、下列做法不利于控制二氧化碳排放的是A、提倡公共出行 B、植树造林 C、推广燃油汽车 D、利用二氧化碳制氧气22. 中国口腔专家发现钛酸钡(BaTiO3)可美白牙齿。生产BaTiO3的反应为;钛元素在元素周期表中的信息如下图。完成下面小题。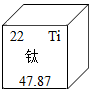 (1)、下列有关钛元素的说法错误的是A、元素符号是Ti B、原子序数是22 C、属于非金属元素 D、相对原子质量为47.87(2)、钛原子的核外电子数是A、22 B、26 C、48 D、70(3)、TiO2中钛元素的化合价是A、+1 B、+2 C、+3 D、+4(4)、下列有关钛酸钡的说法错误的是A、由三种元素组成 B、由5个原子构成 C、相对分子质量为233 D、氧元素的质量分数计算式为
(1)、下列有关钛元素的说法错误的是A、元素符号是Ti B、原子序数是22 C、属于非金属元素 D、相对原子质量为47.87(2)、钛原子的核外电子数是A、22 B、26 C、48 D、70(3)、TiO2中钛元素的化合价是A、+1 B、+2 C、+3 D、+4(4)、下列有关钛酸钡的说法错误的是A、由三种元素组成 B、由5个原子构成 C、相对分子质量为233 D、氧元素的质量分数计算式为三、填空题
-
23. 空气中的各种成分用途广泛。(1)、空气中体积分数最大的物质是。(2)、氧气可用于医疗急救,是因为氧气能。(3)、氮气的化学性质不活泼,可用做。24. 2021年北京市空气质量首次全面达标。(1)、对空气造成污染的是___________(填序号)。A、SO2 B、PM2.5 C、N2(2)、北京市是最早实施机动车污染物国六B排放标准的城市。
①发动机上安装颗粒捕捉器,可使尾气中的碳颗粒在高温下燃烧,以达到国六B排放标准。碳颗粒充分燃烧的化学方程式为。
②排气系统中安装催化器,可使尾气中的CO、NO2催化转化为CO2和N2 , 该反应的化学方程式为。
25. 下面是两种海水淡化的原理示意图。
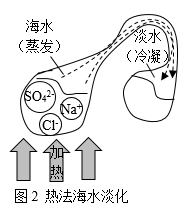 (1)、图1中,加压后钠离子、镁离子等不能通过反渗透膜。镁离子的符号是。(2)、图2中,海水蒸发冷凝得到淡水的过程中,不发生变化的是___________(填序号)。A、分子的质量 B、分子的种类 C、分子的间隔26. 目前使用的燃料大多来自化石燃料。(1)、化石燃料包括煤、、天然气等。(2)、天然气的主要成分充分燃烧的化学方程式为。(3)、依下图分析:燃烧后更易导致酸雨的燃料是。为减少该污染应采取的措施是。
(1)、图1中,加压后钠离子、镁离子等不能通过反渗透膜。镁离子的符号是。(2)、图2中,海水蒸发冷凝得到淡水的过程中,不发生变化的是___________(填序号)。A、分子的质量 B、分子的种类 C、分子的间隔26. 目前使用的燃料大多来自化石燃料。(1)、化石燃料包括煤、、天然气等。(2)、天然气的主要成分充分燃烧的化学方程式为。(3)、依下图分析:燃烧后更易导致酸雨的燃料是。为减少该污染应采取的措施是。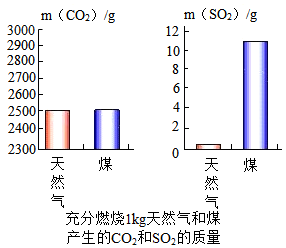 27. 开发和利用新能源是解决能源问题的重要途径。(1)、下列应用利用了新能源的是___________(填序号)。A、太阳能飞机 B、风力发电机 C、潮汐能动力机(2)、氢气是理想的清洁能源。
27. 开发和利用新能源是解决能源问题的重要途径。(1)、下列应用利用了新能源的是___________(填序号)。A、太阳能飞机 B、风力发电机 C、潮汐能动力机(2)、氢气是理想的清洁能源。①氢气燃烧的化学方程式为。
②自然界中水是氢的大“仓库”。若全球水的总质量为1.38×1021kg,其中氢元素质量的计算式为。
28. 电池是生活中常见的储能设备。(1)、锂电池工作时,锂原子释放出电子变为锂离子。下列结构示意图中能表示锂离子的是___________(填序号)。
A、 B、
B、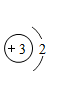 (2)、铅酸电池两极的主要成分为二氧化铅(PbO2)和铅(Pb)。
(2)、铅酸电池两极的主要成分为二氧化铅(PbO2)和铅(Pb)。①配平放电反应的化学方程式:。
②硫酸铅中硫原子与氧原子的个数比为。
四、综合题
-
29. 空气制水机能充分利用大气中的水分制出饮用水,其工作原理如下:
 (1)、①中可阻挡直径(填“大于”或“小于”)滤孔直径的物质。(2)、③中常用活性炭除去异味,活性炭的作用是。30. 氨气(NH3)在化工、科研等领域用途广泛,一种合成氨的主要流程如下图。
(1)、①中可阻挡直径(填“大于”或“小于”)滤孔直径的物质。(2)、③中常用活性炭除去异味,活性炭的作用是。30. 氨气(NH3)在化工、科研等领域用途广泛,一种合成氨的主要流程如下图。
资料:Ⅲ中反应的化学方程式为
(1)、Ⅱ中发生化合反应的化学方程式为。(2)、该流程的优势有___________(填序号)。A、N2可从空气中获得 B、MgCl2可循环使用 C、不需要任何能源31. 近年来,研究人员提出利用含硫物质的化学变化实现能量的存储与转化,同时生产纯净硫酸。主要生产流程如下图。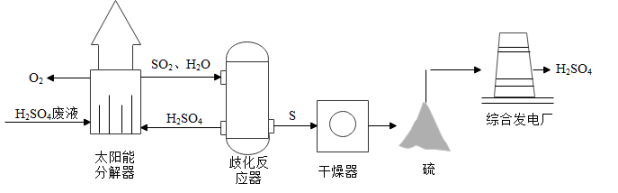 (1)、歧化反应器中发生反应的化学方程式: , 其中化合价变化的元素是。(2)、硫在综合发电厂燃烧时需要通入足量空气的目的是。(3)、该流程实现了能量的转化:太阳能→化学能→热能→。32. 阅读下面科普短文。
(1)、歧化反应器中发生反应的化学方程式: , 其中化合价变化的元素是。(2)、硫在综合发电厂燃烧时需要通入足量空气的目的是。(3)、该流程实现了能量的转化:太阳能→化学能→热能→。32. 阅读下面科普短文。中国是“茶之国”,喝茶已有四千多年的历史。茶叶中含有多种生物碱,咖啡因(C8H10N4O2)是其中之一,咖啡因具有刺激心脏、促进血液循环及兴奋大脑等作用。
从茶叶中提取咖啡因的过程,如图1。
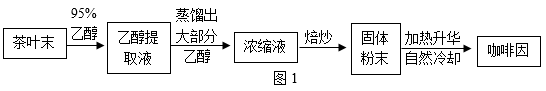
咖啡因能溶于水,可使用分光光度法比较不同茶叶水提物中咖啡因的含量,结果如表1.吸光度值越高,咖啡因含量越高。
表1四种茶叶咖啡因吸光度值
茶叶品种
铁观音
滇红茶
白毫银针
龙井
吸光度值
0.076
0.103
0.123
0.047
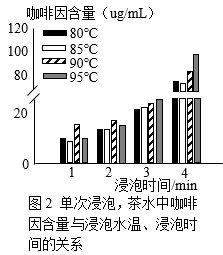
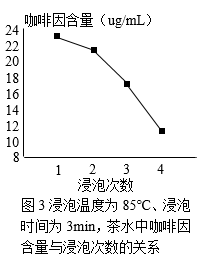
实验人员使用信阳毛尖、控制茶叶与水的质量比为1:75进行其他研究,结果如图2、3。
咖啡因摄入过多容易刺激胃肠道,引起骨质疏松等,生活中应将其摄入量控制在合理范围内。
依据文章内容回答下列问题。
(1)、喝茶能提神的原因是。(2)、图1中,获得浓缩液的过程发生的是(填“物理”或“化学”)变化。(3)、由表1可知,咖啡因含量最低的茶叶是。(4)、判断下列说法是否正确(填“对”或“错”)。①由图2可知,单次浸泡、浸泡时间相同时,温度在80~95℃范围内,浸泡温度越高,茶水中咖啡因含量越高。
②咖啡因摄入过多对人体有害。
(5)、由图3得出的结论是:使用信阳毛尖、、、浸泡3min,浸泡次数4次内,随浸泡次数增加,茶水中咖啡因含量降低。33. 根据下图回答问题。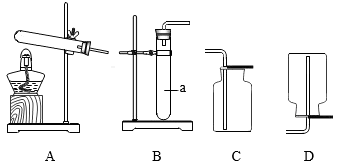 (1)、仪器a的名称是。(2)、实验室用高锰酸钾制取氧气的化学方程式为。(3)、实验室制取二氧化碳的化学方程式为 , 选用的发生和收集装置分别是。检验二氧化碳已收集满的操作是。34. 将充满两种气体的集气瓶如下图放置。抽出玻璃片,静置一段时间,继续实验。
(1)、仪器a的名称是。(2)、实验室用高锰酸钾制取氧气的化学方程式为。(3)、实验室制取二氧化碳的化学方程式为 , 选用的发生和收集装置分别是。检验二氧化碳已收集满的操作是。34. 将充满两种气体的集气瓶如下图放置。抽出玻璃片,静置一段时间,继续实验。 (1)、取下集气瓶2,正放于桌面,滴加澄清石灰水,振荡,石灰水变浑浊。反应的化学方程式为。(2)、向集气瓶1中伸入燃着的木条,证明1中含有氧气的实验现象是。(3)、该实验说明分子具有的性质是。35. 用下图装置进行实验。
(1)、取下集气瓶2,正放于桌面,滴加澄清石灰水,振荡,石灰水变浑浊。反应的化学方程式为。(2)、向集气瓶1中伸入燃着的木条,证明1中含有氧气的实验现象是。(3)、该实验说明分子具有的性质是。35. 用下图装置进行实验。 (1)、实验1,缓慢倒入二氧化碳,观察到燃着的蜡烛由下至上依次熄灭。从灭火原理的角度分析,蜡烛熄灭的原因是;此实验能验证二氧化碳的性质是。(2)、实验2,能证明二氧化碳和水发生反应的现象是 , 反应的化学方程式为。36. 用下图实验探究物质的组成。
(1)、实验1,缓慢倒入二氧化碳,观察到燃着的蜡烛由下至上依次熄灭。从灭火原理的角度分析,蜡烛熄灭的原因是;此实验能验证二氧化碳的性质是。(2)、实验2,能证明二氧化碳和水发生反应的现象是 , 反应的化学方程式为。36. 用下图实验探究物质的组成。 (1)、实验1:
(1)、实验1:①一段时间后关闭电源,负极与正极产生的气体体积比约为。结合其他实验,可得出水是由组成。
②补全该反应的微观示意图。
 (2)、实验2:
(2)、实验2:①红磷燃烧的化学方程式为。
②能证明空气是混合物的现象是。
37. 用如图装置进行两组实验。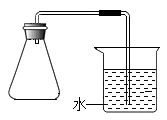 (1)、连接装置。检验装置气密性的操作是。(2)、按下表加入物质,塞紧胶塞,观察现象。
(1)、连接装置。检验装置气密性的操作是。(2)、按下表加入物质,塞紧胶塞,观察现象。实验序号
锥形瓶中的物质
向锥形瓶中加入的物质
1
红棕色NO2气体
活性炭
2
生石灰
水
①实验1,一段时间后,观察到的实验现象:瓶中颜色变浅,。
②实验2,瓶中反应的化学方程式为。观察到烧杯中导管口有气泡冒出,一段时间后,导管内液面上升。“烧杯中导管口有气泡冒出”的原因是。
38. 用下图实验验证可燃物燃烧的条件。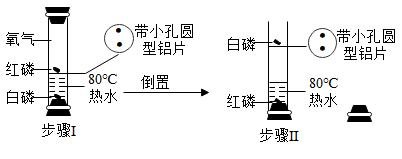
资料:白磷和红磷的着火点分别为40℃、240℃。
(1)、步骤I中,热水的作用是提供热量和。(2)、步骤Ⅱ中,实验现象是。(3)、该实验说明可燃物的燃烧条件有。39. 用下图实验研究质量守恒定律。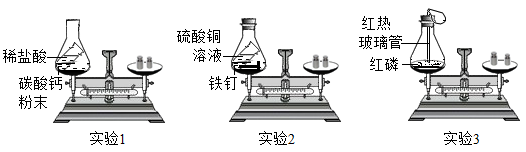 (1)、实验1,反应后天平指针(填“偏左”、“偏右”或“不偏转”)。(2)、实验2,能证明化学反应发生的现象是。(3)、下列说法正确的是___________(填序号)。A、实验3中观察到气球先变鼓后变瘪 B、实验1生成的CO2中的氧元素与参加反应的CaCO3中氧元素的质量相等 C、三组实验的称量结果均可用质量守恒定律解释40. 实验室常用过氧化氢溶液制取氧气。实验小组同学对该反应进行探究。(1)、实验1:验证MnO2是H2O2分解的催化剂。
(1)、实验1,反应后天平指针(填“偏左”、“偏右”或“不偏转”)。(2)、实验2,能证明化学反应发生的现象是。(3)、下列说法正确的是___________(填序号)。A、实验3中观察到气球先变鼓后变瘪 B、实验1生成的CO2中的氧元素与参加反应的CaCO3中氧元素的质量相等 C、三组实验的称量结果均可用质量守恒定律解释40. 实验室常用过氧化氢溶液制取氧气。实验小组同学对该反应进行探究。(1)、实验1:验证MnO2是H2O2分解的催化剂。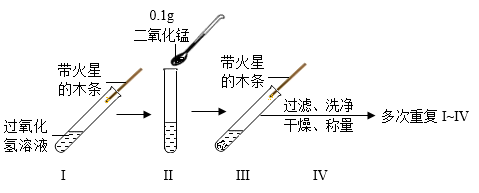
H2O2分解的化学方程式为。
(2)、IV中过滤需要的玻璃仪器有烧杯、玻璃棒和;称得的固体质量为g。(3)、证明MnO2能加快H2O2分解速率的实验现象是。(4)、实验2:探究催化剂种类和质量对H2O2分解的催化效果的影响。【进行实验】
称取催化剂置于三颈瓶中,塞紧胶塞,用注射器将3mL5%过氧化氢溶液快速注入。测定氧气浓度达到最高值时所用的时间,实验记录如下:

序号
初始温度/℃
催化剂种类
催化剂质量/g
氧气浓度达到最高值时所用时间/s
①
30
MnO2
0.03
8
②
30
FeCl3
0.03
32
③
30
FeCl3
0.04
29
④
30
FeCl3
0.05
28
⑤
30
CuCl2
0.03
3364
⑥
30
CuCl2
0.04
837
⑦
30
CuCl2
0.05
464
注:①氧气浓度达到最高值时H2O2已完全分解。
②在可控范围内,过氧化氢分解速率越快,催化效果越好。
【解释与结论】
实验2中,效果最好的催化剂是。
(5)、实验⑤⑥⑦的目的是。(6)、与实验③⑥目的相同的实验组还有(写全对比组)。(7)、【反思与评价】继续实验,发现活性炭比MnO2的催化效果差。其实验方案:称取0.03g活性炭置于三颈瓶中,塞紧胶塞,用注射器将3mL5%过氧化氢溶液快速注入。在初始温度30℃时测定,测定结果是。
五、计算题
-
41. 处理火力发电厂烟气中二氧化氮的反应为。若吸收46kgNO2 , 计算生成N2的质量(写出计算过程及结果)。