北京市怀柔区2022-2023学年高一上学期期末考试化学试题
试卷更新日期:2023-02-06 类型:期末考试
一、单选题
-
1. 2022年3月神舟十三号航天员在中国空间站进行了“天宫课堂”授课活动,其中太空“冰雪实验”演示了过饱和醋酸钠溶液的结晶现象。醋酸钠()属于A、单质 B、酸 C、盐 D、碱2. 当光束通过下列分散系时,能观察到丁达尔效应的是( )A、溶液 B、溶液 C、胶体 D、溶液3. 下列属于电解质的是A、Zn B、NaOH C、NaCl溶液 D、稀4. 下列气体难溶于水的是A、SO2 B、HCl C、NH3 D、CO5. 下列物质中,S元素的化合价最高的是A、 B、 C、 D、6. 下列不属于浓硫酸性质的是A、挥发性 B、吸水性 C、脱水性 D、强氧化性7. 粗食盐提纯的实验操作中,不需要用到的实验仪器为A、
 B、
B、 C、
C、 D、
D、 8. 反应中,还原剂是A、CuO B、Cu C、 D、9. 实验室中,下列行为不符合安全要求的是A、在通风橱内制备有毒气体 B、观察Na与反应的现象时要佩戴护目镜 C、把过期的化学药品溶水倒入下水道 D、闻气体时用手轻轻扇动,使少量气体飘进鼻孔10. 中国茶道既是饮茶的艺术,也是生活的艺术。下列泡茶的主要步骤中,属于过滤操作的是( )
8. 反应中,还原剂是A、CuO B、Cu C、 D、9. 实验室中,下列行为不符合安全要求的是A、在通风橱内制备有毒气体 B、观察Na与反应的现象时要佩戴护目镜 C、把过期的化学药品溶水倒入下水道 D、闻气体时用手轻轻扇动,使少量气体飘进鼻孔10. 中国茶道既是饮茶的艺术,也是生活的艺术。下列泡茶的主要步骤中,属于过滤操作的是( )A.投茶
B.冲泡
C.滤茶
D.分茶



 A、A B、B C、C D、D11. 科学家发现一种化学式为H3的氢分子,则1molH3和1molH2具有相同的( )A、分子数 B、原子数 C、质子数 D、电子数12. 下列说法正确的是A、的分子数为 B、标准状况下:乙醇体积约为 C、氧气的质量为 D、中含有的氢原子数目为13. 抗疫居家期间,同学们在参与家务劳动的过程中体会到化学知识无处不在。下列劳动与所涉及的化学知识不相符的是
A、A B、B C、C D、D11. 科学家发现一种化学式为H3的氢分子,则1molH3和1molH2具有相同的( )A、分子数 B、原子数 C、质子数 D、电子数12. 下列说法正确的是A、的分子数为 B、标准状况下:乙醇体积约为 C、氧气的质量为 D、中含有的氢原子数目为13. 抗疫居家期间,同学们在参与家务劳动的过程中体会到化学知识无处不在。下列劳动与所涉及的化学知识不相符的是选项
家务劳动
化学知识
A
用白醋除去水壶中的水垢
白醋可溶解沉淀
B
用小苏打粉作膨松剂焙制糕点
加热容易分解放出
C
用含NaClO的84消毒液拖地
NaClO有还原性
D
用洁厕灵洗马桶
洁厕灵中含有盐酸,可以与尿垢反应
A、A B、B C、C D、D14. 下列说法错误的是A、为红棕色粉末 B、碳酸钠俗称纯碱 C、为黄绿色气体 D、为红棕色气体15. 下列关于氨的性质的描述错误的是A、无色有刺激性气味的气体 B、能使湿润的红石蕊试纸变蓝 C、难溶于水,密度比空气的小 D、能与氧气在催化剂条件下被氧化成NO16. 下列各组离子在水溶液中不能大量共存的是A、 B、 C、 D、17. 下列离子方程式书写正确的是A、通入水中: B、溶液中滴加盐酸: C、钠加入水中: D、碳酸钙与盐酸反应:18. 下列有关实验装置(如图)进行的相应实验,不能达到实验目的的是A
B
C
D




用上图装置完成喷泉实验
实验室制氨气
比较碳酸钠和碳酸氢钠的热稳定性
检验浓硫酸与铜反应产生的二氧化硫
A、A B、B C、C D、D19. 研究氮及其化合物的性质,可以有效改善人类的生存环境。氮元素化合价-物质类别关系如图,以下说法正确的是 A、物质A转化为NO发生氧化还原反应 B、标准状况下,3.36 L物质B与水完全反应,电子转移0.3 mol C、物质C的浓溶液与Cu反应的离子方程式为 D、的检验方法是取少量溶液于试管中,加热,生成气体能使湿润的红色石蕊试纸变蓝20. 下列关于硫酸和硝酸的叙述错误的是A、稀硫酸和稀硝酸都具有氧化性 B、浓硫酸可以氧化 C、浓硝酸可以氧化金属铜 D、浓硫酸和浓硝酸都具有很强的腐蚀性21. 某儿童检验报告单的部分数据如表所示
A、物质A转化为NO发生氧化还原反应 B、标准状况下,3.36 L物质B与水完全反应,电子转移0.3 mol C、物质C的浓溶液与Cu反应的离子方程式为 D、的检验方法是取少量溶液于试管中,加热,生成气体能使湿润的红色石蕊试纸变蓝20. 下列关于硫酸和硝酸的叙述错误的是A、稀硫酸和稀硝酸都具有氧化性 B、浓硫酸可以氧化 C、浓硝酸可以氧化金属铜 D、浓硫酸和浓硝酸都具有很强的腐蚀性21. 某儿童检验报告单的部分数据如表所示××医院检验报告单
名称
检测结果
单位
参考值(儿童)
锌()
115.92
73~180
铁()
36.95↓
40~160
钙()
1.48
1.1~1.6
…
下列叙述错误的是
A、报告单中“”、“”均是物质的量浓度的单位 B、该儿童易患铁缺乏症 C、服用维生素C可使食物中的在人体内转化为 , 体现了维生素C的还原性 D、检验某补铁口服液中铁元素的价态,可向口服液中先加少量氯水,再加过量硫氰酸钾溶液22. 甲、乙两个装置中(如图),胶头滴管分别吸有某液体,平底烧瓶中置有其他物质,挤压胶头滴管加入液体,一段时间后两装置中的气球都明显胀大(忽略液体体积对气球的影响)。所用试剂分别是 A、甲:浓硫酸和木炭 乙:浓氨水和 B、甲:双氧水和 乙:NaOH溶液和 C、甲:NaOH溶液和 乙:NaOH溶液和 D、甲:浓硫酸和铁屑 乙:水和氨气23. 氢能是一种极具发展潜力的清洁能源。以太阳能为热源,热化学硫碘循环分解水是一种高效、无污染的制氢方法。其反应过程如下图:
A、甲:浓硫酸和木炭 乙:浓氨水和 B、甲:双氧水和 乙:NaOH溶液和 C、甲:NaOH溶液和 乙:NaOH溶液和 D、甲:浓硫酸和铁屑 乙:水和氨气23. 氢能是一种极具发展潜力的清洁能源。以太阳能为热源,热化学硫碘循环分解水是一种高效、无污染的制氢方法。其反应过程如下图:
下列说法错误的是
A、反应I属于氧化还原反应 B、反应II为2H2SO42SO2↑+O2↑+2H2O C、该方法的最终产物只有H2 D、反应II中的SO2、反应III中的I2均可循环利用24. 下列有关实验现象与物质性质对应关系的说法中,正确的是A、溶液遇酚酞变红,说明溶液呈碱性 B、使湿润的有色布条褪色,说明具有漂白性 C、向溶液中滴加氯水,溶液颜色变成棕黄色,说明有氧化性 D、通入碘水中,碘水褪色说明具有漂白性25. 研究金属钠的性质,实验如下:实验装置
实验方案
液体a
现象

蒸馏水
I.钠浮在水面,剧烈反应,有少量白雾
0.1 mol·L-1盐酸
II.钠浮在液面,反应比Ⅰ剧烈,有白雾产生
浓盐酸
III.钠浮在液面,反应比Ⅰ缓慢,产生大量白雾,烧杯底部有白色固体
下列说法错误的是
A、II中反应的离子方程式为2Na + 2H+ = 2Na+ + H2↑ B、对比I、II、III可知,随着c(H+) 增大,反应的剧烈程度增大 C、实验I、II、III均有白雾产生,说明Na与水或酸反应均放出大量热 D、推测III中浓盐酸的c(Cl-)以及生成的NaCl固体对反应剧烈程度有影响二、填空题
-
26. 钛被誉为“21世纪金属”,工业冶炼钛的第一步反应为(1)、该反应中氧化剂是 , 氧化产物是(2)、生成1 mol CO需要的的质量为g,转移电子的物质的量为mol27. 中学化学中常见的几种物质:①氢氧化钡固体②铁丝③氯化氢气体④二氧化碳⑤碳酸钠固体⑥熔融氯化钠,用上述序号填空:(1)、上述状态下可导电的 , 不属于电解质的是(2)、属于碱的是 , 属于盐的是(3)、写出①在水溶液中的电离方程式:(4)、按要求书写下列反应的离子方程式:
②加入③的溶液中
⑤的溶液与③的溶液混合
28. 某工厂的废水中含有大量的、较多的和少量的。为了减少污染并变废为宝,某实验小组设计了如下流程制备绿矾()并回收金属铜。已知加入试剂②时,固体H部分溶解同时有气体生成。 (1)、操作I和II的名称为(2)、加入试剂①的作用是为了除去 , 写出加入试剂①的离子方程式(3)、固体H的成分(4)、试剂②为____(填标号)A、稀硫酸 B、稀盐酸 C、硫酸亚铁溶液29. A,B,C,D是钠及其重要化合物,有着非常广泛的用途,已知B是常见的供氧剂。其相互转化关系如图所示(部分条件省略),回答下列问题:
(1)、操作I和II的名称为(2)、加入试剂①的作用是为了除去 , 写出加入试剂①的离子方程式(3)、固体H的成分(4)、试剂②为____(填标号)A、稀硫酸 B、稀盐酸 C、硫酸亚铁溶液29. A,B,C,D是钠及其重要化合物,有着非常广泛的用途,已知B是常见的供氧剂。其相互转化关系如图所示(部分条件省略),回答下列问题: (1)、已知B为淡黄色粉末,则B为(2)、写出B→C的化学方程式:(3)、写出D→C的化学方程式:(4)、若A为金属钠,46 g A完全转化成D(涉及的其它反应物均足量),生成D的质量为g。30. 从物质类别和元素化合价两个维度研究物质的性质及转化是重要的化学学习方法。氯及其化合物的“价一类”二维图的部分信息如图:
(1)、已知B为淡黄色粉末,则B为(2)、写出B→C的化学方程式:(3)、写出D→C的化学方程式:(4)、若A为金属钠,46 g A完全转化成D(涉及的其它反应物均足量),生成D的质量为g。30. 从物质类别和元素化合价两个维度研究物质的性质及转化是重要的化学学习方法。氯及其化合物的“价一类”二维图的部分信息如图: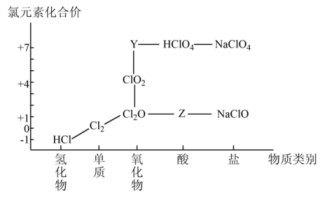
回答下列问题:
(1)、据图中信息,写出Y、Z的化学式:、。(2)、已知高氯酸()是强酸,写出高氯酸溶液与氢氧化钠溶液反应的离子方程式:。(3)、氯气既有氧化性又有还原性,结合上图说明理由:。(4)、二氧化氯()为新时代绿色消毒剂,制备原理为:①按照物质类别对上述反应中的各物质进行分类,未涉及的物质类别是(填序号)。
A.金属氧化物 B.非金属氧化物 C.酸 D.盐
②发生还原反应的产物是(写化学式);该反应(填“能”或“不能”)用稀硫酸代替盐酸。
31. 实验室需用500 mL 0.1 mol/L NaOH溶液,现用NaOH固体配制该溶液。请回答下列问题:(1)、配制时需要使用的玻璃仪器有烧杯、玻璃棒、量筒、胶头滴管、。(2)、用托盘天平准确称取g NaOH固体。(3)、配制溶液时,有以下操作步骤:①将容量瓶盖紧,振荡摇匀
②用托盘天平准确称量所需的NaOH,放入烧杯中,再加入适量水,用玻璃棒慢慢搅拌,使其溶解
③用适量水洗涤烧杯和玻璃棒2~3次,洗涤液均注入容量瓶中并摇匀
④改用胶头滴管加水,使溶液凹液面恰好与刻度线相切
⑤将已冷却的溶液沿玻璃棒注入容量瓶中
⑥继续往容量瓶内小心加水,直到液面接近刻度线1~2cm处
这些操作步骤的正确顺序为____(填序号)
A、②⑤③⑥④① B、②⑤③④⑥① C、②⑤③①⑥④(4)、定容时的操作正确,将容量瓶的玻璃塞盖紧,颠倒摇匀后发现溶液的液面稍低于刻度线,其原因可能是;取出10 mL该NaOH溶液稀释至20 mL,稀释后的NaOH溶液的物质的量浓度为mol/L。(5)、下列操作会造成所配溶液的浓度偏高的是(填序号)。①定容时俯视刻度线
②称量固体时所用的砝码生锈
③溶解NaOH的烧杯未洗涤
④溶解时有溶液溅出烧杯