北京市大兴区2022-2023学年高一上学期期末考试化学试题
试卷更新日期:2023-02-06 类型:期末考试
一、单选题
-
1. 中国空间站“天宫课堂”第二次太空授课:“太空教师”往蓝色水球里塞入半片泡腾片,做成蓝色太空欢乐球。水球中产生的大量小气泡并没有离开水球,而是一直附着在泡腾片放入蓝色水球做成的太空欢乐球容器内部。属于
 A、单质 B、化合物 C、酸 D、碱2. 当光束通过下列分散系时,可以观察到丁达尔效应的是A、胶体 B、溶液 C、NaOH溶液 D、溶液3. 下列物质中,属于电解质的是A、铜 B、NaOH溶液 C、蔗糖 D、氯化钠4. 下列各组中的离子,能在溶液中大量共存的是A、、、、 B、、、、 C、、、、 D、、、、5. 下列物质中,含有离子键的是A、 B、 C、 D、6. 下列物质不能由相应单质通过化合反应生成的是A、 B、 C、 D、7. 下列转化中,需要加入氧化剂才能实现的是( )A、 B、 C、 D、8. 114号元素为Fl(中文名“鈇”),它是主族元素,其原子核外最外层电子数是4。下列说法错误的是A、Fl的原子核内有114个质子 B、Fl是第七周期第VIA族元素 C、Fl在同主族元素中金属性最强 D、Fl的原子半径大于同主族其他元素9. 下列分子结构模型中,不能正确表示分子的空间结构的是
A、单质 B、化合物 C、酸 D、碱2. 当光束通过下列分散系时,可以观察到丁达尔效应的是A、胶体 B、溶液 C、NaOH溶液 D、溶液3. 下列物质中,属于电解质的是A、铜 B、NaOH溶液 C、蔗糖 D、氯化钠4. 下列各组中的离子,能在溶液中大量共存的是A、、、、 B、、、、 C、、、、 D、、、、5. 下列物质中,含有离子键的是A、 B、 C、 D、6. 下列物质不能由相应单质通过化合反应生成的是A、 B、 C、 D、7. 下列转化中,需要加入氧化剂才能实现的是( )A、 B、 C、 D、8. 114号元素为Fl(中文名“鈇”),它是主族元素,其原子核外最外层电子数是4。下列说法错误的是A、Fl的原子核内有114个质子 B、Fl是第七周期第VIA族元素 C、Fl在同主族元素中金属性最强 D、Fl的原子半径大于同主族其他元素9. 下列分子结构模型中,不能正确表示分子的空间结构的是A
B
C
D
HCl



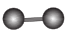 A、A B、B C、C D、D10. 下列说法中,错误的是A、的摩尔质量是 B、所占体积一定是 C、中含有的分子数约为 D、溶液中含的物质的量为11. 下列对图示的解释错误的是
A、A B、B C、C D、D10. 下列说法中,错误的是A、的摩尔质量是 B、所占体积一定是 C、中含有的分子数约为 D、溶液中含的物质的量为11. 下列对图示的解释错误的是A
B
C
D
向溶液中加入稀硫酸,溶液导电能力变化

NaCl的形成

光照过程中氯水的pH变化

NaCl溶于水

a时刻溶液与稀硫酸恰好完全中和

pH降低的原因可能是HClO分解
A、A B、B C、C D、D12. 下列用来解释事实的化学用语中,不合理的是A、用溶液“腐蚀”覆铜电路板: B、用在呼吸面具中与反应: C、小苏打溶液加入氢氧化钠: D、硝酸酸化的溶液检验溶液中的13. 工业制备锰(Mn)单质的过程中会产生高浓度SO2。酸性条件下,用MnO2进行脱硫处理的原理如下图所示。
下列说法中,错误的是
A、反应1中,锰元素化合价升高 B、反应2属于氧化还原反应 C、脱硫的最终产物为MnSO4 D、上述过程中Fe2+、Fe3+可以循环使用14. X、Y、Z、a为中学化学常见物质,且X、Y、Z含有一种或两种、三种相同元素,可以发生如下转化关系(水参与的反应,水未标出,反应条件未标出)。
下列说法错误的是
A、若为碳酸钠溶液、a为盐酸,则Z为氯化钠溶液 B、若是氯化铁溶液,则反应的离子方程式为 C、若为参与植物光合作用的气体,则为碳单质,a是氧气 D、若X、Y、Z的焰色试验呈黄色,a为 , 则Z的化学式为二、填空题
-
15. 回答下列问题(1)、补齐物质与其用途之间的连线。
物质 用途
A.氧化铁 a.作红色颜料
B.次氯酸钠 b.作食用碱
C.碳酸钠 c.漂白剂
(2)、为治理汽车尾气中的NO和CO对环境的污染,可在汽车排气管上安装催化转化催化剂器,发生如下反应:①该反应中作还原剂的物质是。
②若反应中消耗了0.2mol则生成的物质的量为mol,转移电子的物质的量为mol。
(3)、小组同学用NaCl固体配制100mL1.00mol/LNaCl溶液。根据下表有关溶液配制的实验步骤和仪器,回答下列①~④问题。实验步骤
实验仪器
a.将称量好的NaCl固体放入烧杯中,加入适量蒸馏水,用玻璃棒搅拌,使NaCl固体全部溶解。
b.根据计算结果,称量NaCl固体。
c.计算需要的NaCl固体的质量
d.将烧杯中的溶液沿玻璃棒注入100mL容量瓶,并用少量蒸馏水洗涤烧杯内壁和玻璃棒2~3次,将洗涤液也都注入容量瓶。轻轻摇动容量瓶,使溶液混合均匀。
e.将配制好的溶液倒入试剂瓶中,并贴好标签。
f.将蒸馏水注入容量瓶,当液面离容量瓶颈部的刻度线1~2cm时,改用胶头滴管滴加蒸馏水,至溶液的凹液面与刻度线相切。盖好瓶塞,反复上下颠倒,摇匀。
量筒
托盘天平
圆底烧瓶
100mL容量瓶
烧杯
玻璃棒
胶头滴管
①计算需要NaCl固体的质量为g。
②配制过程中不需要使用的仪器是。
③配制溶液时,正确的实验操作顺序是c-b。
④定容时俯视容量瓶刻度线,会导致所配制的NaCl溶液浓度。(填“偏大”或“偏小”)
三、综合题
-
16. 某小组同学用下图1装置制取氯气并探究其性质(夹持装置和加热仪器略)。

请回答:
(1)、装置A中制取氯气的化学方程式是 , 反应中利用了的(填字母)。a.氧化性 b.还原性
若生成的物质的量是0.2mol,该气体在标准状况下的体积为L。
(2)、装置C中的现象是。(3)、装置D的作用是。(4)、氯气溶解在石灰乳中可以制漂白粉,发生反应的化学方程式为。(5)、若将上述图1中B和C分别换成图2中的M和N,则:
①M中发生反应的离子方程式为。
②取一支试管,加入2mLN中变橙黄色的溶液。再滴入几滴淀粉KI溶液,观察到溶液变为蓝色。通过以上实验,能否得出结论:的氧化性强于 , 的。理由。
17. 铁是人体必需的微量元素,铁摄入不足可能引起缺铁性贫血。小组同学利用化学实验进行菠菜中铁元素的检验和铁元素含量测定。(1)、实验1.菠菜中铁元素的检验
操作1的名称是。
(2)、溶液②为浅红色,说明溶液①中含有(填离子符号)。(3)、溶液③中 (填实验现象),证明溶液②中还含有 , 其推理过程是。(4)、实验2.测定菠菜中铁元素的含量i.沉淀法:向实验1滤液①中加入足量NaOH溶液,过滤、洗涤沉淀、加热烘干、称量。
滤液①中加入足量NaOH溶液后生成的沉淀有、;在沉淀生成或后续处理过程中,沉淀转化发生的氧化还原反应为。
(5)、ii.比色法:利用色度传感器测定其对光的透过率或者吸收率,颜色越深,吸收率越高。测得不同浓度的标准液吸收率如下图。

菠菜处理后得到溶液(3) , 色度传感器测得吸收率为上图中a点,则 , 菠菜中含铁=g。
18. 某实验小组欲通过加热蒸发硝酸钾溶液的方法获得固体。已知固体在一定温度下能发生反应:。为了探究加热蒸发所得固体中是否含有亚硝酸钾 , 小组同学设计并完成了以下实验。【查阅资料】
i.是微溶于水的白色(略带黄色)固体
ii.、能在酸性条件下与KI反应,生成
【实验过程】
 (1)、【分析解释】
(1)、【分析解释】在反应中,和属于(填“酸”或“碱”或“盐”)。
(2)、的原子结构示意图为。中的化合价是 , 从化合价的角度预测,具有的性质是(填“氧化性”或“还原性”或“既有氧化性,又有还原性”)。(3)、试管①中,观察到有少量白色沉淀生成,该白色沉淀是。(4)、试管②中,观察到的现象是;KI发生反应(填“氧化”或“还原”)。(5)、试管③中,观察到新制氯水褪色,利用对比实验排除了稀释对溶液颜色变化的影响。补齐该反应的离子方程式。□_++□_。
(6)、【反思评价】综合上述实验,甲同学得出以下结论。你认为甲同学所得结论正确的是。
a.从试管②中的现象可得出酸性条件下,氧化性:
b.试管①、③中的实验现象均可以证明固体X中含有
(7)、通过该探究实验,对于从溶液中获得固体,你有哪些收获或建议(写一条即可)。19. 1869年,俄国化学家门捷列夫制出的第一张元素周期表,成为化学发展史上重要的里程碑之一。下图代表元素周期表的一部分,①~④表示元素在周期表中的位置,回答下列问题。 (1)、将硅的元素符号填写在上述周期表相应的空格中。(2)、①、②、④三种元素形成的化合物的化学式为。(3)、用电子式表示①和③形成化合物的过程。(4)、硫的最高价氧化物对应的水化物与氢氧化钠溶液反应的离子方程式为。(5)、根据元素在周期表中的位置,下列各组性质比较正确的是。
(1)、将硅的元素符号填写在上述周期表相应的空格中。(2)、①、②、④三种元素形成的化合物的化学式为。(3)、用电子式表示①和③形成化合物的过程。(4)、硫的最高价氧化物对应的水化物与氢氧化钠溶液反应的离子方程式为。(5)、根据元素在周期表中的位置,下列各组性质比较正确的是。a.酸性: b.非金属性:
c.碱性: d.热稳定性:
(6)、亚硒酸钠()具有消除活性氧,抗人体衰老的作用。亚硒酸钠中硒(Se)元素的原子结构示意 。
。i.下列关于硒的说法正确是。
a.硒元素在元素周期表中位于第四周期第VA族
b.Se的气态氢化物的化学式为
c.Se的一种核素的中子数为46,这种核素是
ii.非金属性S>Se,从原子结构角度解释其原因。
-