北京市朝阳区2022-2023学年高二上学期期末考试化学试题
试卷更新日期:2023-02-06 类型:期末考试
一、单选题
-
1. 下列仪器中,不属于酸碱中和滴定中常用仪器的是




A.分液漏斗
B.酸式滴定管
C.碱式滴定管
D.锥形瓶
A、A B、B C、C D、D2. 下列基态原子的最外层电子排布式表示的元素,不一定属于主族元素的是A、 B、 C、 D、3. 基元反应的反应过程如下图。下列分析错误的是 A、该基元反应涉及键断裂和键形成 B、该基元反应属于吸热反应 C、使用催化剂,可以改变该反应 D、增大 , 该反应单位体积内活化分子数增多4. 下列用于解释事实的方程式书写错误的是A、向溶液中滴入酚酞溶液,溶液变红: B、在气流中加热得到无水 C、向亚硫酸溶液中滴入紫色石蕊溶液,溶液变红:、 D、用KI溶液将转化为5. 化学小组研究金属的电化学腐蚀,实验如下:
A、该基元反应涉及键断裂和键形成 B、该基元反应属于吸热反应 C、使用催化剂,可以改变该反应 D、增大 , 该反应单位体积内活化分子数增多4. 下列用于解释事实的方程式书写错误的是A、向溶液中滴入酚酞溶液,溶液变红: B、在气流中加热得到无水 C、向亚硫酸溶液中滴入紫色石蕊溶液,溶液变红:、 D、用KI溶液将转化为5. 化学小组研究金属的电化学腐蚀,实验如下:序号
实验Ⅰ
实验Ⅱ
实验


现象
铁钉周边出现____色
锌片周边未见明显变化
铁钉周边出现蓝色
铜片周边略显红色
下列说法错误的是
A、实验Ⅰ中铁钉周边出现红色 B、实验I中负极的电极反应式: C、实验Ⅱ中正极的电极反应式: D、对比实验I、Ⅱ可知,生活中镀锌铁板比镀铜铁板在镀层破损后更耐腐蚀6. 生产钛的方法之一是将金红石()转化为 , 再进一步还原得到钛。转化为有直接氯化法和碳氯化法,相关能量示意图如下所示。下列说法错误的是 A、将反应物固体粉碎可以加快直接氯化,碳氯化的反应速率 B、可推知 C、判断直接氯化反应能否自发进行需要综合考虑体系的焓变和熵变 D、对于碳氯化反应,温度升高,平衡时的产率变小7. 下列所述的粒子(均为36号以前的元素),按原子半径由大到小的顺序排列正确的是( )
A、将反应物固体粉碎可以加快直接氯化,碳氯化的反应速率 B、可推知 C、判断直接氯化反应能否自发进行需要综合考虑体系的焓变和熵变 D、对于碳氯化反应,温度升高,平衡时的产率变小7. 下列所述的粒子(均为36号以前的元素),按原子半径由大到小的顺序排列正确的是( )①基态X原子的结构示意图为

②基态的价电子排布式为
③基态的轨道表示式为
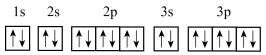
④基态的最高能级的电子对数等于其最高能层的电子层数
A、②>③>① B、④>③>② C、③>②>④ D、④>②>③8. 室温下,用溶液溶液和蒸馏水进行如下表所示的5个实验,分别测量浑浊度随时间的变化。编号
溶液
溶液
蒸馏水
浑浊度随时间变化的曲线

①
1.5
3.5
10
②
2.5
3.5
9
③
3.5
3.5
x
④
3.5
2.5
9
⑤
3.5
1.5
10
下列说法错误的是
A、实验③中 B、实验①②③或③④⑤均可说明其他条件相同时,增大反应物浓度可增大该反应速率 C、降低溶液浓度比降低溶液浓度对该反应化学反应速率影响程度更大 D、。将装有实验②的试剂的试管浸泡在热水中一段时间后再混合,其浑浊度曲线应为a9. 常温下,用0.10mol/LNaOH溶液分别滴定20.00mL浓度均为0.10mol/L的CH3COOH溶液和HCN溶液,所得滴定曲线如图。下列说法错误的是已知:;
 A、曲线M为的滴定曲线 B、点①和点②所示溶液中: C、点③所示溶液中: D、点④所示溶液中:10. 下列实验不能得出相应实验结论的是
A、曲线M为的滴定曲线 B、点①和点②所示溶液中: C、点③所示溶液中: D、点④所示溶液中:10. 下列实验不能得出相应实验结论的是选项
A
B
C
D
实验




结论
该反应的
平衡正向移动
醋酸的大于碳酸的
相同温度下的溶液度:
A、A B、B C、C D、D11. 一定温度下,在两个容积均为的恒容密闭容器中加入一定量的反应物,发生反应 , 相关数据见下表。容器编号
温度/℃
起始物质的量/
平衡物质的量/
Ⅰ
0.4
0.4
0.2
Ⅱ
0.4
0.4
0.24
下列说法错误的是
A、 B、Ⅰ中反应达到平衡时,的转化率为50% C、Ⅱ中反应平衡常数 D、的容器中,若四种气体的物质的量均为 , 则12. 新型双离子可充电电池是一种高效,低成本的储能电池,其装置示意图如下。当闭合K2时,该电池的工作原理为。下列关于该电池的说法正确的是 A、放电时,电子从N电极经导线流向M电极 B、放电时,正极的电极反应式: C、充电时,外加直流电源的正极与M电极相连 D、充电时,电路中每通过 , 左室溶液增加13. 以石灰石矿(主要成分为 , 含少量等)为原料制备高纯轻质碳酸钙的一种工艺流程如下。
A、放电时,电子从N电极经导线流向M电极 B、放电时,正极的电极反应式: C、充电时,外加直流电源的正极与M电极相连 D、充电时,电路中每通过 , 左室溶液增加13. 以石灰石矿(主要成分为 , 含少量等)为原料制备高纯轻质碳酸钙的一种工艺流程如下。
已知:固体B中含有及
下列说法错误的是
A、过程Ⅱ中,溶液浸出而非是因为 B、过程Ⅲ中,反应的离子方程式为 C、过程Ⅱ和过程Ⅲ的操作均应在较高温度下进行 D、整个流程中,“变废为宝、循环利用”的物质是14. 室温下,向新制酸化的和未酸化的的溶液中通入氧气且搅拌时,变化曲线如图。
已知:的;的
开始沉淀时的;开始沉淀时的
下列说法错误的是
A、M点对应的溶液中水解程度小于Р点对应的溶液中水解程度 B、导致M点→N点升高的反应为: C、导致Р点→Q点降低的反应为: D、O点和Q点后变化不大,推测两个反应体系中一定不再发生的氧化反应二、综合题
-
15. 是汽车尾气中的主要污染物,在汽车尾气系统中装配催化转化器,可有效降低的排放。(1)、当尾气中空气不足时,(以为主)在催化转化器中被还原成排出。
①基态碳原子中,电子占据最高能级的电子云轮廓图的形状是。
②氧的基态原子的轨道表示式为。
③C、N、O电负性由大到小顺序为。
(2)、当尾气中空气过量时,催化转化器中的金属氧化物吸收生成盐。其吸收能力顺序如下:。已知:镁、钙、锶、钡的部分电离能数据如下表所示。元素
738
589.7
549
502.9
1451
1145
1064
965.2
7733
4910
a
3600
①推测的第三电离能a的范围:。
②对的吸收能力增强,从原子结构角度解释原因:为同主族元素, , 元素的金属性逐渐增强,金属氧化物对的吸收能力逐渐增强。
(3)、研究作为脱硝催化剂的性能时发现:在上适当掺杂不同的金属氧化物如等有利于提高催化脱硝性能。①基态V原子的核外电子排布式为。
②若继续寻找使催化性能更好的掺杂金属氧化物,可以在元素周期表区寻找恰当元素(填序号)。
A.s B.p C.d D.ds
16. 电解食盐水可以制备烧碱、次氯酸钠消毒液等。(1)、【用途一】制备烧碱离子交换膜法电解饱和食盐水原理示意图如图1。

①气体a的电子式为:。
②结合电极反应式解释阴极区得到溶液的原因。
(2)、【用途二】制备次氯酸钠溶液采用无隔膜电解槽,电解3%~5%的溶液,可制备溶液。控制较低温度,适宜电压电解制备溶液原理示意图如图2。

已知:与次氯酸盐相比,次氯酸具有更强的氧化性。
电解食盐水制备溶液总反应的化学方程式为。
(3)、研究发现,电解制备溶液时,中性溶液为宜,若初始过高()或过低()都会降低的浓度。分析可能原因:①过高,阳极会发生放电,导致电解效率降低,电极反应为。
②过低,产生影响的可能原因:
假设过低时,导致溶解度 , 生成的减少。
假设过低时,浓度增大氧化 , 生成和。
I.查阅文献,假设b成立。相应反应的离子方程式为。
Ⅱ.若通过检测反应前后溶液酸性的变化证实假设b成立,实验操作和现象为:取溶液,。可供选择的试剂和仪器:a.稀硫酸| b.稀盐酸| c.石蕊溶液 d.计
17. 某小组研究和的氧化性,进行如下实验。
已知:是黄色液体,氧化性:。
(1)、实验Ⅰ过程Ⅰ中与反应的化学方程式是。(2)、实验Ⅰ过程Ⅱ中溶液变红,说明产生了 , 分析可能原因。假设①被氧化。过程Ⅱ发生反应的电极反应式:
a.氧化反应:
b.还原反应:。
假设②和生成 , 进而使清液中的氧化为。设计实验Ⅱ证实假设。

i.。
ⅱ.实验Ⅱ中过程Ⅱ的离子方程式为。
(3)、设计实验进一步研究能否氧化。编号
实验Ⅲ
实验Ⅳ
实验及现象


①实验Ⅲ中溶液的作用是。
②实验Ⅳ证实能氧化的实验现象除电流表指针偏转外,还有(答出2点)。
(4)、分析实验Ⅱ中能氧化 , 实验Ⅲ中未能氧化的原因:。18. 用甲烷制高纯氢气是目前研究热点之一。(1)、一定条件下,反应历程如图1所示,其中化学反应速率最慢的反应过程为。 (2)、甲烷水蒸气催化重整可制得较高纯度的氢气,相关反应如下。
(2)、甲烷水蒸气催化重整可制得较高纯度的氢气,相关反应如下。反应I.
反应Ⅱ.
①总反应:
②已知830℃时,反应Ⅱ的平衡常数。在容积不变的密闭容器中,将与加热到830℃,反应达平衡时的转化率为。
③在常压,600℃条件下,甲烷制备氢气的总反应中平衡产率为82%。若加入适量生石灰后的产率可提高到95%,应用化学平衡移动原理解释原因。
(3)、科学家研究将与联合重整制备氢气:反应I:
反应Ⅲ:
常压下,将和按一定比例混合置于密闭容器中,相同时间不同温度下测得体系中变化如图2所示。

①已知700℃、催化剂条件下,向反应体系中加入少量可增加产率,此条件下还原性(填“>”“<”或“=”)。
②随着温度升高变小的原因可能是。
19. 高纯硫酸锰在电池材料等领域具有重要的用途,可用如下方法制备。(1)、酸浸
酸浸过程中的主要反应为(将离子方程式补充完整):。
□□=□□□
(2)、净化含的浸取液中有等杂质离子,一种制备高纯硫酸锰的工艺流程如下。

已知:a.可溶于水
b.部分难溶电解质的溶度积常数(25℃)如下表:
化学式
①加入的目的是:。
②常温下,除铁过程中调节 , 通过计算判断是否沉淀完全并简述理由。(一般认为溶液中离子浓度小于时沉淀完全)
③结合离子方程式说明选用作为沉淀剂的原因:。
(3)、“酸浸渣”中锰元素含量检测i.称取mg酸浸渣,将其中的锰元素全部溶出成 , 过滤,将滤液定容于容量瓶中;
ⅱ.取溶液于锥形瓶中,加入少量催化剂和过量的溶液,加热、充分反应后,煮沸溶液使剩余的分解;(已知:)
ⅲ.加入指示剂,用溶液滴定,至终点时消耗重新变为。
①“酸浸渣”中锰元素的质量分数为。
②ⅱ中若未充分加热煮沸,将会造成锰元素质量分数的测定结果(填“偏大”“偏小”或“不影响”)。