九年级化学2022年寒假复习21预习
试卷更新日期:2023-01-13 类型:复习试卷
一、单选题
-
1. 菜刀用铁制而不用铝制的主要原因是( )。A、铁的硬度大,铝的硬度小 B、铁的熔点高,铝的熔点低 C、铁的密度大,铝的密度小 D、铁的导电性差,铝的导电性好
-
2. 利用铝合金代替铝制钥匙,主要是利用铝合金的( )。A、密度小 B、熔点低 C、不易腐蚀 D、硬度大
-
3. 向AgNO3溶液中加入一定量的Mg粉和Fe粉,充分反应后过滤,得到滤渣和浅绿色的滤液.关于该滤渣和滤液有下列四种说法:
①向滤渣中加入稀盐酸,一定有气泡产生; ②向滤液中加入稀盐酸一定有沉淀产生;
③滤渣中一定有Ag; ④滤液中一定有Fe(NO3)2、一定不含AgNO3、可能有Mg(NO3)2 .
以上说法中正确的个数为( )
A、1个 B、2 个 C、3个 D、4个 -
4. 下列说法不正确的是( )A、单质铁能从硫酸铜溶液中把铜置换出来 B、能使无色酚酞变红的物质,一定是碱溶液 C、碘是人体必需的微量元素,缺碘会引起甲状腺肿大 D、燃烧必须同时满足两个条件:可燃物与氧气接触,可燃物的温度达到着火点
-
5. 为预防自行车生锈,下列做法中不合理的是( )A、车架表面喷涂油漆 B、钢圈表面镀防护金属 C、链条表面涂机油 D、露天放置,日晒雨淋
-
6. 小明发现月饼盒里的脱氧剂部分呈红棕色,查阅资料得知脱氧剂中含有铁粉和活性炭。他猜想这包脱氧剂中可能含有:①Cu和C;②Fe2O3和C;③Fe3O4和C;④Fe3O4、C和Fe;⑤Fe2O3、C和Fe。其中猜想合理的是( )。A、①③⑤ B、②④⑤ C、②⑤ D、④⑤
-
7. 下列图像能正确反映其对应变化关系的是( )A、
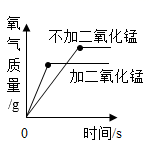 用等质量、等浓度的过氧化氢溶液分别在有、无催化剂的条件下制氧气
B、
用等质量、等浓度的过氧化氢溶液分别在有、无催化剂的条件下制氧气
B、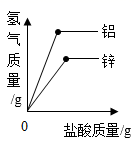 向等质量的铝、锌中分别加入足量的等浓度的稀盐酸
C、
向等质量的铝、锌中分别加入足量的等浓度的稀盐酸
C、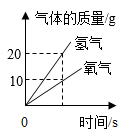 通电电解水
D、
通电电解水
D、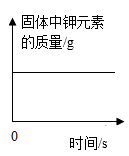 加热一定质量的高锰酸钾
加热一定质量的高锰酸钾
-
8. 有一包金属粉末,可能由Mg、Zn、Fe、Al、Ag 等金属中的一种或几种组成。取该样品4.8g,加入100g 稀硫酸恰好完全反应,只得到0.4gH2和无色溶液,下列说法正确的是( )A、样品中一定只含有Mg B、样品中一定不含有Ag,可能含有Fe C、稀硫酸的溶质质量分数为9.8% D、无色溶液中溶质总质量为24g
-
9. 将一定量铝粉和氧化铜混合加热,反应化学方程式为:3CuO+2Al 3Cu+Al2O3。反应结束后,为了检验氧化铜是否完全反应,取少量反应后的固体,加入足量的稀硫酸,充分反应后,将铁片插入溶液中。下列叙述的现象中,能够说明氧化铜没有完全反应的是( )
①加入稀硫酸后,有气泡生成;
②加入稀硫酸后,没有气泡生成;
③加入稀硫酸后,溶液中有红色不溶物质;
④插入溶液中的铁片表面有红色物质析出。
A、①② B、②④ C、只有④ D、②③④ -
10. 金属和金属材料的性质在很大程度上决定了它们的用途。下列说法错误的是( )。A、不锈钢抗腐蚀性好,常用于制造医疗器械 B、铁具有良好的导热性,可用于制造炊具 C、焊锡的熔点较低、电阻率较大,常用于制成发热体 D、硬铝轻而坚韧,可作为制造汽车、飞机和火箭的材料
-
11. 下列叙述错误的是( )。A、钢筋混凝土是复合材料 B、用肥皂水可以区别硬水和软水 C、生铁和钢都是铁的合金 D、淀粉没有甜味,因此不属于糖类
二、填空题
-
12. 请回答有关金属的问题。(1)、在Cu和Zn中,活动性较强的是;(2)、Cu与AgNO3溶液的反应中,离子变成了原子;(3)、只用少量的盐酸、一支试管和锌、铜、铝,通过加入金属的顺序不同,也能验证这三种金属的活动性的强弱,则加入的顺序为(假设每次的反应均反应完全)。
-
13. 地壳中含量最高的金属元素是;人体中含量最多的金属元素是;熔点最低的金属是;目前世界上年产量最高的金属是。
-
14. 结合常见金属的活动性顺序,回答问题:(1)、在镁与铂(Pt)中,能与稀盐酸发生置换反应的是;(2)、将金属锰放入MgCl2溶液中,锰表面和溶液均无任何变化,说明锰比镁的活动性;(3)、向Cu(NO3)2和NaNO3的混合溶液中加入一定量镁粉,反应停止后过滤,所得滤液中一定含有的溶质是。
-
15. 水与人类的生活和社会发展密切相关,回答下列问题。(1)、日常生活中,常利用的方法降低水的硬度;(2)、生铁和钢性能不同的原因是。
三、简答题
-
16. 金属在生活生产和科学研究方面应用广泛。请根据所学知识回答下列问题:(1)、铝锅轻便、耐用,其原因是;(2)、车轮的钢圈在潮湿的空气中会锈蚀,这是铁与等物质发生化学反应的结果。通常用盐酸除铁锈,该反应的化学方程式为;(3)、灯泡里的灯丝使用金属钨而不用金属锡的原因是。
四、综合题
-
17. 人类社会的发展离不开金属。(1)、黄铜和纯铜,属于合金的是。(2)、铝制品耐腐蚀,是由于其表面生成致密的氧化膜,该反应化学方程式为。(3)、某工厂废液中含有硝酸银、硝酸铜,为回收资源和防止污染,向废水中加一定量铁粉,充分反应后过滤,
①若铁过量,则滤液中,除水外还一定含有的物质是(填写化学式,下同);
②若铁不足,则滤渣中一定含有 , 可能含有。
五、推断题
-
18. 已知A~H均为初中化学常见的物质。其中A、C是组成元素相同的气体,且c能产生温室效应;B为红棕色,是赤铁矿的主要成分;F是紫红色金属;H是蓝色沉淀。根据如图所示的转化关系(图中反应条件均已略去),请回答:
 (1)、写出物质B的化学式:。(2)、写出序号对应的化学方程式:①。②。(3)、反应③的基本反应类型是。
(1)、写出物质B的化学式:。(2)、写出序号对应的化学方程式:①。②。(3)、反应③的基本反应类型是。
六、实验探究题
-
19. 在高温条件下,铁与水蒸气能反应生成一种常见铁的氧化物和一种气体。小莉很好奇,设计如下实验探究铁粉与水蒸气反应后的产物。
 (1)、试管尾部放一团湿棉花的目的是。(2)、探究生成的气体是什么?用燃着的木条靠近飘到空中的肥皂泡,有爆鸣声。说明生成的气体。(3)、探究试管中剩余固体成分是什么?
(1)、试管尾部放一团湿棉花的目的是。(2)、探究生成的气体是什么?用燃着的木条靠近飘到空中的肥皂泡,有爆鸣声。说明生成的气体。(3)、探究试管中剩余固体成分是什么?【查阅资料】
①常见铁的氧化物的物理性质如下表:
常见铁的氧化物
FeO
Fe2O3
Fe3O4
颜色、状态
黑色粉末
红棕色粉末
黑色晶体
能否被磁铁吸引
否
否
能
②稀盐酸(或稀硫酸)与铁反应产生气体,与铁的氧化物反应没有气体产生。
【初步验证】试管中剩余固体为黑色,能全部被磁铁吸引。
【猜想与假设】猜想一:剩余固体是Fe3O4;猜想二:剩余固体是。
(4)、【实验探究】根据猜想与假设,设计实验方案加以检验
实验操作
实验现象
实验结论
剩余固体是Fe3O4
(5)、【实验结论】铁和水蒸气反应的化学方程式为。(6)、【反思与交流】该黑色固体不可能是Fe2O3 , 理由是。
七、计算题
-
20. 要炼出含有2%杂质的铁1600t,需要含氧化铁80%的赤铁矿石多少吨?
