九年级化学2022年寒假复习20预习
试卷更新日期:2023-01-13 类型:复习试卷
一、单选题
-
1. 下列关于金属材料的说法中,不正确的是( )A、汞属于金属材料 B、铜有良好的导电性,因而大量用于制作电线 C、铝表面易生成致密氧化铝薄膜,因而具有良好 的 抗腐蚀性 D、铝、铁、铜都是银白色金属2. 下列与金属材料有关的说法中,正确的是( )A、地壳中含量最高的金属元素是铁 B、2Cu2O+C 4Cu+CO2↑不属于置换反应 C、钢的性能优良,所以钢是纯净物 D、为防止铁制品生锈,可在其表面刷漆3. 下列对古诗词中蕴含的化学知识理解错误的是( )A、“春蚕到死丝方尽”中的蚕丝属于天然材料 B、“金入于猛火,色不夺精光”中金在加热的条件下能与氧气反应 C、“添得醋来风韵美”中的食醋是一种常用的调味品 D、“烈火焚烧若等闲”是指煅烧石灰石,发生了化学变化4. 实验现象或实验原理正确的是( )A、白磷始终不燃烧
 B、小气球变瘪
B、小气球变瘪  C、U型管内液面左低右高
C、U型管内液面左低右高  D、验证Fe、Cu、Ag的金属活动性强弱
D、验证Fe、Cu、Ag的金属活动性强弱  5. 用图1所示装置对暖宝宝(主要成分有铁粉、水、活性炭、食盐等)的发热过程进行探究,传感器获得图2和图3所示的实验数据。下列说法错误的是( )
5. 用图1所示装置对暖宝宝(主要成分有铁粉、水、活性炭、食盐等)的发热过程进行探究,传感器获得图2和图3所示的实验数据。下列说法错误的是( ) A、暖宝宝的发热是一种放热反应 B、由图2可知,足量暖宝宝原料发热过程能消耗掉瓶中全部氧气 C、图3表明,瓶内氧气减少造成的气压变小量与温度升高造成的气压增大量相等 D、装置冷却至室温,图3中的曲线会逐渐降低至06. 铁钉在下列情况下:①在干燥的空气中; ②在潮湿的空气中; ③部分浸在食盐水中; ④浸没在植物油中。容易生锈的是( )A、①④ B、①② C、②③ D、②④7. 下列图像分别与选项中的实验现象及结果相对应,其中正确的是( )A、电解水
A、暖宝宝的发热是一种放热反应 B、由图2可知,足量暖宝宝原料发热过程能消耗掉瓶中全部氧气 C、图3表明,瓶内氧气减少造成的气压变小量与温度升高造成的气压增大量相等 D、装置冷却至室温,图3中的曲线会逐渐降低至06. 铁钉在下列情况下:①在干燥的空气中; ②在潮湿的空气中; ③部分浸在食盐水中; ④浸没在植物油中。容易生锈的是( )A、①④ B、①② C、②③ D、②④7. 下列图像分别与选项中的实验现象及结果相对应,其中正确的是( )A、电解水 B、向等质量的镁粉和铁粉中分别滴加同浓度的稀硫酸至过量
B、向等质量的镁粉和铁粉中分别滴加同浓度的稀硫酸至过量  C、向一定量的二氧化锰中加入过氧化氢溶液
C、向一定量的二氧化锰中加入过氧化氢溶液  D、一定温度时向一定量饱和石灰水中加入氧化钙
D、一定温度时向一定量饱和石灰水中加入氧化钙  8. 类推是学习中常用的思维方法,现在有以下类推结果,其中正确的是( )A、氮肥氯化铵与碱研磨可放出氨气,所以氮肥尿素与碱研磨也能放出氨气 B、金属铝有良好的抗腐蚀性,所以它的化学性质不活泼 C、某物质在氧气中燃烧生成水,所以该物质中一定含有氢元素 D、碱溶液能使紫色石蕊试液变蓝,所以能使石蕊试液变蓝的溶液一定是碱溶液
8. 类推是学习中常用的思维方法,现在有以下类推结果,其中正确的是( )A、氮肥氯化铵与碱研磨可放出氨气,所以氮肥尿素与碱研磨也能放出氨气 B、金属铝有良好的抗腐蚀性,所以它的化学性质不活泼 C、某物质在氧气中燃烧生成水,所以该物质中一定含有氢元素 D、碱溶液能使紫色石蕊试液变蓝,所以能使石蕊试液变蓝的溶液一定是碱溶液二、填空题
-
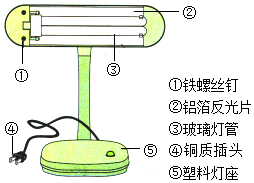
9. 如图台灯中,铜质插头是利用了金属铜的性(填“导电”或“导热”);灯管后面的反光片为铝箔,铝制品耐腐蚀的原因是;制作铁螺丝钉需要利用高炉炼铁,其主要反应原理是一氧化碳与氧化铁的反应,该反应的化学方程式为;制作灯座的塑料属于材料(填“天然”或“合成”)。
 10. 经研究发现,长期使用铁锅炒菜做饭,可有效地防止缺铁性贫血的发生,原因是;如果炒菜时经常加入适量的食醋,效果会更好,理由是。11. 将生锈的铁钉投入到稀盐酸中,刚开始观察到的现象是 , 其反应的化学方程式是;过一段时间后,铁钉可能发生反应的化学方程式是。12. 垃圾分类即将全面铺开,垃圾分类的知识也将纳入中小学教材,旨在帮助学生形成资源综合利用的意识及废旧物资再生利用的观念。
10. 经研究发现,长期使用铁锅炒菜做饭,可有效地防止缺铁性贫血的发生,原因是;如果炒菜时经常加入适量的食醋,效果会更好,理由是。11. 将生锈的铁钉投入到稀盐酸中,刚开始观察到的现象是 , 其反应的化学方程式是;过一段时间后,铁钉可能发生反应的化学方程式是。12. 垃圾分类即将全面铺开,垃圾分类的知识也将纳入中小学教材,旨在帮助学生形成资源综合利用的意识及废旧物资再生利用的观念。 (1)、垃圾箱的板面由塑料制成,塑料属于材料,制作垃圾箱的边框使用了铁的合金,合金与组成它的纯金属比,一般具有的一条优良的物理性质是。(2)、如图所示的垃圾箱分别回收四类垃圾,铝制饮料罐应该往_____________(填字母)类垃圾投放口投放。A、有害垃圾 B、厨余垃圾 C、可回收物 D、其他垃圾(3)、这种垃圾箱安装了太阳能板,白天收集阳光产生电流,能量被蓄电池储存,以便居民为手机、电瓶车充电,夜晚用这种垃圾箱为电瓶车充电时的能量转化是。13. 在Cu(NO3)2、Al(NO3)3和Fe(NO3)2的混合溶液中加入一定量的锌粉,充分反应后过滤,得到滤渣A和滤液B。向滤渣A 上滴加稀硫酸时有气泡产生。则滤液B 中一定含有的溶质有;反应后溶液的质量比原混合溶液的质量(填“大”或“小”)。14. 如图中标示的材料选择钛合金作为螺丝材料,是因为合金的硬度比组成金属的硬度(填“大”或“小”)。一种以甲醇为原料的新型手机电池,其容量为锂电池的10倍,电池反应原理为 。其中X的化学式为。常用的干电池内部填有氯化铵和二氧化锰等物质,若通过分离得到氯化铵,在实验室需进行的操作是、过滤和结晶,得到的氯化铵在农业上又可用作。
(1)、垃圾箱的板面由塑料制成,塑料属于材料,制作垃圾箱的边框使用了铁的合金,合金与组成它的纯金属比,一般具有的一条优良的物理性质是。(2)、如图所示的垃圾箱分别回收四类垃圾,铝制饮料罐应该往_____________(填字母)类垃圾投放口投放。A、有害垃圾 B、厨余垃圾 C、可回收物 D、其他垃圾(3)、这种垃圾箱安装了太阳能板,白天收集阳光产生电流,能量被蓄电池储存,以便居民为手机、电瓶车充电,夜晚用这种垃圾箱为电瓶车充电时的能量转化是。13. 在Cu(NO3)2、Al(NO3)3和Fe(NO3)2的混合溶液中加入一定量的锌粉,充分反应后过滤,得到滤渣A和滤液B。向滤渣A 上滴加稀硫酸时有气泡产生。则滤液B 中一定含有的溶质有;反应后溶液的质量比原混合溶液的质量(填“大”或“小”)。14. 如图中标示的材料选择钛合金作为螺丝材料,是因为合金的硬度比组成金属的硬度(填“大”或“小”)。一种以甲醇为原料的新型手机电池,其容量为锂电池的10倍,电池反应原理为 。其中X的化学式为。常用的干电池内部填有氯化铵和二氧化锰等物质,若通过分离得到氯化铵,在实验室需进行的操作是、过滤和结晶,得到的氯化铵在农业上又可用作。
三、科普阅读题
-
15. 阅读以下科普短文
19世纪初,铝是比黄金还贵的金属,主要是由于铝的化学性质很活泼,在自然界以化合物形式存在。当时采用钠与氯化铝在一定条件下发生置换反应得到铝,因生产成本高,所以铝十分珍贵。
19世纪末,霍尔应用电解熔融金属化合物的方法制备金属。他在用氧化铝制备金属铝的过程中,发现氧化铝的熔点很高(2 050 ℃),很难达到熔融状态,必须寻找一种能够溶解氧化铝而又能降低其熔点的材料,实验过程中发现冰晶石(Na3AlF6)能起到这种作用。
霍尔在坩埚中,把氧化铝溶解在10%~15%的熔融的冰晶石里进行电解,发现有小球状银白色的铝生成,同时放出氧气,冰晶石在电解过程中不被分解,并有足够的流动性,有利于电解的进行。这种廉价炼铝方法的发现,使铝成为广泛应用的金属材料,至今仍在使用。
根据文章内容,回答下列问题:
(1)、金属铝的物理性质(答一条)。(2)、冰晶石中氟元素的化合价为。(3)、写出电解氧化铝的化学方程式为。(4)、电解法制铝的过程中,冰晶石的作用是。四、简答题
-
16. 请用所学的化学知识解释下列问题:(1)、从分子的角度分析,湿衣服在阳光下比在阴凉处干得快的原因。(2)、农药“波尔多液 ”由硫酸铜和石灰乳配制而成,用化学方程式表示不能用铁制容器盛放的原因。
五、综合题
-
17. 质量守恒定律的发现,对科学的发展作出了重要贡献。(1)、为了验证质量守恒定律,实验小组分别选取以下三组药品,通过称量比较各组物质在密闭容器内混合前后的总质量,不能达到目的的有____。A、铁和硫酸铜溶液 B、铜和稀盐酸 C、白磷和空气(2)、在一定条件下,甲和乙反应生成丙,微粒变化如图所示(●、O表示不同原子):

则参加反应的甲、乙物质的分子数之比为 , 甲、乙、丙中属于单质的是 , 下列对反应前后的分析错误的是。
A.元素种类没有改变 B.原子种类没有改变
C.原子个数没有改变 D.分子种类没有改变
(3)、12g的碳在不同质量的氧气中燃烧,数据如右表。其中燃烧产物完全是一氧化碳的是(填标号)。

六、推断题
-
18. 某化工厂排放的废液中含有大量的硫酸锌和硫酸铜,化学兴趣小组的同学根据所学知识设计了一个方案,用来回收金属铜并得到硫酸锌晶体,主要过程如下图所示:

请回答下列问题:
(1)、步骤②中分离物质的方法是。(2)、固体A的成分是。(3)、步骤②中发生反应的化学方程式为 ,(4)、步骤③中加入的B物质是。七、实验探究题
-
19. 古文献记载:距4000—5000年我国古代人们已开始冶铸青铜器。青铜器表面常会有一层绿色的铜锈。
查阅资料:白色硫酸铜遇水变蓝色(反应方程式为Cu+5O=Cu·5O)
(1)、探究I:探究铜锈的组成用右图所示装置进行实验。观察到试管中固体由绿色变为黑色,干燥管内白色粉末变为蓝色,烧杯中澄清石灰水变浑浊。
烧杯中发生反应的化学方程式为。
(2)、由实验推测,铜锈中含有种元素。(3)、探究Ⅱ:探究铜生锈的条件利用下图装置和表中物质分别进行实验,放置相同时间,现象如下表。
 对比实验①和④可得到结论是。(4)、由探究Ⅱ实验得知,铜生锈的条件是。(5)、你对防止铜制品生锈的建议是。(6)、在上述探究的基础上,关于铜生锈,你还想继续探究的问题是 , 针对你提出的问题,验证实验的设计是。
对比实验①和④可得到结论是。(4)、由探究Ⅱ实验得知,铜生锈的条件是。(5)、你对防止铜制品生锈的建议是。(6)、在上述探究的基础上,关于铜生锈,你还想继续探究的问题是 , 针对你提出的问题,验证实验的设计是。八、计算题
-
20. 某工厂利用废铁屑与废硫酸反应制取硫酸亚铁。现有废硫酸19.6t(硫酸的质量分数为20%),与足量的废铁屑反应,可生成硫酸亚铁的质量?
-
-
-
-
-