九年级化学2022年寒假复习15
试卷更新日期:2023-01-13 类型:复习试卷
一、单选题
-
1. 下列有关试管使用的实验操作中错误的是( )A、向试管中加入粉末状固体
 B、用橡皮塞塞住试管
B、用橡皮塞塞住试管 C、加热固体
C、加热固体 D、检查装置气密性
D、检查装置气密性 2. 下列过程不会对空气造成污染的是( )。A、人和动物呼出的二氧化碳 B、煤燃烧产生的烟雾 C、汽车尾气排放的烟雾 D、石油化工厂排放的废气3. 中国科学院历经20余年攻关,研制出具有完整自主知识产权的星载铷原子钟,授时精度达到百亿分之三秒,已经用于“北斗”三号卫星导航系统,可提供分米级定位。在元素周期表中的信息如图所示,下列有关说法正确的是( )
2. 下列过程不会对空气造成污染的是( )。A、人和动物呼出的二氧化碳 B、煤燃烧产生的烟雾 C、汽车尾气排放的烟雾 D、石油化工厂排放的废气3. 中国科学院历经20余年攻关,研制出具有完整自主知识产权的星载铷原子钟,授时精度达到百亿分之三秒,已经用于“北斗”三号卫星导航系统,可提供分米级定位。在元素周期表中的信息如图所示,下列有关说法正确的是( )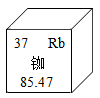 A、铷属于非金属元素 B、Rb+的核外电子数为37 C、铷元素相对原子质量为85.47g D、铷原子核内有37个质子4. 食醋的主要成分是醋酸(分子式为C2H4O2)。下列有关醋酸组成的说法中,正确的是( )A、醋酸分子中含有1个氧分子 B、醋酸是由碳元素、氢元素和氧元素组成的 C、醋酸中碳元素、氢元素和氧元素的质量比为1:2:1 D、醋酸是由2个碳原子、4个氢原子和2个氧原子构成的5. 下列图像与其对应关系正确的是( )A、
A、铷属于非金属元素 B、Rb+的核外电子数为37 C、铷元素相对原子质量为85.47g D、铷原子核内有37个质子4. 食醋的主要成分是醋酸(分子式为C2H4O2)。下列有关醋酸组成的说法中,正确的是( )A、醋酸分子中含有1个氧分子 B、醋酸是由碳元素、氢元素和氧元素组成的 C、醋酸中碳元素、氢元素和氧元素的质量比为1:2:1 D、醋酸是由2个碳原子、4个氢原子和2个氧原子构成的5. 下列图像与其对应关系正确的是( )A、 ①表示加热一定量的高锰酸钾固体
B、
①表示加热一定量的高锰酸钾固体
B、 ②表示一定量的镁在盛有空气的密闭容器中燃烧
C、
②表示一定量的镁在盛有空气的密闭容器中燃烧
C、 ③表示水在通电的条件下发生分解反应
D、
③表示水在通电的条件下发生分解反应
D、 ④表示相同的两份过氧化氢溶液在有无催化剂条件下制取氧气
6. 下列有关说法错误的是( )A、氧气用于病人的急救因为它有助燃性 B、金刚石用于切割玻璃因为它硬度大 C、氮气用作保护气因为它的化学性质不活泼 D、石墨用作电极因为它能导电7. 下列变化过程中不属于缓慢氧化的是( )A、呼吸作用 B、蜡烛燃烧 C、铁的生锈 D、米饭变馊
④表示相同的两份过氧化氢溶液在有无催化剂条件下制取氧气
6. 下列有关说法错误的是( )A、氧气用于病人的急救因为它有助燃性 B、金刚石用于切割玻璃因为它硬度大 C、氮气用作保护气因为它的化学性质不活泼 D、石墨用作电极因为它能导电7. 下列变化过程中不属于缓慢氧化的是( )A、呼吸作用 B、蜡烛燃烧 C、铁的生锈 D、米饭变馊二、填空题
-
8. 香烟烟气中有多种有害物质,(1)、如含碳物质不充分燃烧产生的、尼古丁和焦油,(2)、不吸烟的人能闻到烟味的原因是 ,(3)、随手丢弃的烟头还容易引发火灾,原因是(选填字母)
A 提供可燃物 B 提供氧气 C 使可燃物的温度达到着火点
(4)、一旦发生火灾,通常用水来灭火,该方法的灭火原理是。9. 解释下述实验现象。
序号
现象
解释
A
品红在热水中比在冷水中扩散快
B
湿的紫色石蕊纸条变红
10. 抗击新冠肺炎疫情期间,我县广大居民积极相应号召,减少外出,外出佩戴符合要求的口罩,对房间做好消毒,保持通风等。“84 消毒液”可以用作某些场所的消毒剂,其主要成分是次氯酸钠(NaClO),其中氯元素的化合价为;制取次氯酸钠的原理是: ,X的化学式是。11. 写出下列物质的化学符号(即化学式):汞、氧气、氯气、红磷、五氧化二磷、二氧化碳、二氧化硫、四氧化三铁、臭氧、二氧化锰。12. 早晨起来小张用淡盐水漱口,他从水壶中倒了一杯热水,想到了构成水的微观粒子是 , 他接着向水中加入一些食盐(主要成分是氯化钠),过一会发现食盐不见了,水却有了咸味,从微观角度分析产生此现象的主要原因是 , 用热水而没有用冷水配制盐水的微观原因是。13. 久置在空气中的石灰水,液面会形成一层白色薄膜,原因是空气中含有(化学用语填空);从冰箱中拿出饮料,瓶壁上立即有水珠出现,证明空气中含有 (化学用语填空);工业上制取氧气是利用不同,通过分离液态空气法来制取的,是变化;储存在蓝色钢瓶里的“工业液氧” 是(填“纯净物”或“混合物”)。14. 注意节约药品。应该严格按照试验规定的用量取用药品。如果没有说明用量,一般应该按取用药品,液体取 , 固体只需即可。三、科普阅读题
-
15. 阅读下列短文,回答相关问题。
中国有着悠久的酒文化。2016年, 海昏侯墓葬出土了青铜“蒸馏器”(如图1) ,“ 蒸馏器”上遍体的铜锈[Cu2 (OH) 2CO3]见证了我国蒸馏酒的历史,使现代人对蒸馏酒的认识提早了1000年。白酒一般是用高粱等谷物做主料或佐料酿制而成。制酒工艺主要流程包括:投料→发酵→蒸馏→老熟(贮存)。
发酵是指借助酵母菌所产生的酶的作用,使高粱等籽粒中的淀粉转化为葡萄糖(C6H12O6) ,葡萄糖在酶的作用下进一步氧化产生乙醇(C2H5OH) 和二氧化碳等。发酵环境pH为4-5时、发酵速度快,超出这个范围,就会抑制酵母繁殖、发酵速率减慢、且出酒率降低。在正常条件下,发酵池中酒精含量随时间的变化情况如图2所示。
发酵得到的并不是通常市场上见到的饮用酒、其酒精含量一般在67%,同时含有多种脂类、醛和酸。一般需要蒸馏和浓缩,使酒精浓度达到50-70%,蒸馏得到的酒中还含有杂酯油及酯类等。
新蒸出的白酒,气味不正,因为新酒中含有硫化氢、硫醇等臭味物质。硫化氢、硫醇等低沸点物质挥发出来后,酒的杂味会大为减少,所以需要贮存老熟的过程。硫化氢有剧毒,易溶于水,密度比空气大。硫化亚铁 (FeS) 是一种黑色块状固体,把稀硫酸滴在硫化亚铁表面,会产生硫化氢气体,同时也能得到硫酸亚铁,实验室常利用这个反应制取硫化氢。
老熟过程中会发生氧化、还原、酯化、水解等各种反应,使酒中醇、酸、酯、醛等物质达到最佳值,香气增加,酒味柔和。清香型酒的主体香是乙酸乙酯,在老熟一年半左右时间达到最高值,贮存期延长,主体香成分反而下降。老熟10年的酒,其主体香成分降低大约75%。说明白酒必须有一定的贮存期。

 (1)、铜生锈的过程属于氧化(选填“剧烈”或“缓慢”)。(2)、在粮食发酵生成酒精过程中,酒精含量增长最快的时间为____。A、发酵前两天 B、发酵7天以后 C、在发酵中期(3)、由葡萄糖制取的乙醇可用于酿酒。 此外,乙醇还是发展绿色新能源的重要方法,请写出乙醇燃烧产生二氧化碳与水的化学文字表达式。(4)、在饮酒、酒酿制过程要注意的问题,正确的是____。A、酒越陈越香 B、老熟过程只发生化学变化 C、发酵期越长,发酵池中酒精含量越高 D、白酒的香味不是酒精的气味(5)、实验室制取少量硫化氢气体时,应选用图3中装置作为发生装置(用序号回答),若选用D装置作为收集装置,气体由(填导管口代号)导入集气瓶。图B中e仪器的名称为。
(1)、铜生锈的过程属于氧化(选填“剧烈”或“缓慢”)。(2)、在粮食发酵生成酒精过程中,酒精含量增长最快的时间为____。A、发酵前两天 B、发酵7天以后 C、在发酵中期(3)、由葡萄糖制取的乙醇可用于酿酒。 此外,乙醇还是发展绿色新能源的重要方法,请写出乙醇燃烧产生二氧化碳与水的化学文字表达式。(4)、在饮酒、酒酿制过程要注意的问题,正确的是____。A、酒越陈越香 B、老熟过程只发生化学变化 C、发酵期越长,发酵池中酒精含量越高 D、白酒的香味不是酒精的气味(5)、实验室制取少量硫化氢气体时,应选用图3中装置作为发生装置(用序号回答),若选用D装置作为收集装置,气体由(填导管口代号)导入集气瓶。图B中e仪器的名称为。四、简答题
-
16. 2018年第二十六届“世界水日”,我国的宣传主题是“实施国家节水行动,建设节水型社会”。请你淡淡为什么要节约用水?说出你节约用水的两个例子。
五、综合题
-
17. “珍惜水、节约水、保护水”是每个公民的义务和责任。(1)、下列“水”属于纯净物的是(填序号)
A蒸馏水 B河水 C自来水
(2)、用如下图甲装置进行电解水的实验,b中收集到的气体是该实验说明水是由组成的.电解水的反应文字表达式为。(3)、我国水资源分布不均匀.有些村民用地下水作为生活用水,人们常用检验地下水是硬水还是软水;生活中可用的方法降低水的硬度;某同学自制下图乙所示简易净水器,图中活性炭的主要作用是(4)、请举一例生活中节约用水的具体措施
六、推断题
-
18. 有限的元素可以组成种类繁多的物质,请依据H、C、O、Mn、P等元素回答下列问题。(1)、氧原子最外层电子数有6个,在化学反应中较易(填“得到”或“失去”)电子。(2)、有过氧化氧溶液和水两瓶无色液体,可以用(写化学式)区分。(3)、请写出红磷在氧气中燃烧的化学方程式。(4)、甲、乙、丙是由上述部分元素组成的初中化学常见物质,它们之间有如图所示转化关系(部分反应物、生成物及反应条件已略去,“─”表示相邻的两种物质能发生反应,“→”表示某一物质经一步反应可转化为另一种物质)。

①若丙能通过光合作用转化为乙,则乙的化学式为;
②关于转化,下列说法错误的是(填字母序号)。
A.若丙是二氧化碳,则甲可以是碳
B.若乙是氧气,则乙→丙一定是氧化反应
C.若丙是水,则甲一定是氢气
D.若丙是水,则甲、乙间的反应一定放热
七、实验探究题
-
19. 根据下列实验装置图填空:
 (1)、写出上图中标有序号②的仪器名称是。(2)、实验室中用过氧化氢溶液与二氧化锰固体混合制取氧气,反应的化学方程式是 , 应选择的发生装置为。(填序号)(3)、若选择C装置收集一瓶氧气,判断氧气已收集满的方法是。(4)、甲烷是一种无色无味、难溶于水、密度比空气小的气体。实验室用加热无水醋酸钠和碱石灰的固体混合物制取甲烷并收集较纯净的甲烷气体,应选择的发生装置和收集装置是(填序号)。
(1)、写出上图中标有序号②的仪器名称是。(2)、实验室中用过氧化氢溶液与二氧化锰固体混合制取氧气,反应的化学方程式是 , 应选择的发生装置为。(填序号)(3)、若选择C装置收集一瓶氧气,判断氧气已收集满的方法是。(4)、甲烷是一种无色无味、难溶于水、密度比空气小的气体。实验室用加热无水醋酸钠和碱石灰的固体混合物制取甲烷并收集较纯净的甲烷气体,应选择的发生装置和收集装置是(填序号)。八、计算题
-
20. 牛奶是我们日常生活中一种营养丰富的饮品,每天饮用可补充人们对钙等营养物质的需求。其中营养成分的具体含量如下表所示。
项目
每100mL
能量
272kJ
蛋白质
3.2g
脂肪
3.8g
碳水化合物
4.5g
钠
60mg
钙
110mg
非脂乳固体
≥8.1%
请根据资料回答下列问题:
(1)、通常中学生每天需从牛奶中补充550mg的钙,若一盒牛奶为250mL,则理论上每天应喝盒牛奶。(2)、牛奶中的钙主要以磷酸钙[Ca3(PO4)2]的形式存在,磷酸钙中钙元素的质量分数为(写出计算过程,计算结果保留至0.1%)。
-
-
-
-
-