八年级科学2022年寒假每日一练:22(预习)
试卷更新日期:2023-01-13 类型:复习试卷
一、单选题
-
1. 模型法是学习科学的重要方法,下列不属于模型法的是( )A、
 光线
B、
光线
B、 磁感线
C、
磁感线
C、 水分子
D、
水分子
D、 氢元素
2. 英国科学家在金星大气层中发现了“生物标志”——磷化氢(PH3)气体。如果用“O”表示氢原子,用“
氢元素
2. 英国科学家在金星大气层中发现了“生物标志”——磷化氢(PH3)气体。如果用“O”表示氢原子,用“ ”表示磷原子,则下列模型可以表示磷化氢分子PH3的是( ) A、
”表示磷原子,则下列模型可以表示磷化氢分子PH3的是( ) A、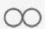 B、
B、 C、
C、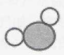 D、
D、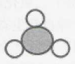 3. 元素“Al”的名称是( )A、氦 B、氯 C、硅 D、铝4. 人体中含有30多种元素,由它们构成了人体的各种化合物,其中水分约占体重的60%一70%,由此判断人体中质量分数最大的元素是( )A、H B、C C、Fe D、O5. 一种有趣的钟表式元素周期表如图所示,下列说法中不正确的是( )
3. 元素“Al”的名称是( )A、氦 B、氯 C、硅 D、铝4. 人体中含有30多种元素,由它们构成了人体的各种化合物,其中水分约占体重的60%一70%,由此判断人体中质量分数最大的元素是( )A、H B、C C、Fe D、O5. 一种有趣的钟表式元素周期表如图所示,下列说法中不正确的是( ) A、一点整,时针所指元素为金属元素 B、六点整,时针所指元素的质子数为6 C、十一点整,时针所指元素的离子符号为Na D、钟面上时针、分针所指的两种元素组成化合物的化学式为MgO6. 化学式H2O2能表示多种意义,下列说法错误的是( )A、表示过氧化氢这一物质 B、表示过氧化氢由氢元素和氧元素组成 C、表示一个过氧化氢分子 D、表示过氧化氢由2个氢原子和2个氧原子组成7. 2020年初出现了罕见的新型冠状病毒疫情,过氧乙酸(分子模型如图)能有效杀灭病毒。下列关于过氧乙酸的说法中正确的是( )
A、一点整,时针所指元素为金属元素 B、六点整,时针所指元素的质子数为6 C、十一点整,时针所指元素的离子符号为Na D、钟面上时针、分针所指的两种元素组成化合物的化学式为MgO6. 化学式H2O2能表示多种意义,下列说法错误的是( )A、表示过氧化氢这一物质 B、表示过氧化氢由氢元素和氧元素组成 C、表示一个过氧化氢分子 D、表示过氧化氢由2个氢原子和2个氧原子组成7. 2020年初出现了罕见的新型冠状病毒疫情,过氧乙酸(分子模型如图)能有效杀灭病毒。下列关于过氧乙酸的说法中正确的是( )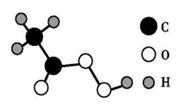 A、 过氧乙酸的分子式为CH3COOH B、过氧乙酸是由碳、氢、氧三种原子构成 C、过氧乙酸的相对分子质量是76 D、过氧乙酸中碳元素的质量分数最大
A、 过氧乙酸的分子式为CH3COOH B、过氧乙酸是由碳、氢、氧三种原子构成 C、过氧乙酸的相对分子质量是76 D、过氧乙酸中碳元素的质量分数最大二、填空题
-
8. 已知一个SO2 分子的质量为a克,一个SO3分子的质量为b克,若以一个硫原子质量的1/32作为相对原子质量的标准,则SO2的相对分子质量为9. 氕、氘、氚是氢的三种同位素原子,它们的原子结构模型如图所示,相关信息如下表。试回答:
名称
符号
相对原子质量
氕
H
1
氘
D
2
氚
T
3
 (1)、原子结构模型中的“〇”表示的粒子是。(2)、超重水有一定的放射性。一个超重水分子由两个氚原子和一个氧原子构成,其化学式可表示为T2O,T2O中T的化合价为。(3)、重水是由氘和氧组成的化合物,化学式可表示为D2O,重水和普通水化学性质相似。在海水中重水的质量约占0.02%,则100吨海水中所含氘的质量是吨。10. 我们可以从元素周期表上获得有关元素的许多信息。下表是元素周期表的一部分,请回答下列问题:
(1)、原子结构模型中的“〇”表示的粒子是。(2)、超重水有一定的放射性。一个超重水分子由两个氚原子和一个氧原子构成,其化学式可表示为T2O,T2O中T的化合价为。(3)、重水是由氘和氧组成的化合物,化学式可表示为D2O,重水和普通水化学性质相似。在海水中重水的质量约占0.02%,则100吨海水中所含氘的质量是吨。10. 我们可以从元素周期表上获得有关元素的许多信息。下表是元素周期表的一部分,请回答下列问题: (1)、①和③处于同一(选填“周期”或“族”)。(2)、②和⑤是不同种元素,它们之间最本质的区别是(选填“质子数”或“中子数”)不同。(3)、③和④组成的物质是由 (选填“分子”、“原子”或“离子”)构成的。11. 用化学用语填空:(1)、氩气;(2)、4 个二氧化硫分子;(3)、2 个氢氧根离子;(4)、空气中含量最多的物质(5)、保持水的化学性质的最小微粒;12. 常见的分子模型的形象表示方法有2种:球棍模型、比例模型。(1)、请你写出下图乙烷对应的模型。
(1)、①和③处于同一(选填“周期”或“族”)。(2)、②和⑤是不同种元素,它们之间最本质的区别是(选填“质子数”或“中子数”)不同。(3)、③和④组成的物质是由 (选填“分子”、“原子”或“离子”)构成的。11. 用化学用语填空:(1)、氩气;(2)、4 个二氧化硫分子;(3)、2 个氢氧根离子;(4)、空气中含量最多的物质(5)、保持水的化学性质的最小微粒;12. 常见的分子模型的形象表示方法有2种:球棍模型、比例模型。(1)、请你写出下图乙烷对应的模型。
 (2)、能清楚地反映乙烷分子里碳、氢原子的大小和相对位置的是( )A、球棍模型 B、比例模型13. 碘是一种由碘分子构成的非金属,某同学利用碘进行了如下的实验:
(2)、能清楚地反映乙烷分子里碳、氢原子的大小和相对位置的是( )A、球棍模型 B、比例模型13. 碘是一种由碘分子构成的非金属,某同学利用碘进行了如下的实验:①把少量的固体碘放在湿润的馒头上,发现馒头会变成蓝色;
②再取少量的碘溶解在水中,用馒头去蘸取碘液,发现馒头也会变成蓝色。则:
(1)、取少量的碘放入烧杯中,用酒精灯加热,碘升华变成碘蒸气,把湿润的馒头放在碘蒸气中,馒头(选填“会”或“不会”)变成蓝色。(2)、把碘溶解在酒精中,用馒头去蘸取少量的碘酒,馒头(选填“会”或“不会”) 变成蓝色。(3)、请用分子的观点来解释实验中的现象。14. 下表是小明收集的一些微粒的资料,请根据表格数据,回答下列问题。粒子名称
质子数
中子数
电子数
A
14
14
14
B
26
30
24
C
14
14
18
D
14
18
14
(1)、表中的元素共有种。(2)、属于阳离子的是(填字母)。(3)、与A互为同位素原子的是。三、实验探究题
-
15. 为纪念门捷列夫发明的元素周期表诞生150周年,联合国大会宣布2019年是“国际化学元素周期表年”。
材料一:门捷列夫将元素按照相对原子质量从小到大排列后,发现元素的化学性质成周期性出现,故将相似化学性质的元素排在同一列。
材料二:门捷列夫无可非议地成为元素周期律的主要发现者,因为门捷列夫的元素周期表有强大的预测功能。
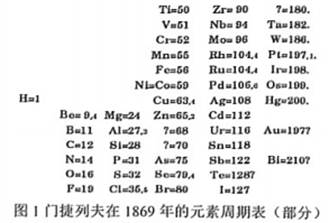
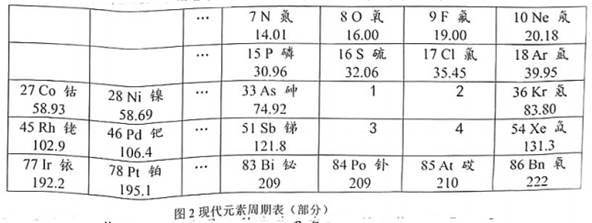
材料三:氟是一种非金属化学元素,氟元素的单质是F2 , 它是一种淡黄色有剧毒的气体。氟气的腐蚀性很强,化学性质极为活泼,是氧化性最强的物质之一。
硫是一种非金属元素,通常单质硫是黄色的品体。硫元素在自然界中通常以化合物或单质的形式存在。硫单质难溶于水,微溶于酒精对人体而言,单质硫通常是无毒无害的。
(1)、根据现代周期表的元素排布特点,下列哪两种元素的化学性质相似?( )A、F、Ne B、N、O C、N、S D、N、P(2)、结合材料中图1和图2,现在的元素周期表编制与门捷列夫的元素周期表排列规律有什么相矛盾的地方?(3)、溴是一种化学元素,相对原子质量是79.9, 溴单质是红黑色液体,溴蒸气具有腐蚀性,并且有毒。请你结合材料预测溴在图2元素周期表中的位置(选择标准序号),并说明理由。四、解答题
-
16. 2022年3月23日,“天宫课堂”第二课开讲,航天员王亚平利用过饱和醋酸钠(化学式为CH3COONa)溶液,演示了太空“冰雪”实验(如图)。
 (1)、醋酸钠由种元素组成;(2)、醋酸钠的相对分子质量为;(3)、16.4克醋酸钠中钠元素质量为多少?
(1)、醋酸钠由种元素组成;(2)、醋酸钠的相对分子质量为;(3)、16.4克醋酸钠中钠元素质量为多少?
-