江苏省淮安市淮阴区2021-2022学年九年级下学期3月质量监测化学试题
试卷更新日期:2023-01-12 类型:月考试卷
一、单选题
-
1. 把少量下列物质分别放入水中,充分搅拌,可以得到溶液的是( )A、面粉 B、泥土 C、蔗糖 D、汽油2. 下列溶液在空气中敞口久置,因发生化学变化导致溶液质量减小的是( )A、浓盐酸 B、浓硫酸 C、石灰水 D、烧碱溶液3. 下列实验操作正确的是:A、
 称取食盐
B、
称取食盐
B、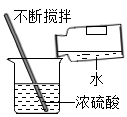 稀释浓硫酸
C、
稀释浓硫酸
C、 测定溶液的pH
D、
测定溶液的pH
D、 固体药品的取用
4. 下表是一些食物的pH值,其中酸性最强的是
固体药品的取用
4. 下表是一些食物的pH值,其中酸性最强的是物质
A.酸奶
B.鸡蛋清
C.牙膏
D.肥皂水
pH范围(常温)
4-5
7-8
8-9
10-11
A、A B、B C、C D、D5. 下面是小芳同学在学习酸、碱的性质时记录的部分实验现象。其中正确的是A、打开盛有浓硫酸的试剂瓶瓶盖,瓶口有白雾产生 B、氢氧化钠固体露置于空气中,表面变湿润 C、向硫酸铜溶液中滴加氢氧化钠溶液,产生红色沉淀 D、向金属镁中滴加稀盐酸,有氢气生成6. 将X、Y、Z三块大小相同的金属片分别投入到10%的稀硫酸中,X表面无明显现象,Y表面缓慢产生气泡,Z表面迅速产生大量气泡。则X、Y、Z的金属活动性顺序为A、X>Z>Y B、Z>X>Y C、X>Y>Z D、Z>Y>X7. 误差分析是定量实验的一个重要内容,下列分析正确的是A、用量筒量取10mL水,仰视读数会导致水的实际体积偏小 B、测定溶液的pH,先用水将pH试纸润湿,会导致测出的pH偏大 C、用红磷燃烧测定空气中氧气的体积分数,红磷的量不足会导致结果偏小 D、配制溶质量分数为6%的氯化钠溶液,氯化钠中含有杂物,导致氯化钠的质量分数偏大8. 食醋里通常含有3~5%的醋酸(CH3COOH,食醋与鸡蛋壳反应产生能使澄清石灰水变浑浊的气体。下列说法错误的是A、食醋能使石蕊试液变红 B、加水稀释食醋,溶液pH变小 C、醋酸在水溶液里能解离出H+ D、不宜用铝制容器盛装食醋9. 在密闭容器中有甲、乙、丙、丁四种物质,在一定条件下反应,测得反应前后各物质的质量分数如图所示.下列说法正确的是( ) A、丙可能是单质 B、丁一定是该反应的催化剂 C、若消耗3 g的乙,则生成17 g的丙 D、反应前甲、乙的质量之和一定等于反应后丙的质量10. 下列物质的提纯所用试剂和主要实验操作均正确的是( )
A、丙可能是单质 B、丁一定是该反应的催化剂 C、若消耗3 g的乙,则生成17 g的丙 D、反应前甲、乙的质量之和一定等于反应后丙的质量10. 下列物质的提纯所用试剂和主要实验操作均正确的是( )选项
物质(括号内为杂质)
所用试剂
主要实验操作
A
H2O(H2O2)
MnO2
过滤
B
CaCl2(NaCl)
适量Na2CO3溶液
沉淀、过滤、蒸发、结晶
C
CO2(CO)
过量O2
点燃
D
Al(Al2O3)
足量稀H2SO4
溶解、过滤
A、A B、B C、C D、D二、填空题
-
11. 现有①熟石灰②生石灰③盐酸,选择适当的物质填空(填序号)。(1)、可用作干燥剂的是。(2)、用于中和酸性土壤的是。(3)、胃液中含有的酸是。12. 化学与生活息息相关,请用学过的化学知识解决下列问题。(1)、餐具上的油污用加入洗洁精的水更容易洗掉,原因是洗洁精具有作用。(2)、人们用稀盐酸除去铁制品表面铁锈的反应方程式为:。13. 如图是足超市销售的一种食盐标签的部分文字说明。从成分上看,食盐中除含NaCl外还有KIO3 , 其中KlO3的作用是 , KIO3中碘元素(I)的化合价是 , 食用时勿长时间加热,原因是碘酸钾受热会分解: , R的化学式是。
 14. 如图是KNO3和NaCl两种物质的溶解度曲线。
14. 如图是KNO3和NaCl两种物质的溶解度曲线。 (1)、10℃时,硝酸钾的溶解度是。(2)、60℃时,将60g硝酸钾晶体放入50g水中,充分搅拌后,所得溶液的质量为g。(3)、a点的KNO3和NaCl两份饱和溶液,同时升温至60℃(不考虑水的蒸发),则此时两溶液的溶质质量分数(ω)的大小关系为:ω(KNO3)(填“>”、“<”或“=”)ω(NaCl)。(4)、NaCl固体中含有KNO3杂质,若要得到纯净的NaCl固体,实验步骤为溶解、、洗涤、干燥。
(1)、10℃时,硝酸钾的溶解度是。(2)、60℃时,将60g硝酸钾晶体放入50g水中,充分搅拌后,所得溶液的质量为g。(3)、a点的KNO3和NaCl两份饱和溶液,同时升温至60℃(不考虑水的蒸发),则此时两溶液的溶质质量分数(ω)的大小关系为:ω(KNO3)(填“>”、“<”或“=”)ω(NaCl)。(4)、NaCl固体中含有KNO3杂质,若要得到纯净的NaCl固体,实验步骤为溶解、、洗涤、干燥。三、综合题
-
15. 归纳总结是学习化学的重要方法,某同学用图1总结了NaOH的四条化学性质(即NaOH能够与四类物质发生化学反应)。
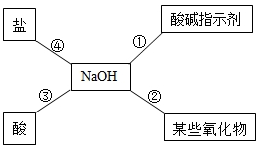 (1)、依据图中反应②写出NaOH在空气中变质的化学方程式:。(2)、二氧化碳与氢氧化钠溶液的反应本身没有明显现象,但可以通过转化产生现象。
(1)、依据图中反应②写出NaOH在空气中变质的化学方程式:。(2)、二氧化碳与氢氧化钠溶液的反应本身没有明显现象,但可以通过转化产生现象。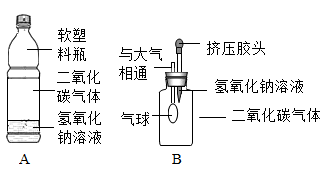
①A组实验(如图所示),看到软塑料瓶变瘪,这种现象是因为试管内外产生差,B中实验现象为:。
②上述实验不足以说明二氧化碳与氧氧化钠溶液发生了化学反应,需将A中氢氧化钠溶液换成等体积的重做实验。进行对比。
16. 实验室利用实验装置进行有关化学实验,回答下列问题: (1)、写出图中仪器甲的名称:甲。(2)、实验室制取二氧化碳发生装置可选择图中的(填标号),用装置C收集二氧化碳,验满时,燃着木条应放在(填“a”或“b”)端。某同学误用浓盐酸制取二氧化碳,生成的气体通入澄清石灰水没有看到沉淀是因为气体中含有较多的(填化学式)。(3)、用上述制取二氧化碳实验后的固液残留物进行过滤,应选择图中(填标号)装置,该操作中玻璃棒的作用是。17. 如图是实验室配制一定溶质质量分数的氯化钠溶液的流程图。请回答:
(1)、写出图中仪器甲的名称:甲。(2)、实验室制取二氧化碳发生装置可选择图中的(填标号),用装置C收集二氧化碳,验满时,燃着木条应放在(填“a”或“b”)端。某同学误用浓盐酸制取二氧化碳,生成的气体通入澄清石灰水没有看到沉淀是因为气体中含有较多的(填化学式)。(3)、用上述制取二氧化碳实验后的固液残留物进行过滤,应选择图中(填标号)装置,该操作中玻璃棒的作用是。17. 如图是实验室配制一定溶质质量分数的氯化钠溶液的流程图。请回答: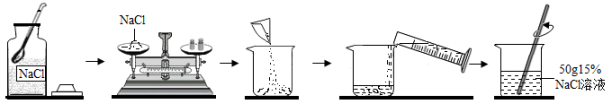 (1)、应称量g氯化钠固体。(2)、若称量氯化钠固体时指针向右偏转,则应直到天平平衡。(3)、下列操作中可能导致配制氯化钠溶液的溶质质量分数偏小的是| 。(填序号)A、氯化钠中含有杂质 B、量取水时俯视 C、用已有少量水的烧杯溶解氯化钠 D、转移时,有少量溶液溅出(4)、取上述溶液10g,需加g水稀释,可得到5%的氯化钠溶液。18. 某化学兴趣小组的同学向氢氧化钠溶液中滴加稀盐酸时,没有看到明显现象。
(1)、应称量g氯化钠固体。(2)、若称量氯化钠固体时指针向右偏转,则应直到天平平衡。(3)、下列操作中可能导致配制氯化钠溶液的溶质质量分数偏小的是| 。(填序号)A、氯化钠中含有杂质 B、量取水时俯视 C、用已有少量水的烧杯溶解氯化钠 D、转移时,有少量溶液溅出(4)、取上述溶液10g,需加g水稀释,可得到5%的氯化钠溶液。18. 某化学兴趣小组的同学向氢氧化钠溶液中滴加稀盐酸时,没有看到明显现象。(提出问题)氢氧化钠与盐酸是否发生了化学反应?
(查阅资料)酸与碱发生中和反应会放出热量,
(1)、(实验设计)甲、乙、丙三位同学分别设计了如下实验方案,请你帮他们完成实验报告。同学
实验操作
现象
结论
甲
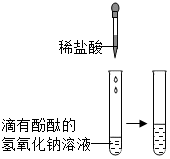
溶液由红色变成色
氢氧化钠与盐酸发生化学反应,化学方程式为
乙
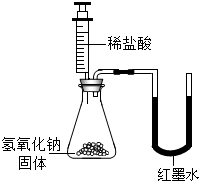
U形玻璃管中边的红墨水液面下降(所加稀盐酸的体积忽略不计)
氢氧化钠与盐酸发生了化学反应
丙
用pH试纸测定氢氧化钠溶液的pH:向其中滴加足量的稀盐酸后再测定溶液的pH
最后溶液的pH(填“≥7”“≤7”或“不变)
氢氧化钠与盐酸发生了化学反应
(2)、乙同学实验设计方案不合理的理由是。(3)、从微观的角度说明酸碱中和反应发生的实质是。(4)、丙同学实验过程中溶液的pH变化曲线如图所示,回答下列问题:
①当两种溶液恰好完全反应时,对应的是图中的点(填“a” “b”或“c”)。
②图中的c点溶液中含有的阳离子是(填离子符号)。
四、计算题
-
19. 化学探究小组为测定某石灰石样品中碳酸钙的质量分数,取25g石灰石样品放在烧杯中,然后向其中逐滴加入一定量某质量分数的稀盐酸,使之与样品充分反应(杂质不参加反应),随着反应进行,加入稀盐酸的质量与反应得到气体的质量变化关系如图所示。请完成下列计算内容:
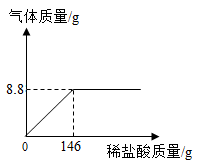 (1)、反应生成二氧化碳质量为g。(2)、所用稀盐酸溶质的质量分数是多少?(写出计算过程)。
(1)、反应生成二氧化碳质量为g。(2)、所用稀盐酸溶质的质量分数是多少?(写出计算过程)。