八年级科学下册2.3原子结构的模型同步练习
试卷更新日期:2023-01-10 类型:同步测试
一、单选题
-
1. 道尔顿的原子学说曾经起到了很大作用。他的学说中,包含下述三个论点:①原子是不能再分的粒子;②同种元素的原子各种性质和质量都相同;③原子是微小的实心球体。从现在的观点看,你认为这三个论点中不确切的是( )A、只有③ B、只有①③ C、只有②③ D、①②③2. 科学家在地壳中发现了氦-3原子,它的中子数量与普通氦原子不同,故表现出众多优越特性。如图为其原子结构示意图,其中“
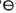 ”表示核外电子,则氦-3原子含有的质子数为( )
”表示核外电子,则氦-3原子含有的质子数为( )  A、1 B、2 C、3 D、53. 鈈(xi)元素是首个由亚洲科学家发现的新元素。鈈原子的相对原子质量为286,核外电子数为113,则质子数为( )A、286 B、113 C、173 D、3994. 2021年,我国科学家首次合成铀-214,是目前已知质量最小的铀原子。其相对原子质量为214,质子数为92,则铀-214 原子的中子数为( )A、92 B、122 C、214 D、3065. 考古人员使用碳-14年代检测法印证了三星堆遗址属于商代晚期。碳-14原子与碳-12原子不同的是( )A、核电荷数 B、质子数 C、核外电子数 D、中子数6. 日本政府计划在2023年春季将福岛核废水排入海里,核废水中含有大量的氚。氚一旦进入人体可能会对人造成辐射损害。氢原子和氚原子结构如图所示,下 列说法正确的是( )
A、1 B、2 C、3 D、53. 鈈(xi)元素是首个由亚洲科学家发现的新元素。鈈原子的相对原子质量为286,核外电子数为113,则质子数为( )A、286 B、113 C、173 D、3994. 2021年,我国科学家首次合成铀-214,是目前已知质量最小的铀原子。其相对原子质量为214,质子数为92,则铀-214 原子的中子数为( )A、92 B、122 C、214 D、3065. 考古人员使用碳-14年代检测法印证了三星堆遗址属于商代晚期。碳-14原子与碳-12原子不同的是( )A、核电荷数 B、质子数 C、核外电子数 D、中子数6. 日本政府计划在2023年春季将福岛核废水排入海里,核废水中含有大量的氚。氚一旦进入人体可能会对人造成辐射损害。氢原子和氚原子结构如图所示,下 列说法正确的是( )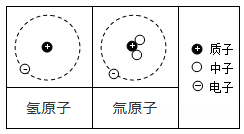 A、氚原子与氢原子的核外电子数相同 B、氚原子与氢原子的核电荷数不同 C、氚与氢元素不属于同种元素 D、氚原子与氢原子相对原子质量相同7. 科学家在挑战人工合成更高顺位的元素,目前已合成到了118号元素
A、氚原子与氢原子的核外电子数相同 B、氚原子与氢原子的核电荷数不同 C、氚与氢元素不属于同种元素 D、氚原子与氢原子相对原子质量相同7. 科学家在挑战人工合成更高顺位的元素,目前已合成到了118号元素 。
。  原子的相对原子质量为294,质子数为118。则该原子的核外电子数为( ) A、118 B、176 C、294 D、4128. 二氧化锰(MnO2)、二氧化硫(SO2)、二氧化碳(CO2)这三种物质都含有( )A、氧元素 B、氧分子 C、氧原子 D、氧离子9. 下列所描述的粒子与氧原子一致的是( )A、该粒子有8个质子,9个中子,10个电子 B、该粒子有9个质子,8个中子,10个电子 C、该粒子有8个质子,10个中子,8个电子 D、该粒子有9个质子,10个中子,8个电子10. 如图是卢瑟福将带正电的a粒子流轰击金箔上出现散射的实验示意图。以下是根据该实验现象作出的推断,不合理的是( )
原子的相对原子质量为294,质子数为118。则该原子的核外电子数为( ) A、118 B、176 C、294 D、4128. 二氧化锰(MnO2)、二氧化硫(SO2)、二氧化碳(CO2)这三种物质都含有( )A、氧元素 B、氧分子 C、氧原子 D、氧离子9. 下列所描述的粒子与氧原子一致的是( )A、该粒子有8个质子,9个中子,10个电子 B、该粒子有9个质子,8个中子,10个电子 C、该粒子有8个质子,10个中子,8个电子 D、该粒子有9个质子,10个中子,8个电子10. 如图是卢瑟福将带正电的a粒子流轰击金箔上出现散射的实验示意图。以下是根据该实验现象作出的推断,不合理的是( )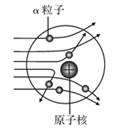 A、绝少数a粒子向两侧偏转,说明原子中心的“核”带正电 B、绝少数a粒子偏转的角度很大,说明原子“核”外有带负电的电子 C、绝大多数a粒子仍沿原来方向穿过,说明原子中绝大部分是“空”的 D、绝少数a粒子被反弹回来,说明原子中心有一个体积小而质量大的“核”11. 如图所示,1911年卢瑟福用带正电的α粒子轰击金属箔,实验发现:
A、绝少数a粒子向两侧偏转,说明原子中心的“核”带正电 B、绝少数a粒子偏转的角度很大,说明原子“核”外有带负电的电子 C、绝大多数a粒子仍沿原来方向穿过,说明原子中绝大部分是“空”的 D、绝少数a粒子被反弹回来,说明原子中心有一个体积小而质量大的“核”11. 如图所示,1911年卢瑟福用带正电的α粒子轰击金属箔,实验发现:
①大多数α粒子能穿透金属箔而不改变原来的运动方向;②一小部分α粒子改变了原来的运动方向;
③有极少数α粒子被弹了回来。根据以上实验现象, 可以得到( )
A、原子核带正电荷 B、原子是一个实心球体 C、电子只能在原子内的一些特定的稳定轨道上运动 D、原子核体积很大,但是质量比α粒子小得多12. 科学家通常采用两种相对较“轻”的元素,让它们的原子核高速碰撞聚合为一个新的核,从而合成出新的元素,如原子序数为113、114、115等元素,这些元素最本质的区别是( )A、中子数不同 B、电子数不同 C、质子数不同 D、相对原子质量不同13. 为了进一步探索原子的结构,卢瑟福用粒子轰击金属箔。如图所示表示a粒子的运动轨迹,其中错误的是( )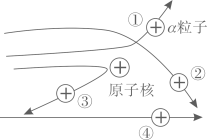 A、① B、② C、③ D、④14. 化学上常用符号“ZAX”表示原子的组成,其中X代表元素符号,Z表示原子核内的质子数,A表示原子核内质子数与中子数之和。已知 abXn+和 cdYm﹣的电子层排布完全相同,则下列关系正确的是( )A、b-a=d-c B、a+n=c-m C、a-n=c+m D、b-n=d+m15. 医学上用碘的同位素治疗甲亢已非常普遍。从 1942 年第一例放射性元素碘-131 治疗甲亢以来有效性和安全性就得到了充分的证实。已知碘-131 原子的核电荷数为 53,中子数为 78,则该原子核外电子数为( )A、25 B、53 C、78 D、131
A、① B、② C、③ D、④14. 化学上常用符号“ZAX”表示原子的组成,其中X代表元素符号,Z表示原子核内的质子数,A表示原子核内质子数与中子数之和。已知 abXn+和 cdYm﹣的电子层排布完全相同,则下列关系正确的是( )A、b-a=d-c B、a+n=c-m C、a-n=c+m D、b-n=d+m15. 医学上用碘的同位素治疗甲亢已非常普遍。从 1942 年第一例放射性元素碘-131 治疗甲亢以来有效性和安全性就得到了充分的证实。已知碘-131 原子的核电荷数为 53,中子数为 78,则该原子核外电子数为( )A、25 B、53 C、78 D、131二、填空题
-
16. 人类对微观世界的探究永无止境。请根据所学知识回答:
 (1)、1911年,卢瑟福进行α粒子散射实验后,认为原子是“行星模型”,即原子是由带电荷的原子核和核外电子构成。(2)、如图甲是卢瑟福用α粒子轰击金属箔而产生散射的实验,在分析实验结果的基础上,他提出了图乙所示的原子核式结构,卢瑟福的这一研究过程是一个__ 。A、建立模型的过程 B、得出结论的过程 C、提出问题的过程 D、验证证据的过程(3)、卢瑟福在α散射实验中( α粒子带正电荷) ,断定原子中的绝大部分空间是空的,他的依据是。17. 人类为了揭示原子结构的奥秘,经历了漫长的探究过程。请回答:(1)、汤姆生认为原子是个球体,正电荷均匀分布在整个球体内,而如今这个观点是 (选填“正确”或“错误")的。(2)、卢瑟福提出了原子的核式结构模型,认为原子的全部正电荷和几乎全部的质量都集中。(3)、卢瑟福核式结构模型是利用a粒子轰击金箔实验的基础上提出的。下列能正确反映他的实验结果的示意图是 (选填序号)。
(1)、1911年,卢瑟福进行α粒子散射实验后,认为原子是“行星模型”,即原子是由带电荷的原子核和核外电子构成。(2)、如图甲是卢瑟福用α粒子轰击金属箔而产生散射的实验,在分析实验结果的基础上,他提出了图乙所示的原子核式结构,卢瑟福的这一研究过程是一个__ 。A、建立模型的过程 B、得出结论的过程 C、提出问题的过程 D、验证证据的过程(3)、卢瑟福在α散射实验中( α粒子带正电荷) ,断定原子中的绝大部分空间是空的,他的依据是。17. 人类为了揭示原子结构的奥秘,经历了漫长的探究过程。请回答:(1)、汤姆生认为原子是个球体,正电荷均匀分布在整个球体内,而如今这个观点是 (选填“正确”或“错误")的。(2)、卢瑟福提出了原子的核式结构模型,认为原子的全部正电荷和几乎全部的质量都集中。(3)、卢瑟福核式结构模型是利用a粒子轰击金箔实验的基础上提出的。下列能正确反映他的实验结果的示意图是 (选填序号)。 18. 人类对原子结构的认识经历了一个相当长的时期,一代代科学家不断地发现和提出新的原子结构模型。(1)、以下是科学家及其提出的原子结构假设模型(如图所示),其中符合原子结构模型建立先后顺序的是。
18. 人类对原子结构的认识经历了一个相当长的时期,一代代科学家不断地发现和提出新的原子结构模型。(1)、以下是科学家及其提出的原子结构假设模型(如图所示),其中符合原子结构模型建立先后顺序的是。 (2)、1919年科学家卢瑟福用氢原子核轰击氮原子核,结果得到氧、氢两种原子。某学生说:”这是一种生成新物质的变化——化学变化,元素可以通过化学反应来制取。”小柯认为这位学生的说法不正确,其理由是。(3)、2022年4月26日,我国首次国产化碳-14批量生产在中核集团秦山核电站启动。下列模型能表示碳-14 (有6个质子,8个中子)原子结构的是( )A、
(2)、1919年科学家卢瑟福用氢原子核轰击氮原子核,结果得到氧、氢两种原子。某学生说:”这是一种生成新物质的变化——化学变化,元素可以通过化学反应来制取。”小柯认为这位学生的说法不正确,其理由是。(3)、2022年4月26日,我国首次国产化碳-14批量生产在中核集团秦山核电站启动。下列模型能表示碳-14 (有6个质子,8个中子)原子结构的是( )A、 B、
B、 C、
C、 D、
D、 19. 嫦娥五号带回的月球土壤中含有较丰富的氦-3,而在地球上氦元素主要以氦-4的形式存在,如图是它们的原子结构示意图,
19. 嫦娥五号带回的月球土壤中含有较丰富的氦-3,而在地球上氦元素主要以氦-4的形式存在,如图是它们的原子结构示意图,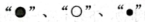 表示原子中的不同微粒。请回答:
表示原子中的不同微粒。请回答:
 (1)、氦-3、氦-4属于同种 , 两者互为同位素;(2)、“O” 表示原子中的(填“质子”“中子”或“电子”)。20. 小明利用12种元素制作了一张如图所示的“元素钟面”。据此请回答:
(1)、氦-3、氦-4属于同种 , 两者互为同位素;(2)、“O” 表示原子中的(填“质子”“中子”或“电子”)。20. 小明利用12种元素制作了一张如图所示的“元素钟面”。据此请回答: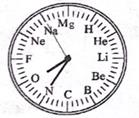 (1)、钟面上的这些元素之间最根本的区别是不同。(2)、此刻钟面上的时针、分针和秒针分别指向三种不同元素,请写出由这三种元素组成的化合物(用化学式表示) 。21. 月球上的“土壤”主要由月球岩石碎屑、粉末等物质组成。太空中长期的太阳风,使得月壤中携带了大量的可作为清洁能源的氦-3,规模总计有100万至500万吨,远远超过了地球的储量。
(1)、钟面上的这些元素之间最根本的区别是不同。(2)、此刻钟面上的时针、分针和秒针分别指向三种不同元素,请写出由这三种元素组成的化合物(用化学式表示) 。21. 月球上的“土壤”主要由月球岩石碎屑、粉末等物质组成。太空中长期的太阳风,使得月壤中携带了大量的可作为清洁能源的氦-3,规模总计有100万至500万吨,远远超过了地球的储量。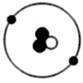 (1)、月壤中岩石碎屑、粉末这些成分相当于地球土壤中的。(“矿物质颗粒”或“腐殖质”)(2)、氦-3是一种氦气同位素气体,其化学符号He,它的核内中子比“正常”氦少一个(如图),氦-3原子内有个电子。22. 在生活、生产中变得越来越重要,氢的同位素原子氘、氚是主要的聚变原料。如图是氢原子的3种同位素原子的结构模型图,它们总称为氢元素,是因为具有的 , 三种微粒中质量最小的是。
(1)、月壤中岩石碎屑、粉末这些成分相当于地球土壤中的。(“矿物质颗粒”或“腐殖质”)(2)、氦-3是一种氦气同位素气体,其化学符号He,它的核内中子比“正常”氦少一个(如图),氦-3原子内有个电子。22. 在生活、生产中变得越来越重要,氢的同位素原子氘、氚是主要的聚变原料。如图是氢原子的3种同位素原子的结构模型图,它们总称为氢元素,是因为具有的 , 三种微粒中质量最小的是。
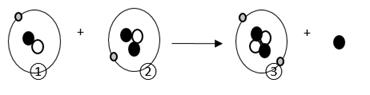
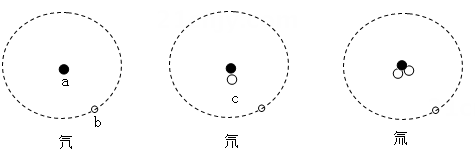 23. 如下图所示,其中①②③表示三种原子,“●”“○”“
23. 如下图所示,其中①②③表示三种原子,“●”“○”“ ”分别表示原子的中子、质子、电子。③是元素的原子;①②③中属于同种元素的原子是(填序号)。
”分别表示原子的中子、质子、电子。③是元素的原子;①②③中属于同种元素的原子是(填序号)。
 24. 当一颗大质量恒星耗尽其自身内部燃料时,它将迎来死亡的时刻,在一次巨大的爆发之后形成每立方厘米的质量达一亿吨的黑洞或中子星。大恒星演变为中子星时,在巨大的压力下,电子会被压缩到原子核内,与(选填“质子或“中子”)电性中和,使原子变得仅由中子组成,原来的原子结构将不复存在,那么发生的这个变化(选填“属于”或“不属于”)化学变化。25. 人类对原子结构的认识,经历了汤姆生、卢瑟福和波尔等提出的模型的过程。
24. 当一颗大质量恒星耗尽其自身内部燃料时,它将迎来死亡的时刻,在一次巨大的爆发之后形成每立方厘米的质量达一亿吨的黑洞或中子星。大恒星演变为中子星时,在巨大的压力下,电子会被压缩到原子核内,与(选填“质子或“中子”)电性中和,使原子变得仅由中子组成,原来的原子结构将不复存在,那么发生的这个变化(选填“属于”或“不属于”)化学变化。25. 人类对原子结构的认识,经历了汤姆生、卢瑟福和波尔等提出的模型的过程。
 (1)、卢瑟福核式结构模型是利用α粒子轰击金箔实验的基础上提出的。下列能正确反映他的实验结果的示意图是 (选填序号)。(2)、从原子结构模型建立的过程中,我们发现 (选填序号) 。A、科学模型的建立是一个不断完善、不断修正的过程 B、模型在科学研究中起着很重要的作用 C、波尔的原子模型建立,使人们对原子结构的认识达到了完美的境界 D、人类借助模型的建立,对原子的认识逐渐接近本质
(1)、卢瑟福核式结构模型是利用α粒子轰击金箔实验的基础上提出的。下列能正确反映他的实验结果的示意图是 (选填序号)。(2)、从原子结构模型建立的过程中,我们发现 (选填序号) 。A、科学模型的建立是一个不断完善、不断修正的过程 B、模型在科学研究中起着很重要的作用 C、波尔的原子模型建立,使人们对原子结构的认识达到了完美的境界 D、人类借助模型的建立,对原子的认识逐渐接近本质三、实验探究题
-
26. 19 世纪以前,人们一直以为原子是不可分的,直到 1887 年,汤姆生发现了带负电的电子后,才引起人们对原子结构模型的探索。1910 年英国科学家卢瑟福进行了著名的α粒子轰击金箔实验。实验做法如图所示:
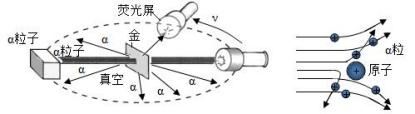
①放射源——放射性物质放出α粒子(带正电荷),质量是电子质量的7000 倍;
②金箔——作为靶子,厚度 1 μm ,重叠了 3000 层左右的原子;
③荧光屏—— α粒子打在上面发出闪光;
④显微镜——通过显微镜观察闪光,且通过360度转动可观察不同角度α粒子的到达情况。
卢瑟福通过实验发现:a.绝大多数α粒子穿过金箔后仍沿原来的方向前进。
b.少数α粒子发生了较大的偏转,并且有极少数α粒子的偏转超过 90°
c.极少数α粒子偏转甚至几乎达到 180°,像是被弹了回来。
(1)、卢瑟福推测“原子内部大部分体积是空的”,支持卢瑟福推测的实验现象是 。(2)、1919年,卢瑟福用加速了的高能α粒子轰击氮原子,结果有种微粒从氮原子中被打出,α粒子留在了氮原子中,使氮原子变成氧原子,从现代观点看,被打出的微粒一定是。27. 为破解原子结构的奥秘,一代又一代科学家进行了不懈探索。1897年,汤姆生提出了一个原子模型:原子是一个球体,正电荷均匀分布在整个球体内,电子像面包里的葡萄干那样镶嵌在其中。
1911年,英国科学家卢瑟福为探索原子的内部结构,用带正电的α粒子轰击金属箔,发现有如下现象:①大多数α粒子能穿透金属箔而不改变原来的运动方向;②有小部分α粒子改变了原来的运动方向;③有极少部分α粒子被弹了回来。
1913年,丹麦科学家波尔改进了卢瑟福的原子核式结构模型,认为电子只能在原子内的一些特定的稳定轨道上运动。
 (1)、卢瑟福的α粒子轰击金属箔实验现象中,能证明原子核带正电的现象是(填序号);(2)、反映卢瑟福α粒子轰击金箔实验结果的示意图最合理的是(填字母);(3)、上述原子结构模型的建立过程,对你有哪些启示?(写出一点即可)。28. 探究原子结构的奥秘:1803年英国科学家道尔顿提出了近代原子学说,他认为一切物质是由原子构成的,这些原子是微小的不可分割的实心球。1911年,英国科学家卢瑟福用一束平行高速运动的α粒子(α粒子是带两个单位正电荷的氦原子)轰击金箔时(金原子的核电荷数为79,相对原子质量为197),发现大多数α粒子能穿透金箔,而且不改变原来的运动方向,但是也有一小部分α粒子改变了原来的运动路径,甚至有极少数的α粒子好像碰到了坚硬不可穿透的质点而被弹了回来。(1)、若原子质量、正电荷在原子内均匀分布,则极少数α粒子就(填“会”或“不会” )发生大角度散射。卢瑟福所说的“极少数的α粒子好像碰到了坚硬不可穿透的质点而被弹了回来的“质点”指的是。(2)、绝大多数α粒子穿过后方向不变,说明 ;(填序号)A、原子的质量是均匀分布的 B、原子内部绝大部分空间是空的(3)、从原子结构模型建立的过程中,我们发现。(选填序号)
(1)、卢瑟福的α粒子轰击金属箔实验现象中,能证明原子核带正电的现象是(填序号);(2)、反映卢瑟福α粒子轰击金箔实验结果的示意图最合理的是(填字母);(3)、上述原子结构模型的建立过程,对你有哪些启示?(写出一点即可)。28. 探究原子结构的奥秘:1803年英国科学家道尔顿提出了近代原子学说,他认为一切物质是由原子构成的,这些原子是微小的不可分割的实心球。1911年,英国科学家卢瑟福用一束平行高速运动的α粒子(α粒子是带两个单位正电荷的氦原子)轰击金箔时(金原子的核电荷数为79,相对原子质量为197),发现大多数α粒子能穿透金箔,而且不改变原来的运动方向,但是也有一小部分α粒子改变了原来的运动路径,甚至有极少数的α粒子好像碰到了坚硬不可穿透的质点而被弹了回来。(1)、若原子质量、正电荷在原子内均匀分布,则极少数α粒子就(填“会”或“不会” )发生大角度散射。卢瑟福所说的“极少数的α粒子好像碰到了坚硬不可穿透的质点而被弹了回来的“质点”指的是。(2)、绝大多数α粒子穿过后方向不变,说明 ;(填序号)A、原子的质量是均匀分布的 B、原子内部绝大部分空间是空的(3)、从原子结构模型建立的过程中,我们发现。(选填序号)a.科学模型的建立是一个不断完善、不断修正的过程
b.模型在科学研究中起着很重要的作用
c.波尔的原子模型建立,使人们对原子结构的认识达到了完美的境界
d.人类借助模型的建立,对原子的认识逐渐接近本质
29. 在 粒子散射实验中,绝大多数 粒子穿过金箔后仍沿原来的方向前进,但是有少数 粒子却发生了较大的偏转,甚至有极少数 粒子偏转几乎达到180°,像是被金箔弹了回来。 粒子遇到电子后,就像飞行的子弹碰到灰尘一样运动方向不会发生明显的改变。卢瑟福推测:除非原子的大部分质量集中到了一个很小的结构上,否则大角度的散射是不可能的。 (1)、支持卢瑟福推测的依据是。(2)、1um金箔包含了3000层金原子,绝大多数 粒子穿过后方向不变,说明______。A、原子的质量是均匀分布的 B、原子内部绝大部分空间是空的(3)、1919年,卢瑟福用加速了的高能a粒子轰击氮原子,结果有种微粒从氮原子被打出,而 粒子留在了氮原子中,使氮原子变成了氧原子,从现代观点看,被打出的微粒是。30. 1910年英国科学家卢瑟福进行了著名的α粒子轰击金箔实验。实验做法如图:
(1)、支持卢瑟福推测的依据是。(2)、1um金箔包含了3000层金原子,绝大多数 粒子穿过后方向不变,说明______。A、原子的质量是均匀分布的 B、原子内部绝大部分空间是空的(3)、1919年,卢瑟福用加速了的高能a粒子轰击氮原子,结果有种微粒从氮原子被打出,而 粒子留在了氮原子中,使氮原子变成了氧原子,从现代观点看,被打出的微粒是。30. 1910年英国科学家卢瑟福进行了著名的α粒子轰击金箔实验。实验做法如图: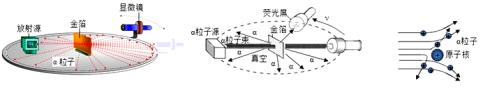
绝大多数α粒子穿过金箔后仍沿原来的方向前进,但是有少数α粒子却发生了较大的偏转,并且有极少数α粒子的偏转超过90°,有的甚至几乎达到180°,像是被金箔弹了回来。
【猜想与假设】α粒子遇到电子后,就像飞行的子弹碰到灰尘一样运动方向不会发生明显的改变,而结果却出乎意料,除非原子的大部分质量集中到了一个很小的结构上,否则大角度的散射是不可能的。
【解释与结论】
(1)、大多数 α 粒子不改变原来的运动方向,原因是 。(2)、卢瑟福所说的“除非原子的大部分质量集中到了一个很小的结构”中的“很小的结构” 指的是 。(3)、科学家对原子结构的探究经历了三个过程,通过 α 粒子散射实验,你认为原子结构为 右图的 。
四、解答题
-
31. 人类对原子结构的认识,经历了汤姆生、卢瑟福和波尔等提出的模型的过程。根据所学完成下列有关问题。(1)、汤姆生最早发现了原子中存在一种带 负电荷的粒子,证明了原子是可以再分的,汤姆生发现的这一粒子是。(2)、卢瑟福提出核式结构模型,他认为在原子的中心有一个很小的原子核,原子的全部正电荷和几乎全部的质量都集中在原子核里,上述结论是卢瑟福在用a粒子(由两个中子和两个质子构成)轰击金箔实验的基础上提出的,如图为该实验示意图。请简要说明图中哪些现象可以作为支持卢瑟福核式结构模型的证据。。
 (3)、从原子结构模型建立的过程中,我们发现(可多选)
(3)、从原子结构模型建立的过程中,我们发现(可多选)A.科学模型的建立是一个不断完善、不断修正的过程。
B.模型在科学研究中起着很重要的作用。
C.波尔的原子模型建立,使人们对原子结构的认识达到了完美的境界。
D.人类借助模型的建立,对原子的认识逐渐接近本质。
32. 人类对微观世界的探究永无止境。请根据所学知识回答:(1)、道尔顿最早提出原子的概念并认为原子是“不可再分的实心球体”,1897年汤姆生发现电子并提出类似“西瓜”的原子模型,认为电子就像“西瓜子”一样镶嵌在带正电荷的“西瓜瓤”中,如今这些观点均是(选填“正确”“错误”)的。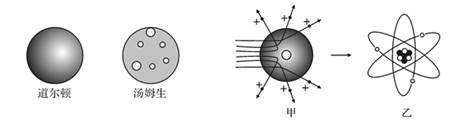 (2)、卢瑟福进行α粒子散射实验后,认为原子是“行星模型”,即原子是由带电荷的原子核和核外电子构成。如图甲是卢瑟福用α粒子轰击原子而产生散射的实验,在分析实验结果的基础上,他提出了图乙所示的原子核式结构,卢瑟福的这一研究过程是一个。
(2)、卢瑟福进行α粒子散射实验后,认为原子是“行星模型”,即原子是由带电荷的原子核和核外电子构成。如图甲是卢瑟福用α粒子轰击原子而产生散射的实验,在分析实验结果的基础上,他提出了图乙所示的原子核式结构,卢瑟福的这一研究过程是一个。A.建立模型的过程 B.得出结论的过程 C.提出问题的过程 D.验证证据的过程
(3)、卢瑟福在α散射实验中(α粒子带正电荷),断定原子中的绝大部分空间是空的,他的依据是。(4)、据报道,中国科学家利用超强超短激光,成功提取出反物质一一超快正电子源,“反物质”是由“反粒子”构成的,“反粒子”与其对应的正粒子具有相同的质量与电量,但电性相反,已知α粒子是带2个正电荷的氦原子核 ,则反α粒子的符号可表示为。33. 为探究原子的结构,1911年英国科学家卢瑟福进行了著名的α粒子轰击金箔实验。(1)、卢瑟福说“原子的大部分质量集中到了一个很小的结构上”这里的“很小的结构”指的是;(2)、图甲为α粒子轰击金箔时的运动轨迹,请在图甲中补全A处α粒子的后半段大致运动轨迹。 (3)、根据α粒子散射实验数据,统计不同偏转角度的α粒子数量,绘制图像如图乙所示。能说明原子 内部绝大部分是空的数据是(用图乙中的字母表示)段曲线;34. 1910年英国科学家卢瑟福进行了著名的α粒子轰击金箔实验。实验结果发现:绝大多数α粒子仍沿原来方向前进,有少数发生了偏转,并且极少数α粒子的偏转超过90°,甚至几乎达到180°像是被金箔弹了回来。(1)、若原子内质量、正电荷分布均匀,则极少数α粒子(填“会”或“不会”)发生大角度散射。卢瑟福所说的“原子的绝大部分质量集中到了一个很小的结构上”,这个“很小的结构”指的是。(2)、1μm金箔包含了3000层金原子,绝大多数α粒子穿过后方向不变说明 (填字母,下同)。A、原子的质量是均匀分布的 B、原子内部绝大部分空间是空的(3)、科学家对原子结构的探究经历了三个过程,通过α粒子散射实验,你认为原子结构为以下的。
(3)、根据α粒子散射实验数据,统计不同偏转角度的α粒子数量,绘制图像如图乙所示。能说明原子 内部绝大部分是空的数据是(用图乙中的字母表示)段曲线;34. 1910年英国科学家卢瑟福进行了著名的α粒子轰击金箔实验。实验结果发现:绝大多数α粒子仍沿原来方向前进,有少数发生了偏转,并且极少数α粒子的偏转超过90°,甚至几乎达到180°像是被金箔弹了回来。(1)、若原子内质量、正电荷分布均匀,则极少数α粒子(填“会”或“不会”)发生大角度散射。卢瑟福所说的“原子的绝大部分质量集中到了一个很小的结构上”,这个“很小的结构”指的是。(2)、1μm金箔包含了3000层金原子,绝大多数α粒子穿过后方向不变说明 (填字母,下同)。A、原子的质量是均匀分布的 B、原子内部绝大部分空间是空的(3)、科学家对原子结构的探究经历了三个过程,通过α粒子散射实验,你认为原子结构为以下的。 35. 人类对原子结构的认识,经历了汤姆生、卢瑟福和波尔等提出的模型的过程。根据所学完成下列有关问题。(1)、汤姆生最早发现了原子中存在一种带 负电荷的粒子,证明了原子是可以再分的,汤姆生发现的这一粒子是。(2)、卢瑟福提出核式结构模型,他认为在原子的中心有一个很小的原子核,原子的全部正电荷和几乎全部的质量都集中在原子核里,上述结论是卢瑟福在用a粒子(由两个中子和两个质子构成)轰击金箔实验的基础上提出的,如图为该实验示意图。请简要说明图中哪些现象可以作为支持卢瑟福核式结构模型的证据。。
35. 人类对原子结构的认识,经历了汤姆生、卢瑟福和波尔等提出的模型的过程。根据所学完成下列有关问题。(1)、汤姆生最早发现了原子中存在一种带 负电荷的粒子,证明了原子是可以再分的,汤姆生发现的这一粒子是。(2)、卢瑟福提出核式结构模型,他认为在原子的中心有一个很小的原子核,原子的全部正电荷和几乎全部的质量都集中在原子核里,上述结论是卢瑟福在用a粒子(由两个中子和两个质子构成)轰击金箔实验的基础上提出的,如图为该实验示意图。请简要说明图中哪些现象可以作为支持卢瑟福核式结构模型的证据。。 (3)、从原子结构模型建立的过程中,我们发现 (可多选)A、科学模型的建立是一个不断完善、不断修正的过程。 B、模型在科学研究中起着很重要的作用。 C、波尔的原子模型建立,使人们对原子结构的认识达到了完美的境界。 D、人类借助模型的建立,对原子的认识逐渐接近本质。
(3)、从原子结构模型建立的过程中,我们发现 (可多选)A、科学模型的建立是一个不断完善、不断修正的过程。 B、模型在科学研究中起着很重要的作用。 C、波尔的原子模型建立,使人们对原子结构的认识达到了完美的境界。 D、人类借助模型的建立,对原子的认识逐渐接近本质。