辽宁省葫芦岛市协作校2022-2023学年高三上学期第二次考试化学试题
试卷更新日期:2023-01-03 类型:月考试卷
一、单选题
-
1. 化学与生产、生活、科技等密切相关。下列说法正确的是( )A、离子交换法适宜软化硬水(指含有较多可溶性钙镁化合物的水) B、苏打水呈弱酸性,能中和胃酸,有助于平衡人体内的酸碱度 C、我国山水画所用的炭黑与卫星所用的碳纤维互为同位素 D、我国出土的青铜器是由铁和铜的合金制成的器具2. 下列有关化学用语表述错误的是( )A、的电子式为
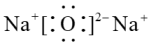 B、
B、 的系统命名为2,2-二甲基丁烷
C、基态铍原子最外层电子的电子云轮廓图为
的系统命名为2,2-二甲基丁烷
C、基态铍原子最外层电子的电子云轮廓图为 D、基态氮原子核外电子排布的轨道表示式为
D、基态氮原子核外电子排布的轨道表示式为 3. 根据图示合成路线分析,下列有关说法错误的是( )
3. 根据图示合成路线分析,下列有关说法错误的是( ) A、a中所有原子不可能共面 B、b中含有一种官能团 C、c的分子式为 D、d的一氯代物有两种4. 根据下列装置和物质,能达到相应实验目的的是( )
A、a中所有原子不可能共面 B、b中含有一种官能团 C、c的分子式为 D、d的一氯代物有两种4. 根据下列装置和物质,能达到相应实验目的的是( )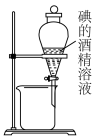
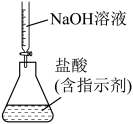


A.分离碘和酒精
B.进行酸碱中和滴定
C.制备并收集
D.制备
A、A B、B C、C D、D5. 下列叙述正确的是( )A、晶体的沸点高于 , 是因为中共价键的键能小于 B、基态原子轨道半充满的元素一定位于第ⅠA族和第ⅠB族 C、元素位于第四周期第ⅥA族,属于p区元素 D、非极性分子往往具有高度对你性,如、、、6. 离子交换法净化水的过程如图所示。下列说法中正确的是( ) A、通过净化处理后,水的导电性保持不变 B、经过阳离子交换树脂后,水中阳离子的种类不变 C、水中的通过阴离子交换树脂后除去 D、阴离子交换树脂中发生了中和反应7. 下列关于常见金属单质的说法中错误的是( )A、金属钠着火不能使用泡沫灭火器灭火,而应该使用干燥的沙土灭火 B、铝合金制品因密度小、强度高且具有较强的抗腐蚀能力而被广泛应用 C、除去Cu粉中混有的CuO,可加入稀硫酸溶解后过滤、洗涤、干燥 D、铁与稀硝酸、稀硫酸反应均有气泡产生,说明铁与两种酸均发生了置换反应8. 下列实验对应的离子方程式正确的是( )A、溶液刻蚀电路板: B、明矾溶液与过量氨水混合: C、用二氧化硫的水溶液吸收溴蒸气: D、用碳酸钠溶液处理水垢中的硫酸钙:9. 为阿伏加德罗常数的值。下列叙述正确的是( )A、标准状况下,中含有C—Cl键的数目为 B、溴化铵水溶液中与的数目之和大于 C、14g聚丙烯中含有的原子总数为 D、3与完全反应时转移的电子数为10. 配位化合物广泛应用于物质分离、定量测定、医药、催化等方面。利用氧化法可制备某些配位化合物,如。设是阿伏加德罗常数的值,下列叙述正确的是( )A、中含有键的数目为 B、的溶液中,的数目为 C、与足量在催化剂作用下合成氨,生成的分子数为 D、质量分数为的溶液中,氧原子总数为11. W、X、Y、Z为原子序数依次增大的短周期主族元素。已知:W、X、Z三种元素在元素周期表中的相对位置如图所示,且常温下W和Z常见单质的状态不同,Y的原子半径在短周期主族元素中是最大的。下列说法正确的是( )
A、通过净化处理后,水的导电性保持不变 B、经过阳离子交换树脂后,水中阳离子的种类不变 C、水中的通过阴离子交换树脂后除去 D、阴离子交换树脂中发生了中和反应7. 下列关于常见金属单质的说法中错误的是( )A、金属钠着火不能使用泡沫灭火器灭火,而应该使用干燥的沙土灭火 B、铝合金制品因密度小、强度高且具有较强的抗腐蚀能力而被广泛应用 C、除去Cu粉中混有的CuO,可加入稀硫酸溶解后过滤、洗涤、干燥 D、铁与稀硝酸、稀硫酸反应均有气泡产生,说明铁与两种酸均发生了置换反应8. 下列实验对应的离子方程式正确的是( )A、溶液刻蚀电路板: B、明矾溶液与过量氨水混合: C、用二氧化硫的水溶液吸收溴蒸气: D、用碳酸钠溶液处理水垢中的硫酸钙:9. 为阿伏加德罗常数的值。下列叙述正确的是( )A、标准状况下,中含有C—Cl键的数目为 B、溴化铵水溶液中与的数目之和大于 C、14g聚丙烯中含有的原子总数为 D、3与完全反应时转移的电子数为10. 配位化合物广泛应用于物质分离、定量测定、医药、催化等方面。利用氧化法可制备某些配位化合物,如。设是阿伏加德罗常数的值,下列叙述正确的是( )A、中含有键的数目为 B、的溶液中,的数目为 C、与足量在催化剂作用下合成氨,生成的分子数为 D、质量分数为的溶液中,氧原子总数为11. W、X、Y、Z为原子序数依次增大的短周期主族元素。已知:W、X、Z三种元素在元素周期表中的相对位置如图所示,且常温下W和Z常见单质的状态不同,Y的原子半径在短周期主族元素中是最大的。下列说法正确的是( )W
X
Z
A、W、X、Z三种元素中电负性最大的是Z B、四种元素的简单离子的半径由大到小的顺序为 C、可与反应生成和 D、W和Z的最高价氧化物对应的水化物均为强酸12. 根据下列实验现象和有关数据,推断错误的是( ) A、原混合物中含0.03molCuO B、白色沉淀M为CuI C、CCl4和I2都是非极性分子 D、气体R分子是V形分子13. 砷化硼的晶胞结构如图所示,晶胞的边长为 , 下列说法中正确的是( )
A、原混合物中含0.03molCuO B、白色沉淀M为CuI C、CCl4和I2都是非极性分子 D、气体R分子是V形分子13. 砷化硼的晶胞结构如图所示,晶胞的边长为 , 下列说法中正确的是( ) A、砷化硼的化学式为 B、砷化硼晶胞中,的配位数是4 C、砷化硼晶胞中,原子之间的最短距离为 D、晶体的密度为14. 由下列实验操作及现象得出的结论正确的是( )
A、砷化硼的化学式为 B、砷化硼晶胞中,的配位数是4 C、砷化硼晶胞中,原子之间的最短距离为 D、晶体的密度为14. 由下列实验操作及现象得出的结论正确的是( )选项
实验操作
现象
结论
A
取溶液于试管中,加入溶液,充分反应后滴入5滴15%KSCN溶液
溶液变血红色
KI与的反应有一定限度
B
向溶液X中滴加少量NaOH稀溶液,将湿润的红色石蕊试纸靠近试管口
石蕊试纸不变蓝
溶液X中肯定不含
C
将硫酸酸化的溶液滴入溶液中
溶液变黄色
氧化性:(酸性条件)
D
向一定浓度的溶液中通入适量气体
产生黑色沉淀
的酸性比的强
A、A B、B C、C D、D二、多选题
-
15. 氮化钙是高端荧光粉的主要成分之一,极易与水反应生成氨气。利用如图装置测定一定质量的氮化钙产品的纯度(杂质只有氮化钠,氨不溶于煤油)。下列说法正确的是( )
 A、上下移动水准瓶,量气管与水准瓶内液面不发生变化,说明气密性良好 B、若Y形管内残留有反应产生的气体,则会影响测定结果 C、反应结束,装置冷却至室温后,量气管(与滴定管类似)的读数越大,产品的纯度越高 D、反应结束,装置冷却至室温后,未调整水准瓶的液面高度即读数,会造成结果偏低
A、上下移动水准瓶,量气管与水准瓶内液面不发生变化,说明气密性良好 B、若Y形管内残留有反应产生的气体,则会影响测定结果 C、反应结束,装置冷却至室温后,量气管(与滴定管类似)的读数越大,产品的纯度越高 D、反应结束,装置冷却至室温后,未调整水准瓶的液面高度即读数,会造成结果偏低三、综合题
-
16. 已知是一种易溶于水的白色或微红色晶体。某化学兴趣小组利用如图所示装置(夹持及加热装置省路)米制备该晶体。已知:多孔球泡能增大气体与液体的接触面积。
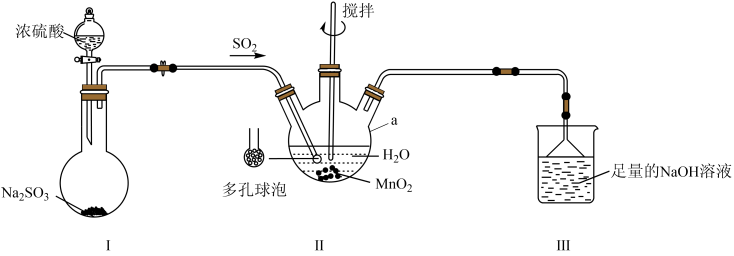 (1)、仪器a名称为 , 图中为了提高装置B中的反应速率采取了的措施有(填两条)。(2)、分液漏斗在使用前需检查。(3)、装置A中发生反应的化学方程式为。(4)、装置B中发生反应的氧化剂和还原剂的物质的量之比:n(氧化剂):(还原剂)= , 从反应后的溶液中得到的操作为过滤、、、过滤、洗涤、干燥。(5)、装置C中倒置漏斗的作用为 , 用离子方程式表示装置C中溶液的作用:。17. 一种以废旧钴酸锂电池材料(主要成分为LiCoO2 , 含单质及为改善电池性能添加的单质等)为原料回收钴酸锂的工艺流程如下:
(1)、仪器a名称为 , 图中为了提高装置B中的反应速率采取了的措施有(填两条)。(2)、分液漏斗在使用前需检查。(3)、装置A中发生反应的化学方程式为。(4)、装置B中发生反应的氧化剂和还原剂的物质的量之比:n(氧化剂):(还原剂)= , 从反应后的溶液中得到的操作为过滤、、、过滤、洗涤、干燥。(5)、装置C中倒置漏斗的作用为 , 用离子方程式表示装置C中溶液的作用:。17. 一种以废旧钴酸锂电池材料(主要成分为LiCoO2 , 含单质及为改善电池性能添加的单质等)为原料回收钴酸锂的工艺流程如下:
回答下列问题:
(1)、废旧钴酸锂电池需经放电,拆解后,再经“碱浸”处理,为提高碱浸速率,可采取的措施有(任写一点)。(2)、“碱浸”所得滤液中含有的阴离子为。(3)、“酸浸”时作还原剂,还原产物为 , 反应的离子方程式为;在“酸浸”过程中,由于有的加入,铜也可以被氧化浸出,写出铜被浸出的化学方程式:。(4)、“萃取铜”中的有机萃取剂用表示,发生的萃取反应可表示为。若“酸浸”后的浸取液。多次萃取后水相中为 , 则铜的萃取率为(水相溶液体积变化忽略,保留小数点后两位);为回收铜,可用一定浓度的将“有机相”中的铜反萃取到水相中,其原理是。(5)、“钴、锂共沉淀”时析出和经过滤、无水乙醇洗涤、干燥后在煅烧,反应的化学方程式为。18. 配合物在光电传感器、电镀、染料方面有着重要的应用价值,一氧化碳、氨气、酞菁分子是常见形成配合物的三种配位体,请回答下列问题:(1)、一氧化碳和氨气涉及的元素中电负性最大的是(填元素符号)。(2)、邻苯二甲酸酐( )和邻苯二甲酰亚胺(
)和邻苯二甲酰亚胺(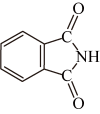 )都是合成酞菁的原料,熔点较高的是(填化学式),原因为。 (3)、和可形成配离子 , 则该配离子的空间结构为。(4)、能与形成配合物。
)都是合成酞菁的原料,熔点较高的是(填化学式),原因为。 (3)、和可形成配离子 , 则该配离子的空间结构为。(4)、能与形成配合物。①中含有键;中心原子的杂化类型为。
②金属的原子堆积模型如图,则金属的晶胞俯视图为(填标号),假设原子的半径是 , 该晶体的密度是 , 则的相对原子质量为(设为阿伏加德罗常数的值)。
 19. 黑色金属材料是工业上对铁、铬、锰的统称,、、及其化合物在日常生活生产中的用途相当广泛。(1)、Ⅰ. 根据所学知识,回答下列问题:
19. 黑色金属材料是工业上对铁、铬、锰的统称,、、及其化合物在日常生活生产中的用途相当广泛。(1)、Ⅰ. 根据所学知识,回答下列问题:具有净水作用,净水的原理是。
(2)、向溶液中加入溶液至过量,微热。再通入 , 可观察到溶液呈紫色(高铁酸钾:)。写出此过程发生反应的离子方程式:。(3)、可用于治疗缺铁性贫血症,为验证药品的还原性,某实验小组取少量药用配制成溶液,并取溶液于试管中,滴入几滴浓硝酸,振荡,试管中产生红棕色气体,溶液变为深棕色。为探究溶液没有变为黄色的原因补充了如下实验:向溶液和溶液中分别通入 , 观察到溶液变为深棕色,溶液无明显变化。①“试管中产生红棕色气体,溶液变为深棕色”的原因是。
②实验小组改进实验,观察到溶液变为黄色的实验操作是。
(4)、Ⅱ.在溶液中存在下列平衡:。下列有关溶液的说法正确的是____(填标号)。
A、加入少量硫酸,溶液的橙色加深 B、加入少量水稀释,溶液中离子总数增加 C、入少量溶液,平衡逆向移动 D、加入少量固体,平衡正向移动,转化率变大(5)、Ⅲ.可用作电讯器材元件材料。还可用作瓷釉、颜料及制造锰盐的原料。它在空气中加热易转化为不同价态锰的氧化物,其固体残留率()随温度的变化如图所示。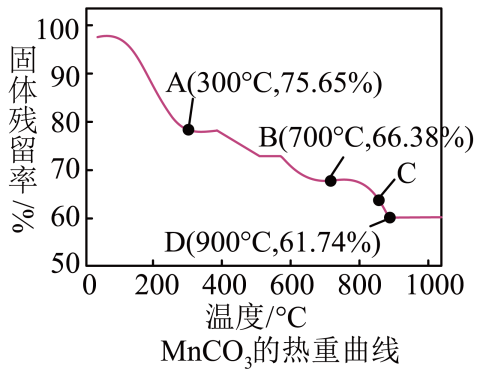
时,剩余固体中为。
(6)、图中C点对应固体的成分为(填化学式)。
-