2022-2023初中化学下学期第八单元金属和金属材料 实验活动4 金属的物理性质和某些化学性质 课堂训练
试卷更新日期:2022-12-24 类型:同步测试
一、单选题
-
1. 将某稀盐酸分成两等份,分别向其中加入30g锌粉和30g铁粉,反应结束后剩余的铁比剩余的锌多,产生氢气分别为ag和bg,则a和b的关系是( )A、a<b B、a>b C、a=b D、无法判断2. 下列物质中,不能用稀硫酸和金属反应直接制得的是( )A、硫酸锌 B、硫酸铁 C、硫酸铝 D、硫酸镁3. 现将X、Y两种金属片分别插入硫酸铜溶液中,X无明显变化,Y表面有铜析出,则X、Y、Cu三种金属的活动性由强到弱的顺序是( )A、X>Y>Cu B、Cu>X>Y C、Y>Cu>X D、X>Cu> Y4. 菜刀用铁制而不用铝制的主要原因是( )。A、铁的硬度大,铝的硬度小 B、铁的熔点高,铝的熔点低 C、铁的密度大,铝的密度小 D、铁的导电性差,铝的导电性好5. 下列关于合金的说法正确的是( )。A、合金属于化合物 B、合金不能导电、导热 C、合金没有延展性 D、合金的许多性能与组成它们的纯金属不同6. 等质量等浓度的稀硫酸分别与足量的镁、铁、锌三种金属反应,下列图像能正确表示产生氢气质量与反应时间之间关系的是( )A、
 B、
B、 C、
C、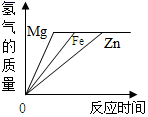 D、
D、 7. 某同学为了验证铁、锌、铜三种金属的活动性顺序,设计了下列四种方案,其中一定能达到实验目的是( )A、将锌粒、铜片分别加入到FeSO4溶液中 B、将锌粒、铜片分别加入到ZnSO4溶液中 C、将锌粒分别加入到FeSO4、CuSO4溶液中 D、将锌粒、铁粉、铜片分别加入到稀硫酸中8. 已知金属锰在金属活动性顺序中位于铝和锌之间。下列化学反应不能发生的是( )A、Mn+H2SO4=MnSO4+H2↑ B、Mg+MnCl2=MgCl2+Mn C、Fe+MnCl2=MgCl2+Mn D、Mn+CuCl2=MnCl2+Cu9. 验证Zn、Fe、Cu金属的活动性强弱,下列的试剂组合实验方案不能达到实验目的是( )A、FeCl2 溶液、Zn、Cu B、ZnSO4溶液、稀盐酸溶液,Fe、Cu C、ZnSO4溶液、CuSO4溶液、Fe D、CuCl2溶液、Zn、Fe10. X、Y、Z、R四种金属与盐酸反应的情况如右图所示,其中一种金属的盐溶液能跟其余三种金属发生置换反应,这种金属是( )
7. 某同学为了验证铁、锌、铜三种金属的活动性顺序,设计了下列四种方案,其中一定能达到实验目的是( )A、将锌粒、铜片分别加入到FeSO4溶液中 B、将锌粒、铜片分别加入到ZnSO4溶液中 C、将锌粒分别加入到FeSO4、CuSO4溶液中 D、将锌粒、铁粉、铜片分别加入到稀硫酸中8. 已知金属锰在金属活动性顺序中位于铝和锌之间。下列化学反应不能发生的是( )A、Mn+H2SO4=MnSO4+H2↑ B、Mg+MnCl2=MgCl2+Mn C、Fe+MnCl2=MgCl2+Mn D、Mn+CuCl2=MnCl2+Cu9. 验证Zn、Fe、Cu金属的活动性强弱,下列的试剂组合实验方案不能达到实验目的是( )A、FeCl2 溶液、Zn、Cu B、ZnSO4溶液、稀盐酸溶液,Fe、Cu C、ZnSO4溶液、CuSO4溶液、Fe D、CuCl2溶液、Zn、Fe10. X、Y、Z、R四种金属与盐酸反应的情况如右图所示,其中一种金属的盐溶液能跟其余三种金属发生置换反应,这种金属是( ) A、X B、Y C、Z D、R
A、X B、Y C、Z D、R二、填空题
-
11. 请回答有关金属的问题。(1)、在Cu和Zn中,活动性较强的是;(2)、Cu与AgNO3溶液的反应中,离子变成了原子;(3)、只用少量的盐酸、一支试管和锌、铜、铝,通过加入金属的顺序不同,也能验证这三种金属的活动性的强弱,则加入的顺序为(假设每次的反应均反应完全)。12. 厉害了我的国!厉害了复兴号!复兴号动车组列车是由中国铁路总公司牵头组织研制、具有完全自主知识产权、达到世界先进水平的动车组列车。(1)、制造列车使用了大量的铝合金材料,铝合金的硬度比纯铝的硬度;在空气中,铝制品耐腐蚀的原因是。(2)、列车轨道建设中常用铝和氧化铁(化学式为Fe2O3)在高温条件下发生反应,生成熔融状态下的铁单质对钢轨中的缝隙进行焊接。其反应的化学方程式为:Fe2O3+2Al X+2Fe,则X的化学式为 , 该反应属于 (填“置换”或“化合”)反应。13. 对于下列金属:铝、铜、锌、钛、铁、钙.
①可用来冶炼高熔点得金属是 .
②可用于制干电池的是 .
③白铁表面所镀的金属是 .
④广泛用于制电线、电缆的是 .
⑤广泛应用于航空工业、制造工业的是 .
14. 含有硝酸锌、硝酸铁、硝酸镁、硝酸铜、硝酸银五种溶质的溶液中加入一定量的铁粉,充分反应后过滤,滤纸上一定有 , 可能有;滤液中一定有 , 可能有;如果滤纸上有铁,则滤纸上一定同时有 , 滤液中一定没有 .15. 在Cu(NO3)2和Zn(NO3)2的混合溶液中加入一定量的铁粉,充分反应后过滤,向滤出的固体中滴加稀硫酸,有气泡产生,则滤出的固体中一定含有 , 滤液中一定含有的物质的化学式为。上述过程中所发生有关反应的化学方程式为。(写出一个即可)三、简答题
-
16. 请你设计化学实验,用两种不同的方案(不同的化学试剂)验证:镁、铁、铜的金属活动性.17. 黄金饰品中的假货常常鱼目混珠,单纯从颜色,外形看与真黄金无多大差异.因为一些不法分子选择的是黄铜(铜锌合金,金黄色,铜和锌保持各自单质的化学性质)假冒黄金进行诈骗活动.现请你设计一实验,证明某金黄色金属块是真金还是黄铜,要求写出实验的方法、现象和结论.
四、综合题
-
18. 结合验证铁、铜、银活动性的实验,回答下列问题:(1)、将铜丝和铁丝分别放入相同的浓度的稀H2SO4中,依据现象,可以判断Fe的活动性比Cu强;(2)、将铜丝放入AgNO3溶液中,Cu与AgNO3溶液反应的化学方程式为;(3)、铝比铁活泼,但铝比铁的耐腐蚀性强,原因是。(4)、向AgNO3和Cu(NO3)2的混合溶液中加入一定量的Zn粉,充分反应后过滤,向滤渣中加盐酸有气泡,则滤渣中一定含有的金属是。
五、实验探究题
-
19. 在研究“铁生锈的条件”的实验中,某兴趣小组对实验进行了创新设计,请把实验报告补充完整.
【实验目的】铁生锈条件的探究.
【实验内容】取3段光亮无锈的细铁丝,绕成螺旋状,放入3支干燥洁净的试管底部,进行下列实验,实验要保证有足够长的时间来观察现象

【实验现象】实验①②无明显现象,实验③中铁丝生锈,且试管内空气体积减小.
(1)、【实验结论】铁生锈实际上是铁与空气中的(填名称)发生反应的结果.【实验思考】
当铁丝足量,时间足够长,实验③进入试管内的水的体积约占试管体积的 .
(2)、该实验创新之处在于:可根据铁丝表面的铁锈和两种现象来判断铁丝反应进行的情况.(3)、用完的菜刀要擦干存放,理由是 .(4)、铝比铁活泼,但铝难腐蚀,原因是 .20. 铝、铁、铜是生活中常见的金属。(1)、铝、铁、铜三种金属都能作导线,是因为它们都具有。(2)、铝在空气中不易被锈蚀,是因为 用化学方程式表示 。(3)、铜锈的主要成分为碱式碳酸铜Cu2(OH)2CO3 , 由此我们可以得到铜生锈是铜和氧气、水、共同作用的结果。(4)、某同学用如图所示装置,设计实验验证铝、铁、铜三种金属活动性强弱。 每步反应金属均有剩余 若甲试管中无明显现象,乙试管中的金属b为时可以验证三种金属活动性强弱,丙试管中反应的化学方程式为若金属a、b、c依次为铁、铝、铜时,则无法比较和的活动性强弱。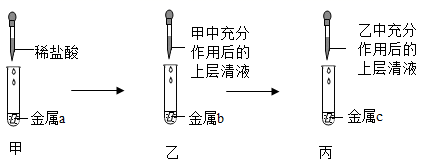
-