浙教版科学中考 物质科学-空气选择专项
试卷更新日期:2022-12-20 类型:二轮复习
一、单选题
-
1. 烧杯中盛放有一定量的硝酸银和硝酸亚铁的混合溶液,现向溶液中缓缓加入锌粉,经搅拌使其与溶液中的溶质恰好完全反应。现以加入锌粉的质量为横坐标,以烧杯中生成的固体质量为纵坐标,甲、乙、丙三位同学分别作出了烧杯中的固体质量随加入的锌粉质量变化的大致关系图。其中A点表示锌粉与溶液中的溶质恰好完全反应时的质量。下列说法正确的是( )

 A、线段BC表示锌与硝酸银反应 B、反应结束时,三种情况的溶液溶质种类不同 C、乙图中表示与硝酸银和硝酸亚铁反应的锌的质量之比是 D、甲图表示反应结束时,参加反应的锌的质量大于生成的银和铁的质量总和2. 在“欢迎来找茬”的趣味活动中,老师举出四个错误实例,在学生的错因分析中错误的是( )
A、线段BC表示锌与硝酸银反应 B、反应结束时,三种情况的溶液溶质种类不同 C、乙图中表示与硝酸银和硝酸亚铁反应的锌的质量之比是 D、甲图表示反应结束时,参加反应的锌的质量大于生成的银和铁的质量总和2. 在“欢迎来找茬”的趣味活动中,老师举出四个错误实例,在学生的错因分析中错误的是( )序号
错误实例
错因分析
A
铁与稀硫酸反应生成硫酸铁
反应产物不正确
B
SO2+NaOH=Na2SO4+H2O
只缺少沉淀符号
C
Fe+S=FeS
反应条件不正确
D
氢氧化钠俗名烧碱或纯碱
俗名纯碱不正确
A、A B、B C、C D、D3. 向氢氧化钡溶液中逐滴加入稀硫酸,某个量y 随加入稀硫酸体积的变化情况如图所示,则 y表示( ) A、沉淀的质量 B、氢氧化钡的质量 C、溶液的 pH D、溶质的质量4. 下列事实与相应化学方程式书写均正确的是( )A、鉴别稀硫酸和稀盐酸一般可用AgNO3溶液:AgNO3+HCl=AgCl↓+HNO3 B、金属铝的表面易生成一层致密的保护膜:4Al+3O2=2Al2O3 C、工业炼铁常采用CO作为还原剂:Fe2O3+3CO2Fe+3CO2 D、使用Ca(OH)2治疗胃酸过多症:Ca(OH)2+2HCl=CaCl2+2H2O5. 下列关于质量守恒定律的理解,错误的是( )A、1g氢气和1g氧气反应能生成2g水 B、反应前后原子种类和个数不变 C、实际参加反应的反应物总质量等于生成物总质量 D、煤燃烧后灰渣质量小于煤,也能用质量守恒定律解释6. 将一定质量的a、b、c、d四种物质放入一密闭容器中在一定条件下反应,测得反应前后各物质的质量如下表所示,以下说法正确的是( )
A、沉淀的质量 B、氢氧化钡的质量 C、溶液的 pH D、溶质的质量4. 下列事实与相应化学方程式书写均正确的是( )A、鉴别稀硫酸和稀盐酸一般可用AgNO3溶液:AgNO3+HCl=AgCl↓+HNO3 B、金属铝的表面易生成一层致密的保护膜:4Al+3O2=2Al2O3 C、工业炼铁常采用CO作为还原剂:Fe2O3+3CO2Fe+3CO2 D、使用Ca(OH)2治疗胃酸过多症:Ca(OH)2+2HCl=CaCl2+2H2O5. 下列关于质量守恒定律的理解,错误的是( )A、1g氢气和1g氧气反应能生成2g水 B、反应前后原子种类和个数不变 C、实际参加反应的反应物总质量等于生成物总质量 D、煤燃烧后灰渣质量小于煤,也能用质量守恒定律解释6. 将一定质量的a、b、c、d四种物质放入一密闭容器中在一定条件下反应,测得反应前后各物质的质量如下表所示,以下说法正确的是( )物质
a
b
C
d
反应前质量/g
6.4
3.0
4.0
2.0
反应后质量/g
3.2
X
8.8
2.0
A、d一定是该反应的催化剂 B、此反应的基本反应类型是分解反应。 C、X的值为1.6 D、若继续反应至b反应完全,则此时反应后a的剩余质量为0.4g7. 将等质量的镁和铁分别放入左右试管中,加入等质量分数的稀盐酸,充分反应后,冷却到室温,金属均没有剩余(U形管内为水,初始液面相平,反应过程中装置气密性良好)。下列说法正确的是( ) A、U形管中液面一直保持相平 B、两支试管中所得溶液的质量相等 C、U形管中液面最终情况为左降右升 D、依据U形管中最终液面的高低可判断金属的活动性强弱8. 下列图像能正确反映对应变化关系的是( )A、
A、U形管中液面一直保持相平 B、两支试管中所得溶液的质量相等 C、U形管中液面最终情况为左降右升 D、依据U形管中最终液面的高低可判断金属的活动性强弱8. 下列图像能正确反映对应变化关系的是( )A、 室温下,相同质量的锌和铁分别与足量的溶质质分数相同的稀硫酸反应
B、
室温下,相同质量的锌和铁分别与足量的溶质质分数相同的稀硫酸反应
B、 向一定量的氢氧化钠溶液中滴加pH=3的稀盐酸
C、
向一定量的氢氧化钠溶液中滴加pH=3的稀盐酸
C、 一定温度时,向一定量的饱和石灰水中加入生石灰
D、
一定温度时,向一定量的饱和石灰水中加入生石灰
D、 向一定量的NaOH和Ba(NO3)2溶液中逐滴加入稀H2SO4
9. 如图所示是磷与氧气反应前后的微观模型图(●表示磷原子,〇表示氧原子),根据质量守恒定律,则虚线框中的微观模型应该是( )
向一定量的NaOH和Ba(NO3)2溶液中逐滴加入稀H2SO4
9. 如图所示是磷与氧气反应前后的微观模型图(●表示磷原子,〇表示氧原子),根据质量守恒定律,则虚线框中的微观模型应该是( ) A、
A、 B、
B、 C、
C、 D、
D、 10. 在一个密闭容器中放入M、N、Q、P四种物质,在一定条件下发生化学反应,一段时间后,测得有关数据如下表,则关于此反应认识不正确的是( )
10. 在一个密闭容器中放入M、N、Q、P四种物质,在一定条件下发生化学反应,一段时间后,测得有关数据如下表,则关于此反应认识不正确的是( )物质
M
N
Q
P
反应前质量(g)
X
26
2
12
反应后质量(g)
18
1
2
32
A、该变化的基本反应类型是化合反应 B、反应前物质M的质量为13g C、反应中N、P的质量比为5:4 D、物质Q可能是该反应的催化剂11. 实验室制取CO2的有关操作如下,不正确的是( )A、检查气密性 B、制气
B、制气 C、收集
C、收集 D、验满
D、验满 12. 有18.6g的NaOH和Na2CO3固体混合物,已知Na元素与C元素的质量比是23:3,把该固体全部加入到盛有100g的足量稀硫酸的烧杯中,充分反应后,烧杯里残留物质的质量是114.2g。则原NaOH和Na2CO3固体混合物中钠元素的质量是( )A、9.2g B、6.9g C、4.6g D、2.3g13. 向含CuCl2和HCl的100g混合溶液中,逐滴加入溶质质量分数为10%的NaOH溶液,参加反应的NaOH溶液质量与生成沉淀质量关系如图。下列说法正确的是( )
12. 有18.6g的NaOH和Na2CO3固体混合物,已知Na元素与C元素的质量比是23:3,把该固体全部加入到盛有100g的足量稀硫酸的烧杯中,充分反应后,烧杯里残留物质的质量是114.2g。则原NaOH和Na2CO3固体混合物中钠元素的质量是( )A、9.2g B、6.9g C、4.6g D、2.3g13. 向含CuCl2和HCl的100g混合溶液中,逐滴加入溶质质量分数为10%的NaOH溶液,参加反应的NaOH溶液质量与生成沉淀质量关系如图。下列说法正确的是( ) A、整个反应过程中,氯离子数目不变 B、P点溶液中的溶质只有一种 C、M点溶液比P点溶液中氯化钠的质量分数小 D、沉淀完全时,m1的数值为8014. 将n克的铁粉和镁粉分别加入到两个烧杯中,再向烧杯内逐渐滴加稀硫酸至m克,产生的氢气质量与滴加稀硫酸质量的关系如右图。若烧杯中加入铁粉和镁粉为t克时( t≠n),重复实验,绘制图像。下列图像可能出现的是( )
A、整个反应过程中,氯离子数目不变 B、P点溶液中的溶质只有一种 C、M点溶液比P点溶液中氯化钠的质量分数小 D、沉淀完全时,m1的数值为8014. 将n克的铁粉和镁粉分别加入到两个烧杯中,再向烧杯内逐渐滴加稀硫酸至m克,产生的氢气质量与滴加稀硫酸质量的关系如右图。若烧杯中加入铁粉和镁粉为t克时( t≠n),重复实验,绘制图像。下列图像可能出现的是( ) A、
A、 B、
B、 C、
C、 D、
D、 15. 将质量相等的镁、锌、铁三种金属,同时分别放入三份质量分数相同且等质量的稀盐酸中,反应生成的氢气与反应时间的关系如图所示.根据图中所提供的信息,得出的结论错误的是( )
15. 将质量相等的镁、锌、铁三种金属,同时分别放入三份质量分数相同且等质量的稀盐酸中,反应生成的氢气与反应时间的关系如图所示.根据图中所提供的信息,得出的结论错误的是( )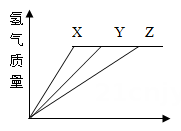 A、图线X表示镁的反应情况 B、盐酸都已完全反应 C、锌可能反应完,镁、铁一定过量 D、镁、锌一定过量,铁可能反应完16. 推理是学习化学时常用的思维方式,以下推理结果正确的是( )A、燃烧都伴随着发光、放热现象,所以有发光、放热现象的就是燃烧 B、电解水生成氢气和氧气,说明水是由氢分子和氧分子构成的 C、化合物是由不同种元素组成的纯净物,则只含一种元素的物质一定不是化合物 D、复分解反应有沉淀、气体或水生成,有沉淀、气体或水生成的反应是复分解反应17. 甲醛是装修时产生的主要污染物质。用化学反应可检测室内甲醛含量是否超标:4KMnO4+5R+6H2SO4=2K2SO4+4MnSO4+5CO2+11H2O,根据质量守恒定律确定R的化学式为( )A、CH2O B、C2H4O2 C、CH4 D、CHO218. 将25克20%的氢氧化钠溶液和25克20%的稀硫酸充分混合,混合后的溶液与下列物质不能发生反应的是( )A、二氧化碳 B、氧化铜 C、氯化钡溶液 D、硫酸铜溶液19. 在反应X+2Y=R+2M中(方程已配平),已知R和M的相对分子质量之比为22∶9,当1.6gX与Y完全反应后,生成4.4gR。则在此反应中Y和M的质量之比为 ( )A、16∶9 B、23∶9 C、32∶9 D、46∶920. 10克10%的盐酸与10克10%的氢氧化钠溶液混合,混合后溶液能与下列哪种物质反应( )A、CuSO4溶液 B、CO2 C、CuO D、H2SO421. 如图表示两种气体发生的化学反应,其中相同的球代表同种原子。下列说法正确的是( )
A、图线X表示镁的反应情况 B、盐酸都已完全反应 C、锌可能反应完,镁、铁一定过量 D、镁、锌一定过量,铁可能反应完16. 推理是学习化学时常用的思维方式,以下推理结果正确的是( )A、燃烧都伴随着发光、放热现象,所以有发光、放热现象的就是燃烧 B、电解水生成氢气和氧气,说明水是由氢分子和氧分子构成的 C、化合物是由不同种元素组成的纯净物,则只含一种元素的物质一定不是化合物 D、复分解反应有沉淀、气体或水生成,有沉淀、气体或水生成的反应是复分解反应17. 甲醛是装修时产生的主要污染物质。用化学反应可检测室内甲醛含量是否超标:4KMnO4+5R+6H2SO4=2K2SO4+4MnSO4+5CO2+11H2O,根据质量守恒定律确定R的化学式为( )A、CH2O B、C2H4O2 C、CH4 D、CHO218. 将25克20%的氢氧化钠溶液和25克20%的稀硫酸充分混合,混合后的溶液与下列物质不能发生反应的是( )A、二氧化碳 B、氧化铜 C、氯化钡溶液 D、硫酸铜溶液19. 在反应X+2Y=R+2M中(方程已配平),已知R和M的相对分子质量之比为22∶9,当1.6gX与Y完全反应后,生成4.4gR。则在此反应中Y和M的质量之比为 ( )A、16∶9 B、23∶9 C、32∶9 D、46∶920. 10克10%的盐酸与10克10%的氢氧化钠溶液混合,混合后溶液能与下列哪种物质反应( )A、CuSO4溶液 B、CO2 C、CuO D、H2SO421. 如图表示两种气体发生的化学反应,其中相同的球代表同种原子。下列说法正确的是( )
 A、生成物一定是混合物 B、分子在化学变化中不可分 C、该反应既不是化合反应也不是分解反应 D、化学反应前后原子的种类不变22. 下列图象正确反映对应的变化关系的是( )
A、生成物一定是混合物 B、分子在化学变化中不可分 C、该反应既不是化合反应也不是分解反应 D、化学反应前后原子的种类不变22. 下列图象正确反映对应的变化关系的是( )

①往食盐溶液中滴加足量的稀硫酸
②向含有HCl和Na2SO4的混合液中滴加足量的Ba(OH)2
③将足量的MgO、MgCO3固体分别加入到相同质量、质量分数的稀盐酸中
④在一定温度下,向接近饱和的KNO3溶液中加入足量的KNO3晶体(不含水分子)
A、①② B、②③ C、③④ D、②④23. 真空包装、食品包装内充氮气、放铁粉包或生石灰包等都是常用的食品防腐、保鲜方法,对.上述方法的分析,错误的是( )A、年糕真空包装:能使食品不与空气接触 B、薯片充氮气:能隔绝空气并防止食品变形 C、月饼放铁粉包:能除去包装袋内的氧气和水蒸气 D、海苔放生石灰包:能除去包装袋内的氧气
