广东省阳江市四校2022-2023学年高一上学期期中联考化学试题
试卷更新日期:2022-12-14 类型:期中考试
一、单选题
-
1. 下列反应一定属于氧化还原反应的是( )A、复分解反应 B、置换反应 C、化合反应 D、分解反应2. 下列各组物质中,按照化合物、单质、混合物顺序排列的一组是( )A、烧碱、液氮、碘酒 B、生石灰、纯碱、熟石灰 C、干冰、铁、氯化氢 D、空气、氮气、苏打3. 下列物质属于电解质的是( )A、铁丝 B、乙醇 C、NaCl溶液 D、MgCl24. 下列电离方程式正确的是( )A、盐酸:HCl = H+ + Cl- B、硫酸:H2SO4 = H+SO C、碳酸氢钠:NaHCO3 = Na++H+ + CO D、氢氧化钠:NaOH = Na+ + H+ + O2-5. 下列说法正确的是( )A、NaHSO4在水中能电离出H+ , 但NaHSO4不属于酸,属于盐 B、盐酸、浓硫酸都属于酸,也都属于化合物 C、石墨导电、金刚石不导电,故二者不是同素异形体 D、HCl不导电,属于非电解质6. 将一块金属钠投入滴有紫色石蕊溶液的盛冷水的烧杯中,甲同学认为可观察到下列现象,其中正确的有( )
①钠投入水中,先沉入水底,后浮出水面②钠立即与水反应,并有气体产生③反应后溶液变红④钠熔成闪亮的小球⑤小球在水面上四处游动⑥有“嘶嘶”的响声发出
A、①②③④ B、②③④⑤ C、②④⑤⑥ D、③④⑥7. 下列古诗词描述的场景中发生的化学反应不属于氧化还原反应的是( )A、爆竹声中一岁除——黑火药受热爆炸(主要反应为) B、蜡炬成灰泪始干——石蜡的燃烧 C、炉火照天地,红星乱紫烟——铁的冶炼(主要反应为) D、粉身碎骨浑不怕——块状的生石灰制成供人们使用的粉末状的熟石灰8. 市面上一种矿泉水标签上印有的主要矿物质成分及含量(单位为mg·L-1)为Ca-48.00、K-39.00、Mg-3.10、Zn-0.08、F-0.02等,则对此矿泉水的叙述正确的是( )A、该矿泉水不属于分散系 B、该矿泉水能导电 C、该矿泉水是电解质 D、该矿泉水是非电解质9. 下列无色溶液中能大量共存的离子组是( )A、K+、H+、SO、OH- B、NH、Ba2+、Cl-、NO C、Ca2+、H+ 、Cl-、CO D、Na+、Cu2+、Cl-、SO10. 下列关于Fe(OH)3胶体的说法错误的是( )A、Fe(OH)3胶体属于混合物 B、可利用渗析的方法除去Fe(OH)3胶体中少量的FeCl3 C、FeCl3溶液和Fe(OH)3胶体的本质区别为是否具有丁达尔效应 D、制备Fe(OH)3胶体时应向沸水中滴加FeCl3溶液至出现透明的红褐色11. 下列反应的离子方程式书写正确的是( )A、稀硫酸滴在铜片上:Cu+2H+=Cu2++H2↑ B、氧化镁溶于盐酸:MgO + 2H+ = Mg2+ + H2O C、稀硝酸滴在大理石上:CO + 2H+ = H2O + CO2↑ D、氢氧化钡溶液与硫酸铜溶液混合:Ba2+ + SO = BaSO4↓12. 下列反应能用2H+ + CO = CO2↑ +H2O表示的是( )A、盐酸与MgCO3溶液反应 B、醋酸与Na2CO3溶液反应 C、HNO3溶液与NaHCO3溶液反应 D、稀硫酸与(NH4)2CO3溶液反应13. 下列各组物质相互混合后,不会发生离子反应的是( )A、Na2SO4溶液和MgCl2溶液 B、Na2CO3溶液和稀硫酸 C、NaOH溶液和Fe2(SO4)3溶液 D、Ca(OH)2溶液和盐酸14. 下列化学变化中,需要加入氧化剂才能实现的是( )A、Na→Na+ B、Cl2→HCl C、CuO→Cu D、SO2→Na2SO315. 不是所有灭火都适用CO2灭火器,比如万一金属镁失火,应该用沙土而不是CO2灭火器。原因是CO2可以支持镁燃烧,发生反应:2Mg+CO2=2MgO+C,下列关于该反应的判断正确的是( )A、Mg的化合价由0升高到+2,所以MgO是还原产物 B、由此反应可以判断该反应条件下:氧化性CO2 > MgO,还原性Mg > C C、CO2作氧化剂,表现出氧化性,发生氧化反应 D、Mg原子失去电子的数目与C原子得到电子的数目之比为2∶416. 下列反应中,HCl充当还原剂的是( )A、NaOH + HCl = NaCl +H2O B、Zn + 2HCl = ZnCl2 + H2↑ C、MnO2 + 4HCl = MnCl2 +2H2O + Cl2↑ D、Fe2O3 + 6HCl = 2FeCl3 + 3H2O17. 在实验室中,用镊子从煤油中取出一小块金属钠,然后用滤纸将煤油吸干,再用小刀切开观察。在这一实验过程中不能得出的钠的物理性质是( )A、钠在常温下是固体 B、钠具有银白色的金属光泽 C、钠的熔点很低 D、金属钠很软18. 下列单、双线桥的表示方法错误的是( )A、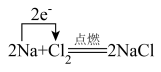 B、
B、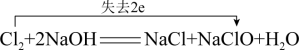 C、
C、 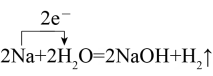 D、
D、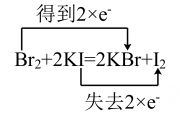 19. 钠与水反应的现象和钠的下列性质无关的是( )A、钠的熔点较低 B、钠的密度小于水 C、钠的硬度较小 D、钠的还原性强20. 向某溶液中加入Ba(OH)2溶液后生成白色沉淀,加入足量稀盐酸后沉淀部分溶解,同时有无色无味的气体生成,将该气体通入澄清石灰水,澄清石灰水变浑浊。下列离子组符合上述现象的是( )A、 、 B、 、 C、Cl-、 D、 、OH-
19. 钠与水反应的现象和钠的下列性质无关的是( )A、钠的熔点较低 B、钠的密度小于水 C、钠的硬度较小 D、钠的还原性强20. 向某溶液中加入Ba(OH)2溶液后生成白色沉淀,加入足量稀盐酸后沉淀部分溶解,同时有无色无味的气体生成,将该气体通入澄清石灰水,澄清石灰水变浑浊。下列离子组符合上述现象的是( )A、 、 B、 、 C、Cl-、 D、 、OH-二、填空题
-
21. 有下列物质:①熔融氯化钠 ②Al2(SO4)3 ③液态HCl ④稀硫酸 ⑤二氧化碳 ⑥铁 ⑦蔗糖
请回答下列问题:
(1)、可以导电的有(填序号,下同)。(2)、属于电解质的有。(3)、属于非电解质的有 。(4)、②在水中的电离方程式为。(5)、请写出④与⑥反应的离子方程式。22. 如图是有关钠与水反应及产物检验的实验装置。实验开始时先向管内加入滴有酚酞的水,使水位达到B端管口,然后迅速塞紧橡胶塞并拔掉大头针,此时Na掉入水中。
回答下列问题:
(1)、钠与水反应的化学方程式为。(2)、钠与水反应的现象很多,不同的现象证明不同的性质。①能证明钠的密度比水小的现象是。
②能证明钠的熔点低的现象是。
③能证明有氢氧化钠生成的现象是。
④能证明有气体产生的现象是A端液面B端液面(填“高于”、或“低于”)
三、综合题
-
23. 央视《每周质量报告》曝光了河北省一些明胶企业将皮革废料熬制成工业明胶,出售给浙江绍兴某些制药企业,最终变成药用胶囊。由工业明胶制成的胶囊往往含有超标的重金属铬,会对人体造成伤害。明胶是水溶性蛋白质混合物,溶于水形成胶体。(1)、已知Fe(CrO2)2中铬元素是+3价,则其中铁元素是价。CrO是一种酸根离子,则Fe(CrO2)2属于(填“酸”、“碱”、“盐”或“氧化物”)。(2)、明胶的水溶液和K2SO4溶液共同具备的性质是(填序号)。
a.都不稳定,密封放置会产生沉淀
b.二者均有丁达尔效应
c.分散质粒子可通过滤纸
(3)、已知胶体的分散质不能透过半透膜,但水分子等小分子或离子能透过半透膜。提纯明胶的装置是下列中的____(填序号)。A、 B、
B、 C、
C、 (4)、现有10mL明胶的水溶液与5mL K2SO4溶液混合装入半透膜内,将此半透膜袋浸入盛蒸馏水的烧杯中,设计实验证明SO能够透过半透膜:。24. 有一包白色粉末,其中可能含有Ba(NO3)2、MgCl2、K2CO3、NaOH,现做以下实验:
(4)、现有10mL明胶的水溶液与5mL K2SO4溶液混合装入半透膜内,将此半透膜袋浸入盛蒸馏水的烧杯中,设计实验证明SO能够透过半透膜:。24. 有一包白色粉末,其中可能含有Ba(NO3)2、MgCl2、K2CO3、NaOH,现做以下实验:①取一定量粉末加入水中,振荡,有白色沉淀生成;②向①的沉淀物中加入足量稀硝酸,白色沉淀完全消失,没有气泡产生;③向①的上层清液中滴入硫酸钠溶液,有白色沉淀产生。根据上述实验事实,回答下列问题:
(1)、原白色粉末中一定含有的物质是 , 一定不含有的物质是。(写化学式)(2)、写出各步变化的离子方程式。①; ②;③。