辽宁省锦州市太和区2022-2023学年九年级上学期期中化学试题
试卷更新日期:2022-12-09 类型:期中考试
一、单选题
-
1. 下列变化中,属于化学变化的是( )A、糖溶于水 B、苹果腐烂 C、汽车爆胎 D、水蒸发2. “减污降碳,保卫蓝天”,校园内下列做法不符合这一主题的是( )A、白天及时关灯 B、循环使用教材 C、集中焚烧落叶 D、垃圾分类处理3. 下列实验操作错误的是( )A、取固体药品
 B、点燃酒精灯
B、点燃酒精灯 C、滴加液体
C、滴加液体 D、加热液体
D、加热液体 4. 日常生活中常接触到含氟牙膏,高钙牛奶,加铁酱油等用品,这里的氟、钙、铁指的是( )A、元素 B、分子 C、原子 D、单质5. 生活中的下列现象不属于缓慢氧化的是( )A、钢铁生锈 B、麦田里堆放的秸秆自燃 C、动植物的呼吸 D、夏天米饭放在空气中一段时间后变馊6. 某同学在吃薯片时,发现包装袋内充满着气体,于是他想到一个问题:包装袋内的气体是什么气体呢?这属于科学探究环节中的( )A、提出问题 B、设计实验 C、交流评价 D、得出结论7. 中学生应有一定的安全常识。发现火险或遇火灾时,下列做法错误的是( )A、电振子着火,立即切断电源再灭火 B、液化气泄漏时,应立即关闭阀门打开门窗 C、室内起火时,立即打开门窗通风 D、火灾被困时,用湿毛巾捂住口鼻低姿前行8. 下列有关微粒的说法正确的是( )A、分子可分,原子不可分 B、原子中都含有质子、中子、电子 C、分子一定是由原子构成的 D、原子不显电性是因为原子中没有带电粒子9. 中国空间站利用铁酸镍(化学式为NiFe2O4)将航天员呼出的二氧化碳转化为航天员需要的氧气,铁酸镍中Ni为+2价,则铁元素的化合价为( )A、+2 B、+3 C、+6 D、+110. 从分子的角度解释下列现象,其中正确的是( )A、岩石能被粉碎成粉末——分子很小 B、春天柳絮飞扬——分子在不断运动 C、变瘪了的乒乓球放在热水中鼓起——分子的体积变大 D、液态二氧化碳和气态二氧化碳都能灭火——同种物质的分子化学性质相同11. 2022年中国空间站天宫课堂上太空教师展示了金属锆熔化与凝固实验。如图是锆在元素周期表中的部分信息及其原子结构示意图。以下从图中获得的信息正确的是( )
4. 日常生活中常接触到含氟牙膏,高钙牛奶,加铁酱油等用品,这里的氟、钙、铁指的是( )A、元素 B、分子 C、原子 D、单质5. 生活中的下列现象不属于缓慢氧化的是( )A、钢铁生锈 B、麦田里堆放的秸秆自燃 C、动植物的呼吸 D、夏天米饭放在空气中一段时间后变馊6. 某同学在吃薯片时,发现包装袋内充满着气体,于是他想到一个问题:包装袋内的气体是什么气体呢?这属于科学探究环节中的( )A、提出问题 B、设计实验 C、交流评价 D、得出结论7. 中学生应有一定的安全常识。发现火险或遇火灾时,下列做法错误的是( )A、电振子着火,立即切断电源再灭火 B、液化气泄漏时,应立即关闭阀门打开门窗 C、室内起火时,立即打开门窗通风 D、火灾被困时,用湿毛巾捂住口鼻低姿前行8. 下列有关微粒的说法正确的是( )A、分子可分,原子不可分 B、原子中都含有质子、中子、电子 C、分子一定是由原子构成的 D、原子不显电性是因为原子中没有带电粒子9. 中国空间站利用铁酸镍(化学式为NiFe2O4)将航天员呼出的二氧化碳转化为航天员需要的氧气,铁酸镍中Ni为+2价,则铁元素的化合价为( )A、+2 B、+3 C、+6 D、+110. 从分子的角度解释下列现象,其中正确的是( )A、岩石能被粉碎成粉末——分子很小 B、春天柳絮飞扬——分子在不断运动 C、变瘪了的乒乓球放在热水中鼓起——分子的体积变大 D、液态二氧化碳和气态二氧化碳都能灭火——同种物质的分子化学性质相同11. 2022年中国空间站天宫课堂上太空教师展示了金属锆熔化与凝固实验。如图是锆在元素周期表中的部分信息及其原子结构示意图。以下从图中获得的信息正确的是( ) A、锆元素属于非金属元素 B、锆的相对原子质量是91.22g C、锆原子核内有40个质子 D、锆原子容易失去2个电子形成阴离子12. 下列有关实验现象的描述,正确的是( )A、木炭在空气中燃烧,发出白光,放出热量 B、红磷在空气中燃烧,产生大量白雾,放出热量 C、石蜡在氧气中燃烧时,发出白光,放出热量 D、镁带在空气中燃烧,发出耀眼的白光,生成黑色粉末13. 分析推理是学习化学常用的思维方法,必须科学严谨。下列推理正确的( )A、氧化物是含氧元素的化合物,则含氧元素的化合物一定是氧化物 B、单质是同种元素组成的纯净物,但同种元素组成的物质不一定是单质 C、不同种分子构成的物质一定是混合物,则混合物一定是由不同种分子构成的 D、混合物中至少含有两种物质,则混合物中至少含有两种元素14. “天宫课堂”上的泡腾片实验让我们感受到化学的魅力。泡腾片中含有维生素C、柠檬酸(化学式为C6H8O7)、碳酸氢钠等物质,下列关于柠檬酸的说法中正确的是( )A、柠檬酸是由碳原子、氢原子和氧原子构成的 B、柠檬酸分子中含有21个原子 C、柠檬酸中质量分数最大的元素是氢元素 D、柠橡酸是由碳、氢、氧三种元素组成的15. 进行化学实验是学习化学知识、培养化学素养的重要方法。下列方案不能达到预目的的是( )
A、锆元素属于非金属元素 B、锆的相对原子质量是91.22g C、锆原子核内有40个质子 D、锆原子容易失去2个电子形成阴离子12. 下列有关实验现象的描述,正确的是( )A、木炭在空气中燃烧,发出白光,放出热量 B、红磷在空气中燃烧,产生大量白雾,放出热量 C、石蜡在氧气中燃烧时,发出白光,放出热量 D、镁带在空气中燃烧,发出耀眼的白光,生成黑色粉末13. 分析推理是学习化学常用的思维方法,必须科学严谨。下列推理正确的( )A、氧化物是含氧元素的化合物,则含氧元素的化合物一定是氧化物 B、单质是同种元素组成的纯净物,但同种元素组成的物质不一定是单质 C、不同种分子构成的物质一定是混合物,则混合物一定是由不同种分子构成的 D、混合物中至少含有两种物质,则混合物中至少含有两种元素14. “天宫课堂”上的泡腾片实验让我们感受到化学的魅力。泡腾片中含有维生素C、柠檬酸(化学式为C6H8O7)、碳酸氢钠等物质,下列关于柠檬酸的说法中正确的是( )A、柠檬酸是由碳原子、氢原子和氧原子构成的 B、柠檬酸分子中含有21个原子 C、柠檬酸中质量分数最大的元素是氢元素 D、柠橡酸是由碳、氢、氧三种元素组成的15. 进行化学实验是学习化学知识、培养化学素养的重要方法。下列方案不能达到预目的的是( )选项
A
B
C
D
方案




结论
检查装置的气密性
验证蜡烛燃烧产生水
比较空气与呼出气体中二氧化碳的含量
证明液态水与气态水可以相互转化
A、A B、B C、C D、D二、填空题
-
16. 化学用语是学习化学的基本工具。(1)、请用化学用语填空:
①氯气;
②3个铜原子;
③地壳中含量最多的元素;
④2个碳酸根;
⑤标出二氧化氮中氮元素的化合价。
(2)、写出符号中数字“2”的含义:①;
②2CO。
17. 我们生活的世界是由丰富多彩的物质组成,物质是由微小的粒子构成的。请你分别写出符合下列要求的一种物质:由原子构成的物质;由分子构成的物质;由离子构成的物质。18. 请写出鉴别下列各组物质的方法(不需要写现象和结论)。(1)、空气和氧气;(2)、铜粉和铁粉;(3)、食醋和酱油。19. 我们生活在物质世界中,每天都要接触很多物质:如①铁 ②氧化镁 ③氯化钠 ④稀有气体 ⑤氯酸钾(KClO3) ⑥冰水混合物 ⑦氧气 ⑧二氧化碳 ⑨空气 ⑩河水(1)、属于混合物的是(填序号,下同);(2)、属于单质的是;(3)、属于化合物的是;(4)、属于氧化物的是;(5)、含有氧元素的是;(6)、含有氧分子的是。20. 下表为元素周期表的一部分,请你根据表中信息回答下列问题: (1)、地壳中含量最多的金属元素位于第周期;(2)、表中3号元素的原子在化学反应中容易 (填“得到”或“失去”)电子形成离子,其离子符号是;(3)、写出核外电子排布与氖原子相同的一种阴离子的符号;(4)、元素M是第三周期中的一种元素,与氯元素形成的化合物的化学式为MCl3 , 则M的元素符号为;(5)、第三周期从左到右各元素原子结构排布规律有(写出一条)。21. 空气是一种重要的自然资源。请沿用科学家认识事物的方法认识“空气”。(1)、从性质决定用途的角度:说明下列应用利用了气体的什么性质。
(1)、地壳中含量最多的金属元素位于第周期;(2)、表中3号元素的原子在化学反应中容易 (填“得到”或“失去”)电子形成离子,其离子符号是;(3)、写出核外电子排布与氖原子相同的一种阴离子的符号;(4)、元素M是第三周期中的一种元素,与氯元素形成的化合物的化学式为MCl3 , 则M的元素符号为;(5)、第三周期从左到右各元素原子结构排布规律有(写出一条)。21. 空气是一种重要的自然资源。请沿用科学家认识事物的方法认识“空气”。(1)、从性质决定用途的角度:说明下列应用利用了气体的什么性质。①氮气填充食品包装袋;
②稀有气体作霓虹灯。
(2)、从环保的角度:①计入空气污染指数的项目中除了可吸入颗粒物外,还包括有害气体,如: (选填一种有害气体化学式);
②汽车工业的发展方便了我们的出行,但汽车尾气的排放严重的污染了空气,请你提出防止汽车尾气污染的两项措施:、。
22. 在学习“燃烧与灭火”的内容时,小文同学用两种不同方法熄灭蜡烛火焰。 (1)、实验1、实验2依据的灭火原理分别是:
(1)、实验1、实验2依据的灭火原理分别是:实验1: ;
实验2: 。
(2)、请写出与上述灭火原理不同的另一个原理及实例:原理:;灭火实例:。
23. 从微观的角度来认识物质的构成和物质的变化,是学习化学的重要方法。图1、图2分别是水蒸气液化和氢气在氯气中燃烧的微观示意图。

请回答:
(1)、图1中第一个框内的物质是(填“纯净物”或“混合物”),请用分子的观点解释;(2)、请写出图2变化的符号表达式 , 基本反应类型是;(3)、从微观角度看,图2的变化前后,一定不变的微粒是(用具体微粒名称填空);(4)、写出从微观的角度由图2获得的信息(写出两点): , 。三、简答题
-
24. 请列举合适的生产、生活实例,说明下列化学原理:(1)、反应物的浓度不同,反应现象可能不同;(2)、可燃物与氧气接触面积不同燃烧现象可能不同;(3)、不同种物质的分子化学性质不同。
四、综合题
-
25. A、B、C、D、E是初中化学常见的物质,A、D是无色气体,D→A可通过植物的光合作用进行转化。B是白色固体,C是黑色固体,E与A反应生成有刺激性气味的气体。物质间的转化关系如图所示(图中“—”表示两端的物质能发生反应,“→”表示一种物质转化为另一种物质,其中部分反应物、生成物、反应条件已略去)。
 (1)、写出B→A反应的文字表达式 , 反应的基本类型是;(2)、写出A→C反应的文字表达式 , 反应现象是;(3)、写出A和E反应的符号表达式;(4)、气体A的用途是。26. 化学是以实验为基础的科学,请根据下图所示实验回答问题:
(1)、写出B→A反应的文字表达式 , 反应的基本类型是;(2)、写出A→C反应的文字表达式 , 反应现象是;(3)、写出A和E反应的符号表达式;(4)、气体A的用途是。26. 化学是以实验为基础的科学,请根据下图所示实验回答问题: (1)、图1所示实验是量取VmL的水。若按照图示进行实验操作,则可能会导致量取水的体积 (填“>”、“<”或“=”)VmL。(2)、图2是铁丝在氧气中燃烧实验。图中实验的不足之处是。(3)、图3实验可观察到现象是 , 说明分子具有的性质是。27. 某兴趣小组开展“测定密闭容器中某种气体的体积分数”的探究实验。
(1)、图1所示实验是量取VmL的水。若按照图示进行实验操作,则可能会导致量取水的体积 (填“>”、“<”或“=”)VmL。(2)、图2是铁丝在氧气中燃烧实验。图中实验的不足之处是。(3)、图3实验可观察到现象是 , 说明分子具有的性质是。27. 某兴趣小组开展“测定密闭容器中某种气体的体积分数”的探究实验。【实验1】按图1所示装置,用红磷燃烧的方法测定空气中氧气的体积分数。
【实验2】已知铁与水和氧气反应生成红色固体铁锈,按图2所示装置,在集气瓶内壁用水均匀涂附铁粉除氧剂(其中辅助成分不干扰实验)测定空气中氧气的体积分数。
 (1)、实验1中,红磷燃烧反应的文字表达式是。红磷熄灭后,集气瓶冷却至室温,打开止水夹K,观察到的现象是。(2)、图2实验的优点是。(3)、结合你的学习经验,若要寻找红磷或铁粉除氧剂的替代物。用图1或图2装置测定空气中氧气的体积分数,该替代物一般情况下应满足的条件是、 (写两点即可)。28. 请根据下图回答下列问题:
(1)、实验1中,红磷燃烧反应的文字表达式是。红磷熄灭后,集气瓶冷却至室温,打开止水夹K,观察到的现象是。(2)、图2实验的优点是。(3)、结合你的学习经验,若要寻找红磷或铁粉除氧剂的替代物。用图1或图2装置测定空气中氧气的体积分数,该替代物一般情况下应满足的条件是、 (写两点即可)。28. 请根据下图回答下列问题: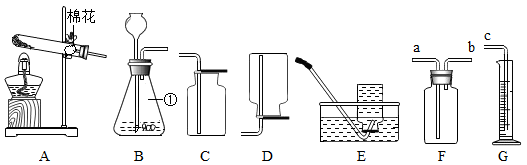 (1)、写出上图中仪器的名称:①。(2)、实验室用A和E装置制取并收集O2 , 反应的文字表达式是 , 实验操作如下:①加热;②检查装置气密性;③装药品及用品;④用排水法收集;⑤从水槽中取出导气管;⑥熄灭酒精灯;⑦连接仪器。正确的操作顺序是。某同学用该方法制取一集气瓶氧气后经检测发现,它并不能使带火星的木条复燃,老师说他收集的氧气浓度太低,请帮他分析可能的原因 (写出一点)。(3)、A装置中试管口向下倾斜的原因是。(4)、用双氧水制取氧气,选择的发生装置为(填字母),反应的文字表达式为 , 选择该方法制氧气的优点是 (写出一点)。(5)、上图中F装置有多种功能。若用装置F、G组合来收集并测定的体积,应先在集气瓶中装满水,然后将导管 (填“a”或“b”)端和导管c端连接。(6)、氨气是一种无色有刺激性气味的气体,密度比空气小,极易溶于水,溶于水形成的溶液是氨水。实验室用加热氯化铵和消石灰的固体混合物制取氨气。则实验室制取氨气选用的发生装置和收集装置是(选填“A~E”字母序号)。29. 某化学兴趣小组阅读课外资料得知,双氧水分解除了二氧化锰作催化剂,还可以用氧化铜等物质作催化剂,于是对氧化铜产生了探究兴趣。
(1)、写出上图中仪器的名称:①。(2)、实验室用A和E装置制取并收集O2 , 反应的文字表达式是 , 实验操作如下:①加热;②检查装置气密性;③装药品及用品;④用排水法收集;⑤从水槽中取出导气管;⑥熄灭酒精灯;⑦连接仪器。正确的操作顺序是。某同学用该方法制取一集气瓶氧气后经检测发现,它并不能使带火星的木条复燃,老师说他收集的氧气浓度太低,请帮他分析可能的原因 (写出一点)。(3)、A装置中试管口向下倾斜的原因是。(4)、用双氧水制取氧气,选择的发生装置为(填字母),反应的文字表达式为 , 选择该方法制氧气的优点是 (写出一点)。(5)、上图中F装置有多种功能。若用装置F、G组合来收集并测定的体积,应先在集气瓶中装满水,然后将导管 (填“a”或“b”)端和导管c端连接。(6)、氨气是一种无色有刺激性气味的气体,密度比空气小,极易溶于水,溶于水形成的溶液是氨水。实验室用加热氯化铵和消石灰的固体混合物制取氨气。则实验室制取氨气选用的发生装置和收集装置是(选填“A~E”字母序号)。29. 某化学兴趣小组阅读课外资料得知,双氧水分解除了二氧化锰作催化剂,还可以用氧化铜等物质作催化剂,于是对氧化铜产生了探究兴趣。【提出问题】氧化铜是否也能作氯酸钾分解的催化剂?它是否比二氧化锰催化效果更好?
实验序号
KClO3质量
其他物质质量
待测数据
①
1.2 g
②
x
CuO 0.5 g
③
1.2 g
MnO2 0.5g
(1)、表中x应该是;上述实验测量的“待测数据”是。(2)、若实验②比实验①的“待测数据”更 (填“大”或“小”),说明氧化铜能加快氯酸钾的分解速率。(3)、对实验②反应后的固体加水溶解、过滤、洗涤、干燥,称量得到0.5g黑色粉末,这是为了证明氧化铜的在反应前后没有改变。(4)、【预期结论】氧化铜也能作氯酸钾分解的催化剂。【评价设计】你认为设计实验③和实验②对比的目的是;上述实验探究不能证明氧化铜能作氯酸钾分解的催化剂,其理由是。
(5)、【实验拓展】大家从课外资料上还获得下列信息:氧化铁、硫酸铜、猪肝、马铃薯等也可以作过氧化氢分解的催化剂。下列有关催化剂的说法正确的是。A.二氧化锰可作任何反应的催化剂
B.同一个反应可能有多种催化剂
C.催化剂一定能加快反应速率
D.没有催化剂化学反应不能发生
E.对很多工业反应,加入催化剂能起到增加生成物的质量的效果
五、计算题
-
30. 常用的医用酒精是体积分数为75%的乙醇溶液,可用于杀菌消毒,乙醇的化学式为C2H5OH。请完成下列计算。(要求写出计算过程)(1)、乙醇的相对分子质量;(2)、乙醇中碳元素和氢元素的质量比为;(3)、92g乙醇中碳元素的质量为。
-