陕西省西安市周至县2021-2022学年九年级上学期期中化学试题
试卷更新日期:2022-12-09 类型:期中考试
一、单选题
-
1. 下列实验室中的交流,属于化学变化的是( )A、锥形瓶:“同学们不爱惜我,我被摔碎了” B、铁架台:“好难受啊!我在潮湿的空气中生锈了” C、试管:“我在试管架上呆了一段时间,原先附着的水怎么不见了?” D、滤纸:“过滤时为什么搅拌?我都被划破了”2. 我国是一个统一的多民族国家,各民族像石榴籽一样紧紧抱在一起。石榴是人们喜爱的一种水果,石榴中含有的钙、磷、铁是指( )A、分子 B、原子 C、离子 D、元素3. 下列物质中,前者属于混合物,后者属于化合物的是( )A、矿泉水、冰水混合物 B、自来水、氢气 C、水、空气 D、氢氧化钠溶液、碘酒4. 化学实验是培养化学素养的重要途径。下列实验操作正确的是( )A、取用液体
 B、滴加液体
B、滴加液体 C、检验氢气纯度
C、检验氢气纯度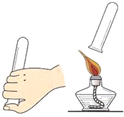 D、振荡试管
D、振荡试管 5. 下面是某同学“化学笔记”中的部分摘录,其中正确的是( )A、工业废水直接灌溉农田,有利于节约水资源 B、地壳中含量前三位的元素依次是O、Fe、Al C、用蜡烛照明是利用石蜡的可燃性,属于物理性质 D、生活中常用加热煮沸的方法将硬水软化6. 下列宏观事实的微观解释错误的是( )A、6000L氧气在加压的情况下可装入容积为40L的钢瓶中——分子体积变小 B、氧气和液氧都能支持燃烧——物质的分子相同,其化学性质相同 C、品红在水中扩散——分子在不断运动 D、1滴水中大约有1.67×1021个水分子——分子很小7. 如图是一种处理汽车尾气的微观反应示意图,下列说法正确的是( )
5. 下面是某同学“化学笔记”中的部分摘录,其中正确的是( )A、工业废水直接灌溉农田,有利于节约水资源 B、地壳中含量前三位的元素依次是O、Fe、Al C、用蜡烛照明是利用石蜡的可燃性,属于物理性质 D、生活中常用加热煮沸的方法将硬水软化6. 下列宏观事实的微观解释错误的是( )A、6000L氧气在加压的情况下可装入容积为40L的钢瓶中——分子体积变小 B、氧气和液氧都能支持燃烧——物质的分子相同,其化学性质相同 C、品红在水中扩散——分子在不断运动 D、1滴水中大约有1.67×1021个水分子——分子很小7. 如图是一种处理汽车尾气的微观反应示意图,下列说法正确的是( ) A、分子在化学变化中不可再分 B、该反应前后原子的种类和数目均发生改变 C、该反应中有单质生成 D、该反应为化合反应8. 20℃时,取甲、乙、丙、丁四种纯净物各40g,分别加入到四个盛有100g水的烧杯中,充分溶解,其溶解情况如下表:
A、分子在化学变化中不可再分 B、该反应前后原子的种类和数目均发生改变 C、该反应中有单质生成 D、该反应为化合反应8. 20℃时,取甲、乙、丙、丁四种纯净物各40g,分别加入到四个盛有100g水的烧杯中,充分溶解,其溶解情况如下表:物质
甲
乙
丙
丁
未溶解固体的质量/g
8.4
4
0
18.4
下列说法正确的是( )
A、所得四杯溶液一定都是饱和溶液 B、四杯溶液中溶质的质量分数大小关系为:丁>甲>乙>丙 C、升高温度,四杯溶液中溶质的质量分数一定会改变 D、四杯溶液中各加入20℃100g的水后,溶液质量相等,且均为不饱和溶液9. 归纳推理是化学学习过程中常用的思维方法,下列推理合理的是( )A、Na+、Cl-的最外层电子数均为8,则最外层电子数为8的粒子都是离子 B、不饱和溶液不一定是稀溶液,则饱和溶液也不一定是浓溶液 C、元素是具有相同质子数的一类原子的总称,则具有相同质子数的粒子一定属于同种元素 D、同种元素组成的纯净物是单质,则含同种元素的物质一定是单质二、填空题
-
10. 晓晨同学在厨房帮妈妈做饭时观察到了一些现象,请你利用所学知识进行回答:(1)、①食用油,②食盐、③面酱,④白醋是厨房中常用的调味品,将它们分别与足量水充分混合后,形成的混合物属于溶液的是(填序号)。(2)、烹煮番茄汤时,为了解汤的咸淡是否适宜,只须取锅中少量汤品尝,这是因为溶液具有(填“均一”或“稳定”)性。(3)、烹煮后的油锅很难用水洗干净,加点洗洁精就能轻松地洗掉,这是因为洗洁精具有作用。11. 通过化学学习,我们认识了一些常见的仪器,掌握了一些基本的实验操作。
 (1)、认识仪器:取用固体粉末用图1中的(填仪器名称)。(2)、掌握基本操作:
(1)、认识仪器:取用固体粉末用图1中的(填仪器名称)。(2)、掌握基本操作:①图2操作可能导致的后果是。
②玻璃仪器洗涤干净的标准是。
③如图3所示,用完酒精灯后,必须用灯帽盖灭,盖灭后轻提一下灯帽 , 再重新盖好。对加点部分原因的叙述错误的是(填字母)。
a.平衡气压,方便取下灯帽
b.挥发水分,利于点燃酒精灯
c.减少挥发,利于节约酒精
12. 在宏观、微观和化学符号之间建立联系是化学学科的特点。
 (1)、构成物质的粒子之间的关系如图1所示,其中空白①处代表的是。(2)、如图2,A是钙原子的结构示意图,B,C,D,E分别是四种粒子的结构示意图。
(1)、构成物质的粒子之间的关系如图1所示,其中空白①处代表的是。(2)、如图2,A是钙原子的结构示意图,B,C,D,E分别是四种粒子的结构示意图。①A中x=。
②A,B,C,D,E中属于阳离子的是(填离子符号)。
③B,C,D,E四种粒子中与A粒子化学性质相似的是(填字母)。
13. 依据下列“水”的变化回答相关问题。
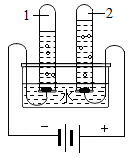


A.水的沸腾
B.水的电解
C.水的应用
D.海水淡化
(1)、上述四种变化中,能够证明水的组成的是(填字母)。(2)、写出B中发生反应的文字表达式。(3)、下列说法正确的是(填序号)。①A,B,C,D中发生的均是物理变化
②B中试管1中收集到的气体可使带火星的木条复燃
③C中可通过观察导管口是否有气泡冒出来确定装置是否漏气
(4)、D是采用膜分离技术的海水淡化装置。对海水加压,水分子可以通过半透膜形成淡水,而海水中的其它物质不能通过半透膜。加压后,装置右侧海水的溶质质量分数会(填“增大”或“减小”)。14. 食盐(主要成分为氯化钠)在生产和生活中具有广泛的用途,是一种重要的资源。(1)、海水晒盐是海水在常温下蒸发得到氯化钠固体的过程,实验室用氯化钠溶液模拟该过程。恒温蒸发一定质量的不饱和氯化钠溶液,该过程中,溶液中溶质质量的变化情况为。(2)、将纯净的氯化钠配制成溶液。20℃时,向4个盛有200g水的烧杯中,分别加入一定质量的氯化钠并充分溶解。4组实验数据如下:实验序号
Ⅰ
Ⅱ
Ⅲ
Ⅳ
加入氯化钠的质量/g
9
36
81
90
溶液质量/g
209
236
272
272
①4组实验所得溶液中,属于不饱和溶液的是(填序号),将其变为饱和溶液的方法是。(写一种)
②20℃时,200g水中最多可溶解氯化钠的质量为g。
三、综合题
-
15. 某实验小组同学设计如下实验探究分子的运动。甲同学的实验如图1所示,图2是乙同学的实验,在锥形瓶中的小瓶里装着浓氨水,锥形瓶口用一张滤纸盖住,滤纸刚刚用酚酞溶液浸过。
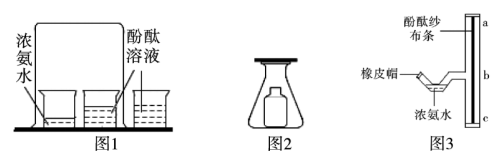 (1)、乙同学的实验中观察到的现象是。(2)、相比甲同学的实验,乙同学实验的优点是。(3)、丙同学用图3探究分子运动快慢与温度的关系。(已知氨气的密度比空气的密度小)
(1)、乙同学的实验中观察到的现象是。(2)、相比甲同学的实验,乙同学实验的优点是。(3)、丙同学用图3探究分子运动快慢与温度的关系。(已知氨气的密度比空气的密度小)①一段时间后,(填“ba”或“be”)段纱布条先变成红色。微热细弯管处的浓氨水,纱布条变红的速率会加快。
②得出结论;分子运动的快慢与温度的关系是。
16. 某同学配制60g溶质质量分数为5%的碳酸钠溶液,准备了下列实验用品: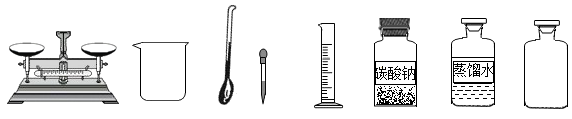 (1)、配制过程中还缺少的一种玻璃仪器是(填仪器名称),该仪器的作用是。(2)、计算所需碳酸钠的质量为g。(3)、量取蒸馏水:将蒸馏水注入量筒,待液面接近量取体积对应刻度线时,改用(填仪器名称)滴加蒸馏水至刻度线。(4)、经检测,实验所得溶液的溶质质量分数偏小,其原因可能是(填序号)。
(1)、配制过程中还缺少的一种玻璃仪器是(填仪器名称),该仪器的作用是。(2)、计算所需碳酸钠的质量为g。(3)、量取蒸馏水:将蒸馏水注入量筒,待液面接近量取体积对应刻度线时,改用(填仪器名称)滴加蒸馏水至刻度线。(4)、经检测,实验所得溶液的溶质质量分数偏小,其原因可能是(填序号)。①碳酸钠固体不纯
②量取水时,俯视读数
③称量时,砝码端忘垫质量相同的纸片
④装瓶时,有少量溶液洒出
(5)、取10g配制好的质量分数为5%的碳酸钠溶液,稀释成质量分数为1%的碳酸钠溶液,需加水g。17. 水是生命之源。某化学小组对市区饮用水的来源及净化产生了兴趣,并开始了系列探究。(1)、问题一:水源地进行处理前水质如何?怎样处理可以达到饮用标准?【调查研究】通过实地调查,明确了该水源中水质情况。
【参观考察】小组同学通过参观考察,绘制了自来水厂处理水的过程模拟图(如图1);


进入X池的水含有少量色素和异味,则X池中应加入的物质是。
(2)、进入气管网或水塔之前,通入氯气的主要目的是。(3)、【反思质疑】处理后的饮用水是纯水吗?经过讨论之后,同学们一致认为不是,理由是。
(4)、问题二:怎样处理才能得到纯水?【实验探究】学习小组在水库取了一烧杯水,然后按照图2步骤进行实验,得到了纯水。
【反思交流】
分离提纯混合物基本思路是:先除去不溶性杂质,再除去可溶性杂质。上述步骤中的(填字母)是将不溶性杂质分离除去。
(5)、要检验上述步骤C得到的水是硬水还是软水,可采用的方法是(写出实验操作、现象及结论)。(6)、【实验拓展】水能溶解很多物质,是一种常用的溶剂。小明同学设计如图所示实验证明物质溶于水,温度是否会发生变化。
进行实验时,打开分液漏斗,一段时间后观察到烧杯中导管口处有气泡冒出,则试管中所加固体物质是。(填序号)
①氢氧化钠 ②硝酸铵 ③氯化钠
出现上述现象的原因是。
四、计算题
-
18. 注射用链霉素试验针的药液配制方法如下:
①把1.0g链霉素溶于水制成4.0mL溶液a;
②取0.1mL溶液a,加水稀释至1.0mL,得溶液b;
③取0.1mL溶液b,加水稀释至1.0mL,得溶液c;
④取0.2mL溶液c,加水稀至1.0mL,得溶 液d.
由于在整个配制过程中药液很稀,其密度都 可近似看作是。试求:
(1)、溶液a中溶质的质量分数为。(2)、最终得到的试验针药液(溶液d)中溶质的质量分数为。(3)、1.0g链霉素可配制毫升试验针药液。