河北省邢台市六校联考2022-2023学年高一上学期期中考试化学试题
试卷更新日期:2022-11-28 类型:期中考试
一、单选题
-
1. 化学与生活密切相关,下列说法错误的是( )A、为防止中秋月饼等富脂食品因被氧化而变质,常在包装袋中放入生石灰 B、铜制器具产生铜绿与氧化还原反应有关 C、消毒用的75%酒精不能产生丁达尔效应 D、苹果削皮后露置于空气中因氧化而变黄,若泡到含维生素C的水中可以避免变黄,说明维生素C具有还原性2. 盐是一类常见的物质,下列种类中的某些物质通过一步反应可直接生成盐的是( )
①金属单质 ②碱性氧化物 ③碱 ④非金属单质 ⑤酸性氧化物 ⑥酸
A、①③④⑥ B、②③⑤⑥ C、①②③⑤⑥ D、都可以3. 下列离子方程式书写正确的是( )A、放入水中: B、向溶液中加过量的NaOH溶液: C、氯气通入水中: D、碳酸钙溶于稀盐酸中:4. 下列物质间的转化一定需要加入还原剂才能实现的是( )A、 B、 C、 D、5. 下列溶液中的离子由于发生氧化还原反应而不能大量共存的是( )A、、、、 B、、、、 C、、、、 D、、、、6. 氢化亚铜(CuH、其中Cu为+1价)是一种难溶于水的物质;不稳定,它与盐酸反应的化学方程式为:;还能在氯气中燃烧。氢化亚铜可用溶液和“另一种物质”在一定条件下反应来制备。下列有关判断错误的是( )A、CuH既有氧化性又有还原性 B、“另一种物质”一定具有还原性 C、CuH与盐酸反应中HCl为氧化剂,CuH为还原剂 D、CuH在足量的中燃烧生成物应该为和HCl7. 下列物质的性质与用途不具有对应关系的是( )A、NaClO具有强氧化性,可用作漂白剂 B、易溶于水,可用于食用碱或工业用碱 C、与水和二氧化碳反应生成氧气,常用于供氧剂 D、受热分解,常用于制作糕点的膨松剂8. 如图所示,试管中盛有水,气球中盛有干燥的固体粉末a,U形管中是滴有红墨水的浅红色的水溶液。将气球用橡皮绳紧系在试管口。实验时将气球中的固体粉末a抖落到试管的液体b(足量)中,下列有关说法错误的是( ) A、若a为 , b为滴有酚酞的水,则试管中的液体先变红后褪色 B、若a为 , b为滴有酚酞的水,则气球被吹大,U形管中水位c<d C、若a为 , b为滴有酚酞的水,则试管中的液体变红,U形管中水位c<d D、若a为 , b为饱和碳酸氢钠溶液,则试管中一定有晶体析出9. 下列说法错误的是( )A、、可用于对自来水的杀菌消毒 B、工业上可用氯气与石灰水反应制备漂白粉 C、欲除去中的少量HCl气体,可将此混合气体通过盛有饱和食盐水的洗气瓶 D、新制氯水中加入溶液,有白色沉淀生成10. 把一小块钠放入下列溶液中,不会出现沉淀的是( )A、硫酸氢钠溶液 B、溶液 C、硫酸铜溶液 D、饱和氢氧化钠溶液11. 下列物质久置于空气中易发生化学变化的有( )
A、若a为 , b为滴有酚酞的水,则试管中的液体先变红后褪色 B、若a为 , b为滴有酚酞的水,则气球被吹大,U形管中水位c<d C、若a为 , b为滴有酚酞的水,则试管中的液体变红,U形管中水位c<d D、若a为 , b为饱和碳酸氢钠溶液,则试管中一定有晶体析出9. 下列说法错误的是( )A、、可用于对自来水的杀菌消毒 B、工业上可用氯气与石灰水反应制备漂白粉 C、欲除去中的少量HCl气体,可将此混合气体通过盛有饱和食盐水的洗气瓶 D、新制氯水中加入溶液,有白色沉淀生成10. 把一小块钠放入下列溶液中,不会出现沉淀的是( )A、硫酸氢钠溶液 B、溶液 C、硫酸铜溶液 D、饱和氢氧化钠溶液11. 下列物质久置于空气中易发生化学变化的有( )①氯水、②碳酸钠晶体、③烧碱、④漂白粉、⑤过氧化钠、⑥碳酸氢钠
A、3种 B、4种 C、5种 D、6种12. 在新制氯水中存在多种分子和离子,它们在不同的反应中表现出各自的性质。下列关于新制氯水的说法错误的是( )A、新制氯水呈浅黄绿色,且有刺激性气味,说明溶液中有分子存在 B、用强光照射新制氯水一段时间后,溶液酸性增强,说明溶液中有HClO存在 C、将加入新制氯水中,有无色气泡产生,说明溶液中有存在 D、向新制氯水中滴加紫色石蕊试液先变红后褪色,说明新制氯水中有和分子存在13. 下列对于某些物质的检验及结论正确的是( )A、向溶液中加入稀盐酸产生气体,气体能使澄清石灰水变浑浊,原溶液中一定有 B、向溶液中加入硝酸银溶液产生白色沉淀,原溶液中一定有 C、用澄清石灰水鉴别、溶液,有白色沉淀生成的是溶液 D、用洁净的铁丝蘸取某物质,在酒精灯外焰上灼烧,火焰为黄色则该物质一定含钠元素14. 已知液氨(密度为)与钠的反应和水与钠的反应相似: , 易溶于液氨。下列说法正确的是( )A、该反应属于置换反应 B、将金属钠投入到液氨中,钠会浮在液面上四处游动 C、将金属钠投入到液氨中,会发出轻微的爆鸣声 D、钠与液氨的反应中为氧化剂,为还原产物二、多选题
-
15. 高锰酸钾溶液在酸性条件下可以与硫酸亚铁反应,化学方程式如下(未配平):
____________________________。
下列说法正确的是( )
A、是氧化剂,是还原产物 B、的还原性强于 C、化学方程式配平后的化学计量数是6 D、配平后高锰酸钾与的系数比为2∶516. 实验室模拟工业制备的装置如图所示。
原理:;
已知能与NaOH溶液发生反应。
下列有关叙述正确的是( )
A、装置甲的作用是除去中的杂质,装置甲中的物质可以是碱石灰 B、应先往装置乙中滴加溶液,再通入气体 C、在制备原理中是还原产物 D、能与NaOH溶液反应生成盐和水,可知属于酸性氧化物三、综合题
-
17. 某无色溶液中可能含、、、、、、、、中的几种,现进行如下实验:
①取适量溶液,加入足量NaOH溶液,生成白色沉淀。
②过滤,向滤液中加入足量溶液,有白色沉淀生成。根据上述实验回答下列问题。
(1)、溶液中一定不存在的离子是;(2)、写出①和②中所发生反应的离子方程式分别为、;(3)、为了进一步验证溶液中存在的阴离子,另取适量原溶液于试管中, , 则说明原溶液中不含 , 一定有;(4)、为确定其他可能存在的离子,可以用来检验的方法为。18. 实验室拟用下图所示仪器(必要时可重复使用)组装一套制备干燥纯净的氯气装置,请回答下列问题。 (1)、若以二氧化锰和浓盐酸为试剂制取氯气,组装氯气的发生装置A必需用到的玻璃仪器有:及导气管;(2)、按气体的流向自左向右导气管的连接顺序为:a接f;(3)、与发生装置A直接相连的装置中所盛放的试剂为;用排空气法收集氯气,判断集气瓶中已充满氯气的简单方法为;(4)、写出工业上制取漂白粉的化学方程式:;(5)、某同学将制取的氯气通过一个加热的内置有铁粉的石英玻璃管E(如图所示)制备某物质。
(1)、若以二氧化锰和浓盐酸为试剂制取氯气,组装氯气的发生装置A必需用到的玻璃仪器有:及导气管;(2)、按气体的流向自左向右导气管的连接顺序为:a接f;(3)、与发生装置A直接相连的装置中所盛放的试剂为;用排空气法收集氯气,判断集气瓶中已充满氯气的简单方法为;(4)、写出工业上制取漂白粉的化学方程式:;(5)、某同学将制取的氯气通过一个加热的内置有铁粉的石英玻璃管E(如图所示)制备某物质。
①写出E中发生反应的化学方程式:。
②资料表明E中的产物有以下性质:
a.受热易升华,冷却后易凝华;b.遇剧烈反应。
为收集E中的产物,在E与F之间增加一个收集装置,同时将装置F换成了装置G,则G的两个作用是、。
19.(1)、Ⅰ.某反应中反应物与生成物有:、、、、、和一种未知物质X。已知1个在反应中得到6个电子生成X,则X的化学式为。
(2)、根据上述反应可推知____。A、氧化性: B、氧化性: C、还原性: D、还原性:(3)、化学方程式配平后氧化剂和还原剂及其系数分别为。(4)、Ⅱ.实验室中利用固体进行如图所示实验:
回答下列问题:
在下列化学方程式中用双线桥法标出电子转移的方向和数目:
(5)、写出图中生成气体单质H的所有离子方程式(不考虑与浓盐酸的反应):。(6)、也可以与浓盐酸反应制取氯气同时生成。若分别用和与浓盐酸反应制取相同数目的分子,则消耗和的个数之比为。20. 完成下列问题(1)、钠元素有多种化合物。下列关于、、NaOH、、的说法正确的有(选填序号)a.均属于电解质 b.溶于水立即加入酚酞试液最终均为红色
c.均能通过化合反应一步生成 d.溶于水均伴随着放热现象
(2)、探究和的相互转化。实验1:加热碳酸氢钠固体,装置如下图所示。
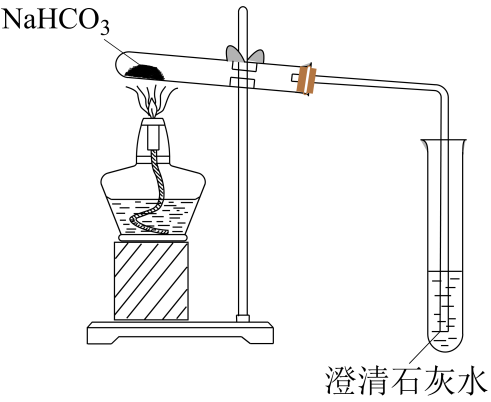
①利用上述装置可实现向的转化,被加热的试管中发生反应的化学方程式为。
实验2:分别向滴有2滴酚酞的和溶液中滴加稀盐酸,实验记录如下:
实验内容
实验现象

实验2-1
溶液浅红色褪去,立即产生大量气泡。

实验2-2
开始时,溶液的红色没有明显变化,电没有明显的气泡产生。继续滴加盐酸,当溶液的红色明显变浅时,气泡的数量血逐渐增多。当溶液的颜色变为浅红色,继续滴加盐酸,溶液的浅红色褪去,有大量气泡出现。
②实验2-1中,反应的离子方程式是。
③实验2-2中,实现碳酸钠向碳酸氢钠转化的现象是 , 反应的化学方程式:。
④碳酸也可实现上述转化,写出将通入溶液中发生反应的离子方程式:。