北京市丰台区2022-2023高二上学期期中考试化学(B卷)试题
试卷更新日期:2022-11-22 类型:期中考试
一、单选题
-
1. 下列装置或过程能实现化学能转化为电能的是( )




A.银锌纽扣电池
B.冶炼金属钠
C.太阳能电池
D.天然气燃烧
A、A B、B C、C D、D2. 由氢气和氧气反应生成水蒸气放出的热量,则反应:的为( )A、 B、 C、 D、3. 如图所示是两种常见的化学电源示意图,下列说法错误的是( ) A、甲电池属于一次电池 B、甲电池放电时,电子从锌简经外电路到石墨电极 C、乙电池的负极反应式为 D、乙电池充电时将电能转化为化学能4. 如图为以为电极的氢氧燃料电池的工作原理示意图,稀为电解质溶液。下列有关说法错误的是( )
A、甲电池属于一次电池 B、甲电池放电时,电子从锌简经外电路到石墨电极 C、乙电池的负极反应式为 D、乙电池充电时将电能转化为化学能4. 如图为以为电极的氢氧燃料电池的工作原理示意图,稀为电解质溶液。下列有关说法错误的是( ) A、b电极为电池的正极 B、a极的电极反应式: C、电池工作一段时间后,装置中增大 D、若将改为等物质的量的 , 消耗的用量增多5. 在298K、100kPa时,已知:
A、b电极为电池的正极 B、a极的电极反应式: C、电池工作一段时间后,装置中增大 D、若将改为等物质的量的 , 消耗的用量增多5. 在298K、100kPa时,已知:2H2O(g)=2H2(g)+O2(g) △H1
H2(g)+Cl2(g)=2HCl(g) △H2
2Cl2(g)+2H2O(g)=4HCl(g)+O2(g) △H3
则△H3与△H1和△H2间的关系正确的是:( )
A、△H3=△H1+2△H2 B、△H3=△H1+△H2 C、△H3=△H1-2△H2 D、△H3=△H1-△H26. P4(白磷,s)⇌4P(红磷,s) ΔH=-17kJ·mol-1 , 根据以上热化学方程式,下列推论正确的是( )A、正反应是一个吸热反应 B、白磷比红磷稳定 C、当1mol白磷完全转变成红磷时放出17kJ热量 D、当4g红磷转变成白磷时吸收17kJ热量7. 锌铜原电池装置如图,下列说法错误的是( ) A、锌电极上发生氧化反应 B、盐桥中的K+移向ZnSO4溶液 C、电子从锌片经电流计流向铜片 D、铜电极上发生反应:Cu2++2e−=Cu8. 已知反应CO(g)+Cl2(g)COCl2(g),反应过程中能量的变化如图所示,下列有关该反应的ΔH、ΔS的说法中正确的是( )
A、锌电极上发生氧化反应 B、盐桥中的K+移向ZnSO4溶液 C、电子从锌片经电流计流向铜片 D、铜电极上发生反应:Cu2++2e−=Cu8. 已知反应CO(g)+Cl2(g)COCl2(g),反应过程中能量的变化如图所示,下列有关该反应的ΔH、ΔS的说法中正确的是( ) A、ΔH<0 ΔS<0 B、ΔH>0 ΔS<0 C、ΔH<0 ΔS>0 D、ΔH>0 ΔS>09. 在一定温度下的恒容密闭容器中发生反应: , 下列证据能说明反应一定达到化学平衡状态的是( )A、单位时间内消耗 , 同时生成 B、体系内物质的总质量保持不变 C、同时在容器中存在 D、10. 下列铁制品防护的装置或方法中,错误的是( )
A、ΔH<0 ΔS<0 B、ΔH>0 ΔS<0 C、ΔH<0 ΔS>0 D、ΔH>0 ΔS>09. 在一定温度下的恒容密闭容器中发生反应: , 下列证据能说明反应一定达到化学平衡状态的是( )A、单位时间内消耗 , 同时生成 B、体系内物质的总质量保持不变 C、同时在容器中存在 D、10. 下列铁制品防护的装置或方法中,错误的是( )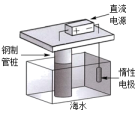

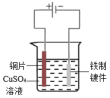

A.外加电流
B.牺牲阳极
C.表面镀铜
D.制成不锈钢
A、A B、B C、C D、D11. 对已达到化学平衡的反应 , 当其他条件不变时,减小压强时,对反应产生的影响是( )A、K值增大,平衡向正反应方向移动 B、K值减小,平衡向逆反应方向移动 C、K值不变,平衡向逆反应方向移动 D、K值不变,平衡向正反应方向移动12. 如图是一种应用广泛的锂电池,是电解质,是溶剂,反应原理是。下列说法错误的是( ) A、该装置将化学能转化为电能 B、电子移动方向是由a极流向b极 C、不可以用水代替作溶剂 D、b极反应式是13. 在恒容密闭容器中,放入镍粉并充入一定量的气体,一定条件下发生反应: , 已知该反应平衡常数与温度的关系如表:
A、该装置将化学能转化为电能 B、电子移动方向是由a极流向b极 C、不可以用水代替作溶剂 D、b极反应式是13. 在恒容密闭容器中,放入镍粉并充入一定量的气体,一定条件下发生反应: , 已知该反应平衡常数与温度的关系如表:温度/
25
80
230
平衡常数/
2
下列说法错误的是( )
A、上述生成的反应为放热反应 B、升高温度,的平衡转化率减小 C、时,反应的平衡常数为 D、时,测得 , 则反应达到平衡状态二、多选题
-
14. 利用含碳化合物合成燃料是解决能源危机的重要方法,已知反应过程中焓的变化情况如图所示。下列判断正确的是( )
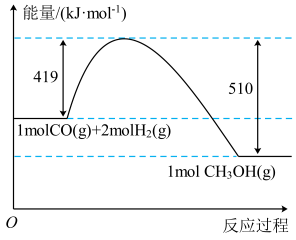 A、该反应的 B、和的总能量小于的能量 C、反应的 D、其他条件相同时,如果该反应生成液态 , 反应放出的能量减少
A、该反应的 B、和的总能量小于的能量 C、反应的 D、其他条件相同时,如果该反应生成液态 , 反应放出的能量减少三、填空题
-
15. 研究大气中含氮化合物、含硫化合物的转化具有重要意义。(1)、汽车发动机工作时会引发和反应,其能量变化示意图如下(常温常压下测定):

写出该反应的热化学方程式:。
(2)、土壤中的微生物可将大气中的经两步反应氧化成 , 两步反应的能量变化如图所示:
①第一步反应为反应(填“放热”或“吸热”),原因是。
②写出第二步反应的热化学方程式。
③结合两步反应过程,全部氧化成时的。
16. 合成氨对人类的生存和发展有着重要意义,1909年哈伯在实验室中首次利用氮气与氢气反应合成氨,实现了人工固氮。(1)、反应的化学平衡常数表达式为。(2)、请结合下列数据分析,工业上选用氮气与氢气反应固氮,而没有选用氮气和氧气反应固氮的原因是。序号
化学反应
的数值
①
②
(3)、如图是合成氨反应平衡混合气中的体积分数随温度或压强变化的曲线,图中、X分别代表温度或压强。其中X代表的是(填“温度”或“压强”);(填“>”“<”或“=”)原因是。
四、综合题
-
17. 电解原理有广泛的应用。(1)、如图所示,X、Y是惰性电极,a是饱和溶液,实验开始时,在电极两侧各滴入几滴酚酞。

①X极电极反应式是。X极附近观察到的现象是。
②检验Y电极产物的方法是。
(2)、若用如图所示装置进行粗铜的精炼,a是溶液。Y电极的材料是 , X极电极反应式是。(3)、二氧化氯()是一种黄绿色气体,是国际上公认的高效、广谱、快速、安全的杀菌消毒剂。如图是目前已开发出用电解法制取的新工艺。
①阳极产生的电极反应式是。
②当阴极产生标准状况下气体时,通过阳离子交换膜的离子的物质的量为。
18. 氢能是一种极具发展潜力的清洁能源,催化重整是目前大规模制取氢气的重要方法。(1)、 催化重整:反应I:
反应II:
①提高平衡转化率的条件是。
a.增大压强 b.加入催化剂 c.增大水蒸气浓度
②、催化重整生成、的热化学方程式是。
③已知时,反应的平衡常数。该温度下在密闭容器中,将与混合加热到反应发生,达到平衡时的浓度为 , 的转化率为。
(2)、实验发现,其他条件不变,相同时间内,向催化重整体系中投入一定量的可以明显提高的百分含量。做对比实验,结果如下图所示:
投入时,百分含量增大的原因是:。
(3)、反应中催化剂活性会因积炭反应而降低,相关数据如下表:反应
I
II
-173
①研究发现,如果反应I不发生积炭过程,则反应II也不会发生积炭过程。因此,若保持催化剂的活性,可适当采取降温的方法,请结合表中数据解释原因。
②如果均发生了I、II的积炭反应,通入过量水蒸气能有效清除积炭,反应的化学方程式是。
19. 利用电化学方法可以将有效地转化为(其中C元素的化合价为价),装置如图1所示。 (1)、在该装置中,左侧电极为(填“阴极”或“阳极”)。(2)、装置工作时,阴极除有生成外,还可能生成副产物降低电解效率。
(1)、在该装置中,左侧电极为(填“阴极”或“阳极”)。(2)、装置工作时,阴极除有生成外,还可能生成副产物降低电解效率。已知:电解效率
①副产物可能是(写出一种即可)。
②标准状况下,当阳极生成氧气体积为时,测得整个阴极区内的 , 电解效率为(忽略电解前后溶液的体积变化)。
(3)、研究表明,溶液会影响转化为的效率。如图2是 (以计)在水溶液中各种存在形式的物质的量分数随变化的情况。
①时,几乎未转化为 , 此时在溶液中的主要存在形式为。
②时,的转化效率较高,溶液中相应的电极反应式为。
-