江苏省无锡市梁溪区2022-2023学年九年级上学期期中化学试题
试卷更新日期:2022-11-15 类型:期中考试
一、单选题
-
1. 每年6月5日是“世界环境日”。下列做法不利于保护环境的是( )A、工业废水无色透明直接排放 B、垃圾分类回收成为新时尚 C、农药化肥科学合理施用 D、大力发展城市绿色公共交通2. 在探究蜡烛燃烧的奥秘时,小明提出:固体石蜡可能需要变成蒸气才能燃烧。这一过程属于科学探究中的( )A、提出问题 B、猜想与假设 C、收集证据 D、获得结论3. 市场上销售的食盐有加钙盐、加锌盐、加碘盐等,这里的“钙”“锌”“镁”指的是( )A、分子 B、元素 C、单质 D、离子4. 下列物质的用途与化学性质无关的是( )A、氧气用于医疗急救 B、稀有气体用作电光源 C、用氮气作食品的保护气 D、二氧化锰用作过氧化氢溶液分解的催化剂5. 下列是中国古代四大发明的某一工艺流程或应用,其中涉及化学变化的是( )A、火药:烟花燃放 B、印刷:活字排版 C、造纸:破布捣烂 D、司南:航海导向6. 用水壶烧开水,水沸腾后壶盖被顶起,说明( )A、分子是由原子构成的 B、分子的质量很小 C、分子的体积变大 D、分子间的间隔变大7. 下列化学用语书写正确的是( )A、氧化铁:FeO B、两个氯原子:Cl2 C、氦气:He2 D、一个铝离子:Al3+8. 下列物质中属于混合物的是( )A、五氧化二磷 B、铁水 C、矿泉水 D、臭氧9. 下列对实验现象的描述,正确的是( )A、铁丝在空气中燃烧,火星四射,生成黑色固体 B、木炭在氧气中燃烧生成黑色固体 C、红磷燃烧,产生大量白色烟雾 D、在蜡烛火焰上罩一个干而冷的小烧杯,烧杯内壁有水雾10. 下列关于过滤操作的叙述错误的是( )A、滤纸的边缘要低于漏斗口 B、液面不要低于滤纸的边缘 C、玻璃棒要靠在三层滤纸的一边 D、漏斗下端的管口要紧靠烧杯内壁11. 为纪念门捷列夫,将在1955年发现的一种新元素命名为“钔”,其在元素周期表中的有关信息如图所示,下列说法错误的是( )
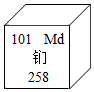 A、属于金属元素 B、相对原子质量是258g C、原子序数是101 D、元素符号是Md12. 下列实验操作中,正确的是( )A、
A、属于金属元素 B、相对原子质量是258g C、原子序数是101 D、元素符号是Md12. 下列实验操作中,正确的是( )A、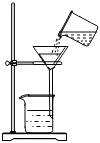 B、
B、 C、
C、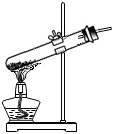 D、
D、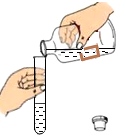 13. 下图是表示气体分子的示意图,图中“●”和“Ο”分别表示质子数不同的两种原子,其中表示化合物的是( )A、
13. 下图是表示气体分子的示意图,图中“●”和“Ο”分别表示质子数不同的两种原子,其中表示化合物的是( )A、 B、
B、 C、
C、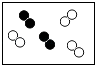 D、
D、 14. 推理是化学学习常用的思维方法之一,下列推理正确的是( )A、同种分子构成的物质一定是纯净物,纯净物一定由同种分子构成的 B、由同种元素组成的纯净物叫做单质,单质一定是由同种元素组成的 C、氧化物中含有氧元素,含氧元素的物质一定是氧化物 D、元素在形成化合物时,金属元素一定显正价,非金属元素一定显负价15. 装修材料能释放出有害的甲醛(化学式CH2O)气体,关于甲醛的说法正确的是( )A、甲醛由碳原子和水分子构成 B、甲醛分子中由一个碳原子、一个氢分子和一个氧原子构成 C、甲醛是由碳和水组成的 D、甲醛由碳、氢、氧三种元素组成的16. 分类是研究物质的常用方法。如图是纯净物、单质、化合物、氧化物 之间关系的形象表示,若整个大圈表示纯净物,则下列物质中属于Z范围的可能是( )
14. 推理是化学学习常用的思维方法之一,下列推理正确的是( )A、同种分子构成的物质一定是纯净物,纯净物一定由同种分子构成的 B、由同种元素组成的纯净物叫做单质,单质一定是由同种元素组成的 C、氧化物中含有氧元素,含氧元素的物质一定是氧化物 D、元素在形成化合物时,金属元素一定显正价,非金属元素一定显负价15. 装修材料能释放出有害的甲醛(化学式CH2O)气体,关于甲醛的说法正确的是( )A、甲醛由碳原子和水分子构成 B、甲醛分子中由一个碳原子、一个氢分子和一个氧原子构成 C、甲醛是由碳和水组成的 D、甲醛由碳、氢、氧三种元素组成的16. 分类是研究物质的常用方法。如图是纯净物、单质、化合物、氧化物 之间关系的形象表示,若整个大圈表示纯净物,则下列物质中属于Z范围的可能是( )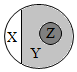 A、液氧 B、高锰酸钾 C、太湖水 D、氧化铁17. 蜡烛在如图所示密闭的集气瓶内燃烧至熄灭,测得瓶内氧气体积分数的变化如图所示。下列判断正确的是( )
A、液氧 B、高锰酸钾 C、太湖水 D、氧化铁17. 蜡烛在如图所示密闭的集气瓶内燃烧至熄灭,测得瓶内氧气体积分数的变化如图所示。下列判断正确的是( ) A、瓶内只要有氧气蜡烛就可以燃烧 B、蜡烛熄灭后集气瓶内只剩二氧化碳气体 C、蜡烛熄灭是因为容器内的氧气全部被消耗 D、燃烧过程中瓶内的水蒸气浓度会升高18. 下列知识整理的内容中三条都正确的选项是( )
A、瓶内只要有氧气蜡烛就可以燃烧 B、蜡烛熄灭后集气瓶内只剩二氧化碳气体 C、蜡烛熄灭是因为容器内的氧气全部被消耗 D、燃烧过程中瓶内的水蒸气浓度会升高18. 下列知识整理的内容中三条都正确的选项是( )A.物质构成
B.性质与用途
①分子、原子、离子都是构成物质的微粒②汞是由汞分子构成的
③原子都由质子、中子、电子构成
①氧气能支持燃烧:可作燃料②氮气化学性质不活泼:做保护气
③稀有气体化学性质不活泼:霓虹灯
C.实验操作
D.实验方法
①先查气密性,再装药品②气体先验纯,再点燃
③用滴管取液,先伸入液体,后挤压胶头
①鉴别O2、CO2---用澄清石灰水②熄灭酒精灯---用灯帽盖灭
③除去水中不溶性杂质---过滤
A、A B、B C、C D、D19. 萌萌同学对期中考试前的内容进行了梳理,归纳了以下知识点。①最外层电子数为8的粒子不一定是稀有气体元素的原子;
②质子数相同的两种粒子一定属于同种元素;
③分子和原子都不显电性;
④由一种元素组成的物质可能是混合物;
⑤同种元素在同种化合物中可显不同化合价。
其中说法正确的有( )
A、1 个 B、2 个 C、3 个 D、4 个20. 某同学误将少量KMnO4当成MnO2加入KClO3中进行加热制取氧气,部分物质质量随时间变化如图所示。下列关于该过程的说法正确的是( ) A、c代表氧气 B、t1时刻,KMnO4开始分解 C、t2时刻,开始有MnO2生成 D、高锰酸钾是氯酸钾分解的催化剂
A、c代表氧气 B、t1时刻,KMnO4开始分解 C、t2时刻,开始有MnO2生成 D、高锰酸钾是氯酸钾分解的催化剂二、填空题
-
21. 如图为某麦片的配料及营养成分表,请回答下列问题:
燕麦片营养成分表
项目
每100g
项目
每100g
能量
1606KJ
钠
8mg
蛋白质
11.4g
镁
110mg
脂肪
8.0g
锌
2.38mg
(1)、该麦片中含量最高的金属元素是。(2)、食用盐的主要成分为氯化钠,其阳离子符号为。(3)、麦片放久了会变质,食品变质实质上是与空气中的氧气发生了缓慢氧化,为了延长保质时间,可以把开封的麦片放入冰箱,这说明物质发生缓慢氧化的速率与有关。(4)、麦片在人体内会转化为葡萄糖(C6H12O6)为人体提供能量。葡萄糖由构成(填“分子”或“原子”或“离子”)。22. 生活离不开水。了解水的知识在日常生活中有着广泛的应用。(1)、自制净水器中常加入 , 用于除去水中异味和色素。(2)、自来水厂用二氧化氯消毒杀菌,二氧化氯的化学式为 , 二氧化氯中氯元素的化合价为。(3)、近年以来,江苏多地区启动深度净化江湖水替换地下水源供水,保障城乡居民饮水安全。太湖水自取水站经过沉淀、过滤、吸附、杀菌消毒,达到国家生活饮用水标准后,输送至千家万户。小侨同学通过向样品中加入的方法,判断自来水仍然是硬水。在生活中,饮用前可将其软化。23. 在宏观、微观和符号之间建立联系是化学特有的思维方式。根据电解水的实验,回答下列问题: (1)、从宏观上观察:如图所示,试管a和b中产生气体的体积比约为 , b中产生的气体是(填化学式)。(2)、从微观上分析:下列说法正确的是____(填字母)。A、水是由氢气和氧气组成的 B、水是由氢原子和氧原子构成的 C、每个水分子是由2个氢原子和1个氧原子构成的 D、化学反应的微观本质是分子破裂,原子重组(3)、从符号上表示:电解水的反应符号表达式:。24. 图甲是铝元素在元素周期表中的信息,图乙是几种微粒的结构示意图,请回答:
(1)、从宏观上观察:如图所示,试管a和b中产生气体的体积比约为 , b中产生的气体是(填化学式)。(2)、从微观上分析:下列说法正确的是____(填字母)。A、水是由氢气和氧气组成的 B、水是由氢原子和氧原子构成的 C、每个水分子是由2个氢原子和1个氧原子构成的 D、化学反应的微观本质是分子破裂,原子重组(3)、从符号上表示:电解水的反应符号表达式:。24. 图甲是铝元素在元素周期表中的信息,图乙是几种微粒的结构示意图,请回答:
 (1)、图甲中,铝元素的信息有一处不正确,请加以改正;(2)、铝原子的相对原子质量;(3)、图乙中,属于稀有气体的原子是(填序号,下同);(4)、图乙中,与铝不属于同一周期元素的是。
(1)、图甲中,铝元素的信息有一处不正确,请加以改正;(2)、铝原子的相对原子质量;(3)、图乙中,属于稀有气体的原子是(填序号,下同);(4)、图乙中,与铝不属于同一周期元素的是。三、综合题
-
25. 如下图是实验室制取氧气及探究其化学性质的装置图:

 (1)、写出标号①仪器的名称:①。(2)、实验室用双氧水和二氧化锰制取氧气应选用的发生装置是 , 反应的文字或符号表达式为 , 收集装置可选用D装置,理由是。如果用E装置收集氧气并测量氧气的体积,应用量筒收集(填“a”或“b”)出来的水。(3)、观察F装置中的实验现象:红磷在氧气中剧烈燃烧,放出热量,。这是因为生成(填化学式)的固体小颗粒的缘故。(4)、若用高锰酸钾制取氧气,写出该反应的文字或符号表达式:。要制取并收集较纯净的氧气应选的装置组合是。26. 如图所示:是以空气等为原料合成尿素[CO(NH2)2]的流程(部分产物略去),请回答:
(1)、写出标号①仪器的名称:①。(2)、实验室用双氧水和二氧化锰制取氧气应选用的发生装置是 , 反应的文字或符号表达式为 , 收集装置可选用D装置,理由是。如果用E装置收集氧气并测量氧气的体积,应用量筒收集(填“a”或“b”)出来的水。(3)、观察F装置中的实验现象:红磷在氧气中剧烈燃烧,放出热量,。这是因为生成(填化学式)的固体小颗粒的缘故。(4)、若用高锰酸钾制取氧气,写出该反应的文字或符号表达式:。要制取并收集较纯净的氧气应选的装置组合是。26. 如图所示:是以空气等为原料合成尿素[CO(NH2)2]的流程(部分产物略去),请回答: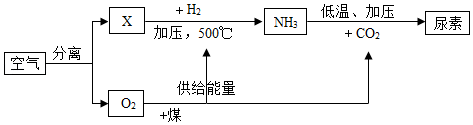 (1)、X和氢气合成氨气的符号表达式是;(2)、分离空气的常用方法有两种:
(1)、X和氢气合成氨气的符号表达式是;(2)、分离空气的常用方法有两种:Ⅰ、将空气液化后再汽化,液态空气汽化时首先分离出氮气。则沸点:N2O2(选填“>”或“=”或“<”)。
Ⅱ、利用分子筛吸附氮气和氧气能力的差异将二者进行分离。在吸附塔中,通过加压与减压的交替循环,可以使分子筛重复使用,部分过程的示意图如下:

①分子筛中发生的变化是(填“物理变化”或“化学变化”)。
②下列说法正确的是(填序号)。
A.变压吸附法制取的氧气中含有稀有气体
B.变压吸附法制取的氧气中含有二氧化碳
C.分子筛对氮气的吸附能力与吸附塔内气体压强有关
(3)、从环保角度考虑:下列保护空气的措施合理的是____(填标号)。A、工厂通过加高烟囱直接排放废气 B、及时清理和妥善处置工业、生活和建筑废渣,减少地面扬尘 C、提倡步行、骑自行车等“低碳”出行方式27. 阅读下面科普短文(改编自屠呦呦瑞典演讲稿)。很多中药古方都提到了青蒿入药抗疟疾,但当1971年开始从青蒿中提取有效成分时,结果却总是不理想。屠呦呦研究组反复研究中医古籍,其中“青蒿一握,以水两升渍,绞取汁,尽服之”激发了她的灵感。是不是高温下破坏了青蒿中抗疟的有效成分?屠呦呦立即改用乙醚在较低温度下进行提取,成功获得了抗疟有效单体的提纯物质,命名为青蒿素。
完成样品纯化后,通过元素分析、光谱测定、质谱及旋光分析等技术手段,测定相对分子质量为282,得出了青蒿素的化学式。但青蒿素的具体结构是什么样的呢?有机所的专家做了一个定性实验,加入淀粉碘化钾后,青蒿素溶液变为蓝色,说明青蒿素中含有过氧基团;而后专家又通过X射线衍射法等方法,最终确定了青蒿素是含有过氧基的新型倍半萜内酯(如图1)。
由于自然界中天然青蒿素的资源是有限的,接下来就要把自然界的分子通过人工合成制成药物。在这一过程中,研究组又有一项重大研究成果,获得了青蒿素的衍生物。衍生物之一是双青蒿素(如图2),它也具有抗疟的疗效,并且更加稳定,水溶性好,比青蒿素的疗效好10倍,进一步体现了青蒿素类药物“高效、速效、低毒”的特点。
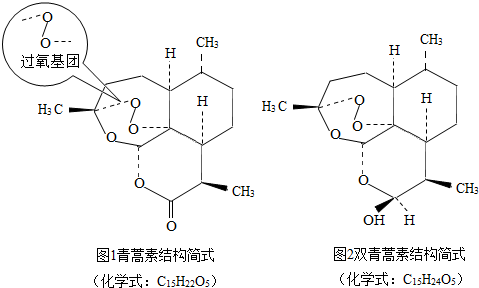
依据文章内容,回答下列问题:
(1)、屠呦呦用乙醚提取青蒿素,获得成功的关键在于改变了哪种条件:。(2)、向无色的青蒿素溶液中加入淀粉碘化钾,实验现象为。(3)、从中国古代青蒿入药,到2004年青蒿素类药物被世界卫生组织列为对抗疟疾的首选药物,经历了漫长的历程。将下列三项针对青蒿素的研究按时间先后排序(填数字序号)。①确定结构 ②分离提纯 ③人工合成
(4)、根据上述科普短文,下列说法正确的是____(填字母序号)。A、确定了青蒿素的组成元素,由此就可以确定青蒿素的化学式 B、青蒿素是含有过氧基的新型倍半萜内酯 C、由于自然界中有青蒿,因此我们应用青蒿素时只需从青蒿中提取即可28. 某化学兴趣小组对如下两个实验进行了探究:(1)、【实验一】某兴趣小组的同学利用图1所示装置对氯酸钾制氧气进行了深入的探究学习。查阅资料:
①氯酸钾的熔点约为356℃,二氧化锰的分解温度约为535℃。用酒精灯给物质加热,受热物质的温度一般约为400℃左右;
②氯酸钾分解时,传感器得到氧气浓度随温度的变化示意图(图2);不同配比时氧气浓度随温度的变化示意图(图3)。
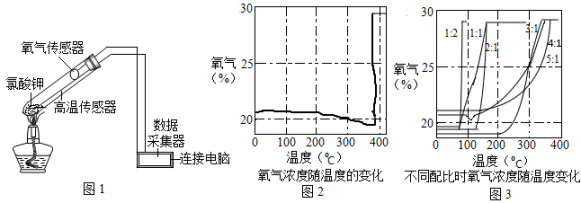
分析图2,氯酸钾熔点(填“高于”、“等于”或“低于”)其分解温度。
(2)、在老师的指导下,该小组同学继续进行深入探究。以氧气的体积分数为纵坐标,温度为横坐标,得到图3所示曲线(图中的配对比“1:2”、“1:1”、“2:1”、“3:1”、“4:1”、“5:1”指的是氯酸钾和二氧化锰的质量比)。根据图3,在上述反应中,两者配对比为时,氯酸钾分解温度最低。该反应的文字表达式或符号表达式为 , 基本类型是(填“化合反应”或“分解反应”)。(3)、为证实二氧化锰的催化作用,小组同学利用图4装置进行实验,步骤如下: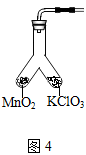
步骤Ⅰ:;
步骤Ⅱ:按照图4装入药品;
步骤Ⅲ:加热右侧支管,用带火星的木条在导管口检验生成的气体;
步骤Ⅳ:冷却后,将装置倾斜,使左侧支管中的药品进入右侧支管,
再加热右侧支管,用带火星的木条在导管口检验生成的气体。
(4)、【实验现象】步骤Ⅲ和步骤Ⅳ中,一段时间后都能观察到带火星的木条复燃,但木条复燃更快的是(选填“步骤Ⅲ”或“步骤Ⅳ”)(5)、【交流反思】要想确认分解氯酸钾制取氧气的反应中二氧化锰是催化剂,还需通过实验证明二氧化锰质量和在反应前后都没有发生变化。(6)、【实验二】该兴趣小组还利用压强传感器,对MnO2、CuO、Fe2O3、Cr2O3四种金属氧化物中、哪一种更适宜作过氧化氢制取氧气的催化剂,做了如下数字化实验探究。实验方案如下:
Ⅰ、用MnO2、CuO、Fe2O3、Cr2O3四种催化剂分别与海藻酸钠溶液混合,滴入氯化钙溶液制成含等质量催化剂、大小相同的海藻酸钠微球备用。
Ⅱ、取30粒含有MnO2海藻酸钠微球,采用图3装置进行实验。改用其他三种微球,分别重复上述实验,得到锥形瓶内压强随时间变化的曲线图如图5。

每次实验时,海藻酸钠微球数应相同的原因是控制相同。
(7)、从实验曲线(图6所示)分析,催化效果较好、反应温和的催化剂是。(8)、通过以上实验可知,催化剂的种类是影响过氧化氢溶液分解速率的因素之一。请你设计实验方案证明还有那些因素会影响过氧化氢溶液分解速率?。