福建省厦门市翔安区2022-2023学年九年级上学期期中化学试题
试卷更新日期:2022-11-15 类型:期中考试
一、单选题
-
1. 李克强总理在2021年《政府工作报告》中提出,2021年的重点工作之一是“加强污染防治和生态建设,持续改善环境质量”。下列做法不符合该理念的是( )A、城市道路喷洒水降尘,净化空气 B、改进燃煤锅炉烟囱,将废气排到高空 C、设计绿色化学工艺,减少水体污染 D、发展公共交通,提倡绿色出行2. 中华文化源远流长。下列工艺品的制作过程中一定发生了化学变化的是( )A、烧制唐三彩 B、裁剪纸窗花 C、雕刻石狮子 D、编制中国结3. 下列有关空气的说法正确的是( )A、洁净的空气属于纯净物 B、工业分离液态空气时发生化学变化 C、食品在空气中因与氧气发生缓慢氧化而变质 D、空气中的二氧化碳含量过高不会对环境造成影响4. 我国的稀土储量居世界第一位。稀土金属广泛应用在冶金、石油化工、材料工业等领域。钕(Nd)是一种制造导弹的稀土元素,钕元素在元素周期表中的信息如图所示。下列有关说法错误的是( )
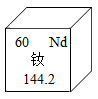 A、钕属于金属元素 B、钕原子中的质子数是60 C、钕原子的核外电子数是60 D、钕的相对原子质量是144.2 g5. 下列有关物质燃烧现象的描述,与事实不符的是( )A、白磷燃烧产生有毒气体 B、镁在空气中燃烧发出耀眼的白光 C、硫在氧气中燃烧发出蓝紫色火焰 D、木炭在氧气中燃烧发出白光6. 下列图示的实验操作中正确的是( )A、
A、钕属于金属元素 B、钕原子中的质子数是60 C、钕原子的核外电子数是60 D、钕的相对原子质量是144.2 g5. 下列有关物质燃烧现象的描述,与事实不符的是( )A、白磷燃烧产生有毒气体 B、镁在空气中燃烧发出耀眼的白光 C、硫在氧气中燃烧发出蓝紫色火焰 D、木炭在氧气中燃烧发出白光6. 下列图示的实验操作中正确的是( )A、 取少量氯化钠
B、
取少量氯化钠
B、 氧气的验满
C、
氧气的验满
C、 滴加液体
D、
滴加液体
D、 闻药品气味
7. 物质是由分子原子等微粒构成的,用分子的相关知识解释下列事实,错误的是( )A、金秋十月,丹桂飘香,是因为分子是不断运动的 B、6000升氧气被压缩在40升的钢瓶中,是因为分子之间有间隔 C、变瘪的乒乓球放入热水中能鼓起来,是因为分子大小随温度改变而改变 D、液氧和氧气都支持燃烧,是因为同种分子性质相同8. 用“
闻药品气味
7. 物质是由分子原子等微粒构成的,用分子的相关知识解释下列事实,错误的是( )A、金秋十月,丹桂飘香,是因为分子是不断运动的 B、6000升氧气被压缩在40升的钢瓶中,是因为分子之间有间隔 C、变瘪的乒乓球放入热水中能鼓起来,是因为分子大小随温度改变而改变 D、液氧和氧气都支持燃烧,是因为同种分子性质相同8. 用“ ”和“
”和“ ”表示不同元素的原子,下列微观示意图可以表示混合物的是( ) A、
”表示不同元素的原子,下列微观示意图可以表示混合物的是( ) A、 B、
B、 C、
C、 D、
D、 9. 小安整理出了空气成分的性质与用途的关系,其中错误的是( )A、氧气支持燃烧,常作宇宙航行中的重要燃料 B、氮气化学性质不活泼,可用作焊接金属的保护气 C、干冰易升华,可用于人工降雨 D、稀有气体化学性质不活泼,可用作灯泡的填充气体10. 加热一定量氯酸钾和二氧化锰混合物制取氧气。下列是有关物质质量和反应时间的关系坐标图,其中合理的是( )A、
9. 小安整理出了空气成分的性质与用途的关系,其中错误的是( )A、氧气支持燃烧,常作宇宙航行中的重要燃料 B、氮气化学性质不活泼,可用作焊接金属的保护气 C、干冰易升华,可用于人工降雨 D、稀有气体化学性质不活泼,可用作灯泡的填充气体10. 加热一定量氯酸钾和二氧化锰混合物制取氧气。下列是有关物质质量和反应时间的关系坐标图,其中合理的是( )A、 B、
B、 C、
C、 D、
D、
二、填空题
-
11. 回答问题(1)、用化学符号填空
①2个钙原子。②保持氧气化学性质的最小粒子。③构成氯化钠的微粒有。④氦气。⑤金元素。
(2)、写出下列符号的意义①2H。②Cu表示;。
12. 氧气是一种化学性质比较活泼的气体,它可以与许多物质发生化学反应,如图是探究氧气化学性质的实验装置。 (1)、B集气瓶中产生的现象是发出蓝紫色火焰,放出热量,产生一种有刺激性气味的气体,这种气体的名称是。(2)、装置B和C的集气瓶里都预先加入少量水,其目的各不相同。其中可以用细沙来代替水的是装置。(填序号)(3)、C集气瓶中发生的反应是(用符号表达式或文字表达式表示),该反应属于(填写基本反应类型),实验现象是。13. 碘是一种人体必需的微量元素,如图是碘离子(I-)的结构示意图。回答下列问题:
(1)、B集气瓶中产生的现象是发出蓝紫色火焰,放出热量,产生一种有刺激性气味的气体,这种气体的名称是。(2)、装置B和C的集气瓶里都预先加入少量水,其目的各不相同。其中可以用细沙来代替水的是装置。(填序号)(3)、C集气瓶中发生的反应是(用符号表达式或文字表达式表示),该反应属于(填写基本反应类型),实验现象是。13. 碘是一种人体必需的微量元素,如图是碘离子(I-)的结构示意图。回答下列问题: (1)、图中x=。(2)、碘属于元素(填“金属”或“非金属”)。碘元素在元素周期表中位于第周期。(3)、下图表示的粒子中,其元素的化学性质与碘元素化学性质相似的是(填标号)。
(1)、图中x=。(2)、碘属于元素(填“金属”或“非金属”)。碘元素在元素周期表中位于第周期。(3)、下图表示的粒子中,其元素的化学性质与碘元素化学性质相似的是(填标号)。 14. 空气和我们关系非常紧密。(1)、在市场上销售的香肠、盐水鸭等食品,常采用真空包装,在空气的成分中,能制造化肥并可以作保护气的是(填名称)。真空包装的目的是为了除去空气,使大多数微生物因缺少而受到抑制,防止食品发生变质。茶叶、膨化食品等采用充入防止食品变质的气体的方法,充入的气体能使食品保持原有的色、香、味及营养价值,防止食品受压而破碎变形,可将空气中的成分充入包装袋内。空气中二氧化碳的含量上升造成了。(2)、目前计入空气质量评价的主要污染物不包括(填字母,下同),向空气中排放的会造成酸雨。
14. 空气和我们关系非常紧密。(1)、在市场上销售的香肠、盐水鸭等食品,常采用真空包装,在空气的成分中,能制造化肥并可以作保护气的是(填名称)。真空包装的目的是为了除去空气,使大多数微生物因缺少而受到抑制,防止食品发生变质。茶叶、膨化食品等采用充入防止食品变质的气体的方法,充入的气体能使食品保持原有的色、香、味及营养价值,防止食品受压而破碎变形,可将空气中的成分充入包装袋内。空气中二氧化碳的含量上升造成了。(2)、目前计入空气质量评价的主要污染物不包括(填字母,下同),向空气中排放的会造成酸雨。a.一氧化碳 b.二氧化硫 c.二氧化碳 d.可吸入颗粒物(PM10) e.臭氧
(3)、测得某地某日的空气质量指数如下图,空气质量分级标准如下表,你认为当日的空气属于(填“优”“良”“轻度污染”或“中度污染”)。
空气质量指数
0-50
50-100
101-150
151-200
201-300
300以上
空气质量级别
一级
二级
三级
四级
五级
六级
空气质量状况
优
良
轻度污染
中度污染
重度污染
严重污染
(4)、为保护人类赖以生存的空气,我们可以做的是。(答出一点即可)15. 元素周期表中部分元素的相关信息如下图所示,回答下列问题。 (1)、16号元素属于(填“金属”或“非金属”)元素,它的最外层电子数为 , 它的离子符号是。(2)、在第三周期中,各元素的原子从左到右由易(填“得到”或“失去”下同)电子到易电子,最后是稳定结构。(3)、不同元素最本质的区别是;科学家宣布已人工合成了第116号元素,则此元素的核电荷数是。(4)、锂元素和钠元素的化学性质相似,是因为锂原子和钠原子的。(5)、地壳中含量最多的元素名称是 , 含量最多的金属元素名称是。
(1)、16号元素属于(填“金属”或“非金属”)元素,它的最外层电子数为 , 它的离子符号是。(2)、在第三周期中,各元素的原子从左到右由易(填“得到”或“失去”下同)电子到易电子,最后是稳定结构。(3)、不同元素最本质的区别是;科学家宣布已人工合成了第116号元素,则此元素的核电荷数是。(4)、锂元素和钠元素的化学性质相似,是因为锂原子和钠原子的。(5)、地壳中含量最多的元素名称是 , 含量最多的金属元素名称是。三、综合题
-
16. 在一个具有刻度一端密封和另一端有左右滑动的活塞的玻璃容器里放入一块白磷(足量),把密封管内的容积分为5等份。将玻璃容器固定好(见图,固定装置已省略),放在盛有80℃水的烧杯上(白磷燃烧所需的最低温度为40℃)进行实验,试回答:
 (1)、实验过程中,可以观察到的现象为:
(1)、实验过程中,可以观察到的现象为:①玻璃管内。
②活塞。
③活塞最后停在约刻度处,由此实验可得出的结论是。
(2)、写出玻璃容器内发生反应的符号表达式。(3)、以上实验可说明氮气的化学性质有(写一条即可)。(4)、测定的氧气的体积含量往往偏低,引起这种结果的原因可能是(写一条)。(5)、已知: , (固体),根据上述反应。能否用镁代替磷测定空气中氧气的成分 , 请说明理由:。17. 根据下列实验装置图,回答问题: (1)、数字标号①的仪器名称:;标号②的仪器名称:。(2)、实验室用氯酸钾和二氧化锰制取并收集纯净的O2 , 应选用的装置是 , 反应的文字或符号表达式为。(3)、用C和D组合制取氧气的符号表达式为。装置C和B比较,用分液漏斗代替长颈漏斗进行实验的优点是 , 排空气法收集O2验满的操作方法是:。(4)、如果使用G装置收集O2 , 应由口进入:如将装置中充满水,O2由口进入。(5)、实验室用加热氯化铵和氢氧化钙固体混合物的方法来制取氨气。氨气密度比空气密度小极易溶于水。则要选择的发生和收集装置是(填字母)。18. 某研究小组发现,将适量淀粉放入过氧化氢溶液中,过氧化氢溶液的分解速率会加快。对于此现象,该小组同学进行了如下探究:
(1)、数字标号①的仪器名称:;标号②的仪器名称:。(2)、实验室用氯酸钾和二氧化锰制取并收集纯净的O2 , 应选用的装置是 , 反应的文字或符号表达式为。(3)、用C和D组合制取氧气的符号表达式为。装置C和B比较,用分液漏斗代替长颈漏斗进行实验的优点是 , 排空气法收集O2验满的操作方法是:。(4)、如果使用G装置收集O2 , 应由口进入:如将装置中充满水,O2由口进入。(5)、实验室用加热氯化铵和氢氧化钙固体混合物的方法来制取氨气。氨气密度比空气密度小极易溶于水。则要选择的发生和收集装置是(填字母)。18. 某研究小组发现,将适量淀粉放入过氧化氢溶液中,过氧化氢溶液的分解速率会加快。对于此现象,该小组同学进行了如下探究:[提出问题]淀粉能否作为过氧化氢分解的催化剂?
[作出猜想]淀粉能作过氧化氢分解的催化剂。
[实验验证]
编号
实验操作
实验现象
①
向试管中加入过氧化氢溶液,再将带火星的小木条伸入试管中
小木条不复燃
②
向盛有过氧化氢溶液的试管中加入0.5g淀粉,再将带火星的小木条伸入试管中
产生大量气泡,小木条复燃
③
将②中反应结束,将试管中的剩余物质过滤、洗涤、干燥、称量
得固体物质0.5g
④
将③中所得固体放放试管中,重新加入过氧化氢溶液,然后将带火星的小木条伸入试管中
产生大量气泡,小木条复燃
(1)、 [分析数据、得出结论]实验①②的目的是证明;
(2)、实验③④证明淀粉的和在反应前后均未发生变化,可作过氧化氢分解的催化剂。(3)、[实验拓展]该小组设计了下图所示装置对比淀粉与二氧化锰的催化效果,实验均以生成25mL气体为准,其他可能的影响因素忽略不计,相关数据见下表:

实验编号
3%过氧化氢溶液的体积
其他物质质量
待测数据
I
20mL
淀粉0.5g
a
II
20mL
二氧化锰0.5g
b
上述实验中的“待测数据”是指 , 若最后结果证明二氧化锰的催化效果较好,则ab(填“<”、“>”或“=”)。
(4)、小明用坩埚钳夹取少量光亮的铜丝,放在酒精灯火焰上灼烧至表面变黑后,迅速插入装有20mL3%过氧化氢溶液的试管中,观察到试管内迅速产生大量气泡。且变黑的铜丝质量和化学性质不发生改变,于是得出结论:氧化铜可以加快过氧化氢分解。有同学认为这个结论不可靠,原因是过氧化氢的分解速率加快还可能与有关,请你设计实验方案证明。