福建省龙岩市上杭县西北片区2022-2023学年九年级上学期期中联考化学试题
试卷更新日期:2022-11-15 类型:期中考试
一、单选题
-
1. 下列生活事例中,主要过程为化学变化的是( )A、佳节到,焰火缤纷 B、功夫深,铁杵成针 C、春天来,冰雪消融 D、美酒开,满屋飘香2. “绿水青山就是金山银山”,下列做法符合要求的的是( )A、力推火力发电 B、焚烧塑料垃圾 C、推广使用公共自行车 D、工业废水就近排放3. 下列实验现象的描述中正确的是( )A、红磷在空气中燃烧时,产生大量的白雾 B、铁丝在空气中剧烈燃烧,火星四射 C、硫粉在氧气中燃烧时,产生淡蓝色火焰,生成有刺激性气味的无色气体 D、水通电一段时间后,正极与负极产生的气体体积比约为 1∶24. 下列实验操作正确的是( )A、
 量取 mL液体
B、
量取 mL液体
B、 检查装置的气密性
C、
检查装置的气密性
C、 加热试管中的液体
D、
加热试管中的液体
D、 点燃酒精灯
5. 甲醛 是室内主要的空气污染物,它是一种无色、有刺激性气味。下列关于甲醛说 法正确的是( )A、甲醛是一种混合物 B、甲醛的相对分子质量为30g C、甲醛分子中含有4个原子 D、甲醛由三种元素组成6. 铝在生产生活中的应用非常广泛,如图为铝在元素周期表中的信息和原子结构示意图,由此不能得到的信息是( )
点燃酒精灯
5. 甲醛 是室内主要的空气污染物,它是一种无色、有刺激性气味。下列关于甲醛说 法正确的是( )A、甲醛是一种混合物 B、甲醛的相对分子质量为30g C、甲醛分子中含有4个原子 D、甲醛由三种元素组成6. 铝在生产生活中的应用非常广泛,如图为铝在元素周期表中的信息和原子结构示意图,由此不能得到的信息是( ) A、铝元素的相对原子质量为 B、铝原子的质子数、核外电子数均为13 C、在化学变化中每个铝原子可失去 3 个电子变成 D、铝是地壳中含量最多的金属元素7. 最近科学家发现,水在﹣157℃超低温、正常压力或真空条件下仍呈液态,比蜂蜜还粘稠。下列关于这种“高密度液态水”的说法正确的是( )A、化学性质与普通水不同 B、分子不再运动 C、氢、氧两种原子的个数比为2:1 D、分子间的间隔比普通水大8. 用“
A、铝元素的相对原子质量为 B、铝原子的质子数、核外电子数均为13 C、在化学变化中每个铝原子可失去 3 个电子变成 D、铝是地壳中含量最多的金属元素7. 最近科学家发现,水在﹣157℃超低温、正常压力或真空条件下仍呈液态,比蜂蜜还粘稠。下列关于这种“高密度液态水”的说法正确的是( )A、化学性质与普通水不同 B、分子不再运动 C、氢、氧两种原子的个数比为2:1 D、分子间的间隔比普通水大8. 用“ ”和“
”和“  ”表示不同元素的原子,下列微观示意图能表示化合物的是( ) A、
”表示不同元素的原子,下列微观示意图能表示化合物的是( ) A、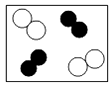 B、
B、 C、
C、 D、
D、 9. 建立模型是学习化学的重要方法。下列有关模型正确的是( )A、原子结构模型
9. 建立模型是学习化学的重要方法。下列有关模型正确的是( )A、原子结构模型 B、物质分类模型
B、物质分类模型 C、地壳中元素含量模型
C、地壳中元素含量模型 D、空气组成模型
D、空气组成模型 10. 下图能正确反映其对应操作中各种量的变化关系的是( )
10. 下图能正确反映其对应操作中各种量的变化关系的是( ) A、①加热一定质量的氯酸钾和二氧化锰的混合固体,生成氧气(符号为O2)的质量与反应时间的关系 B、②一定质量的硫粉在含有足量氧气的密闭容器中燃烧,容器中固体的质量随反应时间的变化关系 C、③用两份等质量、等浓度的过氧化氢溶液分别制取氧气(符号为O2) D、④加热一定质量的高锰酸钾制取氧气,试管中剩余固体的质量随反应时间的变化关系
A、①加热一定质量的氯酸钾和二氧化锰的混合固体,生成氧气(符号为O2)的质量与反应时间的关系 B、②一定质量的硫粉在含有足量氧气的密闭容器中燃烧,容器中固体的质量随反应时间的变化关系 C、③用两份等质量、等浓度的过氧化氢溶液分别制取氧气(符号为O2) D、④加热一定质量的高锰酸钾制取氧气,试管中剩余固体的质量随反应时间的变化关系二、填空题
-
11. 根据下列各式中“2”的含意,把它们的序号填人相应的空格内。
①2CO ② ③Mg2+ ④H2 ⑤2H ⑥2H+ ⑦
 ⑧
⑧  (1)、表示2个原子的是。(2)、表示2个分子的是。(3)、表示2个离子的是。(4)、表示1个分子由2个同种原子构成的是。(5)、表示该元素为正二价的是。(6)、表示该粒子带2个单位正电荷的是。(7)、表示最外电子层有2个电子的是。12. 化学源于生活,生活中很多现象蕴含着化学知识。(1)、中餐食材丰富、烹饪手法多样,深受大众喜爱。
(1)、表示2个原子的是。(2)、表示2个分子的是。(3)、表示2个离子的是。(4)、表示1个分子由2个同种原子构成的是。(5)、表示该元素为正二价的是。(6)、表示该粒子带2个单位正电荷的是。(7)、表示最外电子层有2个电子的是。12. 化学源于生活,生活中很多现象蕴含着化学知识。(1)、中餐食材丰富、烹饪手法多样,深受大众喜爱。①蒸紫薯,紫薯中含有的元素属于人体必需的常量元素的是(填字母序号)。
A.钙 B.铁 C.硒
②煮海带,海带中含有碘元素,适量摄入可预防(填字母序号)。
A佝偻病 B.坏血病 C.甲状腺肿大
(2)、照相机发明的最初,由于没有电子闪光灯,若曝光都需要使用镁粉的燃烧来完成,写出反应的表达式。13. 水是人类重要的自然资源,人类的生活、生产都离不开水。 (1)、自然界的水都不是纯水。自来水厂(如图甲)利用沉淀、过滤、和消毒等方法净化水。在实验室进行过滤操作时,需要用到的玻璃仪器有玻璃棒、烧杯、。(2)、取某小区等量的自来水和直饮水(如图乙),分别加入并搅拌,发现直饮水中有大量泡沫,没有浮渣,自来水中泡沫少且有浮渣,说明直饮水的硬度较(填“大”或“小”)。(3)、生活中硬水会带来许多麻烦,家庭生活中既能降低水的硬度,又可以杀菌消毒的方法是。(4)、某同学用电解水的方法探究水的组成,按图丙所示装置进行实验。电解时,该反应的表达式为;属于反应,此装置中a管产生的气体名称是 , 已知在相同条件下氧气在水中的溶解性强于氢气,那么,在a、b两玻璃管中气体的体积比的测定结果比2:1略(填“小”或“大”)。14. 按下图所示装置探究二氧化碳的性质并填空:
(1)、自然界的水都不是纯水。自来水厂(如图甲)利用沉淀、过滤、和消毒等方法净化水。在实验室进行过滤操作时,需要用到的玻璃仪器有玻璃棒、烧杯、。(2)、取某小区等量的自来水和直饮水(如图乙),分别加入并搅拌,发现直饮水中有大量泡沫,没有浮渣,自来水中泡沫少且有浮渣,说明直饮水的硬度较(填“大”或“小”)。(3)、生活中硬水会带来许多麻烦,家庭生活中既能降低水的硬度,又可以杀菌消毒的方法是。(4)、某同学用电解水的方法探究水的组成,按图丙所示装置进行实验。电解时,该反应的表达式为;属于反应,此装置中a管产生的气体名称是 , 已知在相同条件下氧气在水中的溶解性强于氢气,那么,在a、b两玻璃管中气体的体积比的测定结果比2:1略(填“小”或“大”)。14. 按下图所示装置探究二氧化碳的性质并填空: (1)、A中的实验现象说明CO2具有的化学性质是。(2)、B中的现象是 , 写出反应的文字表达式。(3)、C装置中干石蕊纸花不变色,湿石蕊纸花由紫色变红色的原因。
(1)、A中的实验现象说明CO2具有的化学性质是。(2)、B中的现象是 , 写出反应的文字表达式。(3)、C装置中干石蕊纸花不变色,湿石蕊纸花由紫色变红色的原因。三、综合题
-
15. 如图装置可用于测定空气中氧气的含量。请回答下列问题:
 (1)、红磷燃烧的表达式为 , 实验时红磷一定要足量或过量的目的是。(2)、待红磷熄灭并冷却后,打开弹簧夹,观察到瓶内水面上升约 , 由此得出结论:氧气体积约占空气体积的。(3)、实验前一定要。16. 如图是实验室制取气体的装置,请回答问题:
(1)、红磷燃烧的表达式为 , 实验时红磷一定要足量或过量的目的是。(2)、待红磷熄灭并冷却后,打开弹簧夹,观察到瓶内水面上升约 , 由此得出结论:氧气体积约占空气体积的。(3)、实验前一定要。16. 如图是实验室制取气体的装置,请回答问题: (1)、写出编号仪器名称:① , ②;(2)、图中的收集装置中,不能用来收集氧气的是(填字母),理由是;(3)、实验室用高锰酸钾制取氧气,应选择的发生装置是(填字母),反应的表达式为;若要收集一瓶较纯净应选择的收集装置是(填字母),能用该装置收集的理由是;进行该实验时要在靠近试管口的地方放一团棉花,这是为了防止加热时。由于氧气的密度比空气 , 所以盛满氧气的集气瓶口应盖上玻璃片,立在桌上。(4)、实验室用装置 A制取二氧化碳时,检查装置气密性的方法为:用弹簧夹夹紧橡胶导管,向长颈漏斗中注水,若出现现象,则证明气密性良好。该反应的表达式为。(5)、用C或D装置收集气体时导管末端要伸到集气瓶底部的目的是。17.(1)、FeCl3溶液能对过氧化氢的分解起催化作用。某小组拟在相同浓度FeCl3溶液的催化下,探究过氧化氢浓度对过氧化氢分解速率的影响。写出本实验发生反应的化学式表达式;(2)、Ⅰ.分别取相同体积、不同浓度的过氧化氢溶液于锥形瓶中,注入相同体积、相同浓度的FeCl3溶液,如图观察到 , 就可以粗略判断,得出实验结果。
(1)、写出编号仪器名称:① , ②;(2)、图中的收集装置中,不能用来收集氧气的是(填字母),理由是;(3)、实验室用高锰酸钾制取氧气,应选择的发生装置是(填字母),反应的表达式为;若要收集一瓶较纯净应选择的收集装置是(填字母),能用该装置收集的理由是;进行该实验时要在靠近试管口的地方放一团棉花,这是为了防止加热时。由于氧气的密度比空气 , 所以盛满氧气的集气瓶口应盖上玻璃片,立在桌上。(4)、实验室用装置 A制取二氧化碳时,检查装置气密性的方法为:用弹簧夹夹紧橡胶导管,向长颈漏斗中注水,若出现现象,则证明气密性良好。该反应的表达式为。(5)、用C或D装置收集气体时导管末端要伸到集气瓶底部的目的是。17.(1)、FeCl3溶液能对过氧化氢的分解起催化作用。某小组拟在相同浓度FeCl3溶液的催化下,探究过氧化氢浓度对过氧化氢分解速率的影响。写出本实验发生反应的化学式表达式;(2)、Ⅰ.分别取相同体积、不同浓度的过氧化氢溶液于锥形瓶中,注入相同体积、相同浓度的FeCl3溶液,如图观察到 , 就可以粗略判断,得出实验结果。
为进一步判断上述实验结论的准确性,运用上图,小刚同学进行了如下实验方案设计。
(3)、Ⅱ.[方案一]在不同过氧化氢浓度下,测定收集相同气体体积所需时间。[方案二]在不同过氧化氢浓度下,测定;
方案二的实验测量结果:
物理量实验序号
30%H2O2溶液
的体积(mL)
2%FeCl3溶液
的体积(mL)
加入H2O的
体积(mL)
反应的时间
(min)
生成O2
的体积(mL)
1
5
x
20
5
V1
2
10
3
15
5
V2
表中x=;
实验结论:通过测量,若V1V2(填“>”、“=”或“<”),说明。
四、计算题
-
18. 计算下列物质的相对分子质量(1)、KMnO4。(2)、CaCO3。