2022-2023初中化学下学期第八单元金属和金属材料 课题1 金属材料 课堂训练
试卷更新日期:2022-11-12 类型:同步测试
一、单选题
-
1. 菜刀用铁制而不用铝制的主要原因是( )。A、铁的硬度大,铝的硬度小 B、铁的熔点高,铝的熔点低 C、铁的密度大,铝的密度小 D、铁的导电性差,铝的导电性好2. 金属和金属材料的性质在很大程度上决定了它们的用途。下列说法错误的是( )。A、不锈钢抗腐蚀性好,常用于制造医疗器械 B、铁具有良好的导热性,可用于制造炊具 C、焊锡的熔点较低、电阻率较大,常用于制成发热体 D、硬铝轻而坚韧,可作为制造汽车、飞机和火箭的材料3. 下列物质不属于合金的是()A、不锈钢杯 B、黄铜 C、铁矿石 D、生铁4. 下列有关合金的叙述,正确的是( )
①合金中至少含两种金属
②合金中的元素以化合物形式存在
③合金中一定含有金属
④合金一定是混合物
⑤生铁是含杂质较多的铁合金
⑥合金的强度和硬度一般比组成它们的纯金属更高,抗腐蚀性能等也更好
A、①②③④⑤⑥ B、①② C、①③④ D、③④⑤⑥5. 在选择铸造硬币的金属材料时,不需要考虑的因素是( )A、 硬度 B、导电性 C、耐腐蚀性 D、与硬币面值相应的价值6. 1989年世界卫生组织把铝定为食品污染源之一,铝在下列应用中应当控制的是( )①制铝合金;②制导线;③制炊具;④银银色涂料;⑤明矾净水;⑥明矾与苏打制食品膨松剂;⑦易拉罐;⑧用氢氧化铝凝胶制胃舒平药品;⑨包装糖果和小食品
A、仅③⑤⑧⑨ B、仅⑥⑧⑨ C、仅③⑤⑨ D、仅③⑤⑥⑦⑧⑨7. 下列说法中错误的是( )A、生铁可以用来炼钢 B、铁在氧气中燃烧生成黑色的四氧化三铁 C、生铁和钢都是铁的单质 D、钢的性能优于生铁8. 如图所示,说明中出现了金属材料的是( )A、 “东方之冠”的氟碳涂料
B、
“东方之冠”的氟碳涂料
B、 “阳光谷”的方形钢管
C、
“阳光谷”的方形钢管
C、 石油馆外表的聚碳酸酯
D、
石油馆外表的聚碳酸酯
D、 江西馆外表的青花瓷
9. 从金属利用的历史来看,先是青铜器时代,而后是铁器时代,铝的利用是近百年的事.这个先后顺序主要跟下列有关的是( )
江西馆外表的青花瓷
9. 从金属利用的历史来看,先是青铜器时代,而后是铁器时代,铝的利用是近百年的事.这个先后顺序主要跟下列有关的是( )①地壳中的金属元素的含量;②金属活动性顺序;③金属的导电性;④金属冶炼的难易程度;⑤金属的延展性.
A、①③ B、②⑤ C、③⑤ D、②④10. 下列不属于合金的是( )A、焊锡 B、黄铜 C、生铁 D、石墨二、填空题
-
11. 中国手机厂商中兴推出了极具创新式的折叠手机-Axon m,如图是中兴可折叠手机,请回答下列问题。
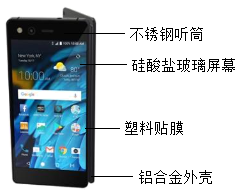 (1)、图中所示部件中属于有机合成材料的是(2)、用铝合金作手机外壳的优点是。(3)、不锈钢属于(填“纯净物”或“混合物”),请写出一个能证明铝金属活动性比铜强的化学反应方程式:。12. 我们的日常生活用品,很多都是由金属材料制成的。例如:体温计中的液体是;制造导线一般是用;水龙头表面镀的一般是;炒菜锅最好用制作;灯泡里的灯丝是;一种合金与人体具有很好的“相容性”,可以用来制造“人造骨”的是。(以上空格均写物质的名称)13. 导电性最强的金属是;硬度最大的金属;熔点最高的金属;熔点最低的金属;人体中含量最高的金属;地壳中含量最高的金属。14. 请说出导致下列差异的因素.
(1)、图中所示部件中属于有机合成材料的是(2)、用铝合金作手机外壳的优点是。(3)、不锈钢属于(填“纯净物”或“混合物”),请写出一个能证明铝金属活动性比铜强的化学反应方程式:。12. 我们的日常生活用品,很多都是由金属材料制成的。例如:体温计中的液体是;制造导线一般是用;水龙头表面镀的一般是;炒菜锅最好用制作;灯泡里的灯丝是;一种合金与人体具有很好的“相容性”,可以用来制造“人造骨”的是。(以上空格均写物质的名称)13. 导电性最强的金属是;硬度最大的金属;熔点最高的金属;熔点最低的金属;人体中含量最高的金属;地壳中含量最高的金属。14. 请说出导致下列差异的因素.(1)生铁和钢都是铁合金,但性能不同,原因是 ;
(2)CO与CO2都是由碳和氧两种元素组成的,但化学性质不同,原因是;
(3)钠原子和钠离子的化学性质不同,原因是;
(4)氧元素和碳元素的元素种类不同,原因是 ;
(5)石墨与金刚石都是碳元素组成的单质,但物理性质差异较大,原因是 .
15. 生铁和钢都是 合金.要使生铁变成钢,必须降低生铁中的 含量,调整的含量,除去等有害杂质.纯铁 ,不宜用来制造机械和其他用品;生铁中的白口铁缺点是 ,不宜铸造和机械加工;灰口铁强度 ,不能煅轧;钢较硬,具有良好 性、 性、 性,可以煅轧和铸造.
三、简答题
-
16. 金属材料在生活、生产中应用十分广泛。

(1)、图①是金属的一个应用实例,请说出利用了金属的什么物理性质。(答出一点即可)(2)、图②中两块金属片互相刻划后,在纯铜片上有明显的划痕。该实验探究的目的是什么?得到什么结论?(3)、请你举一实例说明合金的用途比纯金属更广泛。17. 生活中常用的硬币都是合金制成的,其中一元硬币为钢芯镀镍合金,五角硬币为铜锌合金和铜芯镀铜合金.请说出用来铸造硬币的合金需要具有哪些性质.(答出三点)四、综合题
-
18. 化学不仅支持高新技术的快速发展,还为解决能源、资源等问题提供有效途径。(1)、2019年1月,嫦娥四号登月探测器成功登陆月球表面。构成月球探测器的部件有碳化硅光学仪器、有机高分子反光板、钛合金筛网车轮等,其中碳化硅SiC属于材料。(2)、港珠澳大桥在建造过程中使用了大量的不锈钢钢筋,主要利用了其强度高和的性质。(3)、将生活垃圾中的可燃物分离出来对其进行处理可以得到汽油、煤油等燃料,从而实现资源的循环再利用。下列生活垃圾中能实现上述转化的有 填序号 。
a废铁
b玻璃
c易拉罐
d废塑料
(4)、太阳能的利用为人类提供充足的氢能源。工业上以太阳能为能源,利用铁的氧化物循环分解水制氢气的流程如图所示:
①过程Ⅰ、Ⅱ中能量转化的形式依次是太阳能 热能。
②写出过程Ⅱ反应的化学方程式。
③当过程Ⅱ中得到agH2时,过程I中得到的O2质量为g。
五、实验探究题
-
19. 金属和金属材料在生产、生活中有广泛的用途,请用金属的有关知识填空.
 (1)、锂电池可作为无人机的动力,其工作原理是:FePO4+Li=LiFePO4 。在LiFePO4中锂元素显+1价,磷元素显+5价,则铁元素的化合价是。
(1)、锂电池可作为无人机的动力,其工作原理是:FePO4+Li=LiFePO4 。在LiFePO4中锂元素显+1价,磷元素显+5价,则铁元素的化合价是。
(2)、钛(Ti)具有硬度大,密度小,熔点高,抗腐蚀性能好等优良性能,被誉为“未来金属”。已知Ti2(SO4)3溶于水溶液呈紫色。Ti2O3(紫黑色固体)在加热条件下可溶于硫酸,生成Ti2(SO4)3 。可观察的现象是 , 反应的化学方程式为 。
(3)、工业上,用一氧化碳和赤铁矿炼铁的化学方程式为 , 计算用1000t含氧化铁80%的赤铁矿石,理论上能冶炼出铁的质量为t。
(4)、黄铜片(铜锌合金)与铜片互相刻划时,(如图1所示),纯铜片上留下明显的划痕,说明 ;将它们分别放入稀硫酸中能产生气泡的是;涉及的化学反应可用化学方程式表示为 。
20. 化学课上我们曾经观察过如图所示的实验. (1)、实验中,铜片上的白磷很快燃烧,其化学反应方程式为 .
(1)、实验中,铜片上的白磷很快燃烧,其化学反应方程式为 .
(2)、该实验主要利用了铜片良好的性.(3)、烧杯中的水在实验中没有起到的作用是 (填序号).A、作反应物 B、隔绝空气 C、升高温度.
-