新疆昌吉市教育共同体2022-2023学年高一上学期第一次月考化学试题
试卷更新日期:2022-11-09 类型:月考试卷
一、单选题
-
1. 下列各组物质,前者是酸后者是氧化物的是( )A、CaCO3、H2O2 B、HNO3、CaO C、NaHCO3、Ca(OH)2 D、CO2、HCl2. 下列离子方程式书写正确的是( )A、与反应: B、与反应: C、与Ba(OH)2反应: D、金属钠与水反应:3. 下列反应中,电子转移发生在同种物质的同种元素之间的是( )A、2H2S+SO2=3S+2H2O B、2KMnO4K2MnO4+MnO2+O2↑ C、2KClO32KCl+3O2↑ D、Cu2O+H2SO4=CuSO4+Cu+H2O4. 下列过程需要加入还原剂才能实现的是( )A、Fe2+ → Fe3+ B、KMnO4→Mn2+ C、CO2 → CO D、H2S→SO25. 分类是科学研究的重要方法,下列物质分类正确的是( )A、混合物:澄清石灰水、纯净矿泉水、小苏打 B、同素异形体:臭氧、氧气、 C、非电解质:乙醇、二氧化碳、SO3、葡萄糖 D、化合物:冰水混合物、烧碱、75%医用酒精、石膏6. 随着人们对物质组成和性质研究的深入,物质的分类更加多样化。下列有关说法正确的是( )A、Na2O、Mn2O7、Fe2O3都是碱性氧化物 B、磁铁矿、盐酸、胆矾都是混合物 C、SO2、SO3、CO2都是酸性氧化物 D、烧碱、纯碱、熟石灰都是碱7. 在某透明的强酸性溶液中,能大量共存的无色离子组是( )A、K+、Na+、Cu2+、SO B、Na+、Al3+、Cl-、NO C、Na+、K+、CO、Cl- D、K+、SO、Cl-、Ba2+8. 下列反应不属于氧化还原反应的是( )A、 B、 C、Fe2O3+3CO2Fe+3CO2 D、2KMnO4K2MnO4+MnO2+O2↑9. 下列氧化还原反应中,表示电子转移的方向和数目正确的是( )A、
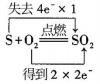 B、
B、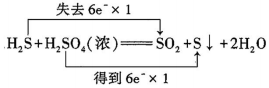 C、
C、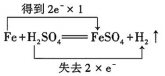 D、
D、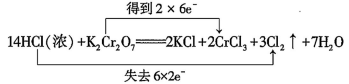 10. 科学家开发出一种低成本光伏材料——蜂窝状石墨烯,生产原理为:Na2O+2CO=Na2CO3+C(石墨烯)。下列说法正确的是( )A、该生产石墨烯的反应属于置换反应 B、石墨烯和金刚石是同素异形体 C、CO在该反应中只做还原剂 D、Na2O属于碱性氧化物,CO属于酸性氧化物11. 下列电离方程式书写正确的是( )A、在熔融状态下: B、加热至熔化: C、溶于水中: D、溶于水中:12. 下列反应可以用同一离子方程式表示的是( )A、溶液溶液,溶液溶液 B、溶液溶液,溶液+溶液 C、溶液溶液,溶液溶液 D、溶液,溶液溶液13. 对于反应3Cl2+6NaOH(热)=5NaCl+NaClO3+3H2O,下列叙述正确的是( )A、Cl2是氧化剂,NaOH是还原剂 B、被氧化的氯原子和被还原的氯原子的个数比为5∶1 C、Cl2既是氧化剂又是还原剂 D、氧化剂的得电子数与还原剂的失电子数之比为5∶114. 符合图中阴影部分的物质是( )
10. 科学家开发出一种低成本光伏材料——蜂窝状石墨烯,生产原理为:Na2O+2CO=Na2CO3+C(石墨烯)。下列说法正确的是( )A、该生产石墨烯的反应属于置换反应 B、石墨烯和金刚石是同素异形体 C、CO在该反应中只做还原剂 D、Na2O属于碱性氧化物,CO属于酸性氧化物11. 下列电离方程式书写正确的是( )A、在熔融状态下: B、加热至熔化: C、溶于水中: D、溶于水中:12. 下列反应可以用同一离子方程式表示的是( )A、溶液溶液,溶液溶液 B、溶液溶液,溶液+溶液 C、溶液溶液,溶液溶液 D、溶液,溶液溶液13. 对于反应3Cl2+6NaOH(热)=5NaCl+NaClO3+3H2O,下列叙述正确的是( )A、Cl2是氧化剂,NaOH是还原剂 B、被氧化的氯原子和被还原的氯原子的个数比为5∶1 C、Cl2既是氧化剂又是还原剂 D、氧化剂的得电子数与还原剂的失电子数之比为5∶114. 符合图中阴影部分的物质是( ) A、 B、 C、 D、15. 下列物质间的转化通过一步反应不能实现的是( )A、CaO →Ca(OH)2 B、CuO→Cu(OH)2 C、Ca(OH)2→CaCO3 D、CuSO4→FeSO416. 下列说法正确的是( )A、BaSO4难溶于水,其水溶液导电能力极弱,所以硫酸钡是弱电解质 B、CO2溶于水得到的溶液能导电,所以CO2是电解质 C、强电解质溶液的导电能力不一定比弱电解质溶液的导电能力强 D、导电能力强的溶液一定是强电解质溶液17. 向Ba(OH)2溶液中逐滴加入等浓度的稀硫酸,溶液导电性变化合理的图像为( )A、
A、 B、 C、 D、15. 下列物质间的转化通过一步反应不能实现的是( )A、CaO →Ca(OH)2 B、CuO→Cu(OH)2 C、Ca(OH)2→CaCO3 D、CuSO4→FeSO416. 下列说法正确的是( )A、BaSO4难溶于水,其水溶液导电能力极弱,所以硫酸钡是弱电解质 B、CO2溶于水得到的溶液能导电,所以CO2是电解质 C、强电解质溶液的导电能力不一定比弱电解质溶液的导电能力强 D、导电能力强的溶液一定是强电解质溶液17. 向Ba(OH)2溶液中逐滴加入等浓度的稀硫酸,溶液导电性变化合理的图像为( )A、 B、
B、 C、
C、 D、
D、 18. 已知反应2FeCl3+Cu=CuCl2+2FeCl2 , 则下列判断正确的是( )A、该反应是置换反应 B、该反应中FeCl3作还原剂 C、氧化性:CuCl2>FeCl3 D、Cu发生了氧化反应19. 有关氧化还原反应的说法正确的是( )A、氧化剂的氧化性大于氧化产物的氧化性 B、一种元素被氧化,一定有另一种元素被还原 C、同种元素化合价不可能变化 D、生成物中可能出现还原剂20. 常温下,在溶液中可发生以下反应:①2Fe2++Br2=2Fe3++2Br﹣②2Br﹣+Cl2=Br2+2Cl﹣③2Fe3++2I﹣=2Fe2++I2 , 由此判断下列说法正确的是( )A、铁元素在反应①中被还原,在③中被氧化 B、反应②中当有1 个Cl2分子被氧化时,有2 个Br-被还原 C、氧化性强弱顺序为Cl2>I2>Br2>Fe3+ D、还原性强弱顺序为I->Fe2+>Br->Cl-
18. 已知反应2FeCl3+Cu=CuCl2+2FeCl2 , 则下列判断正确的是( )A、该反应是置换反应 B、该反应中FeCl3作还原剂 C、氧化性:CuCl2>FeCl3 D、Cu发生了氧化反应19. 有关氧化还原反应的说法正确的是( )A、氧化剂的氧化性大于氧化产物的氧化性 B、一种元素被氧化,一定有另一种元素被还原 C、同种元素化合价不可能变化 D、生成物中可能出现还原剂20. 常温下,在溶液中可发生以下反应:①2Fe2++Br2=2Fe3++2Br﹣②2Br﹣+Cl2=Br2+2Cl﹣③2Fe3++2I﹣=2Fe2++I2 , 由此判断下列说法正确的是( )A、铁元素在反应①中被还原,在③中被氧化 B、反应②中当有1 个Cl2分子被氧化时,有2 个Br-被还原 C、氧化性强弱顺序为Cl2>I2>Br2>Fe3+ D、还原性强弱顺序为I->Fe2+>Br->Cl-二、填空题
-
21. 下列物质①Cu ②SO2 ③NaCl溶液 ④HCl ⑤BaSO4 ⑥NH3 ⑦酒精 ⑧硫酸溶液 ⑨NaOH(1)、其中属于电解质的有;(2)、属于非电解质的有;(3)、能导电的有;(4)、③和④能否发生离子反应(填“能”或“不能”)22. 某课外活动小组进行Fe(OH)3胶体的制备实验并检验其相关性质。(1)、若将饱和FeCl3溶液分别滴入下列物质中,能形成胶体的是____;A、NaOH浓溶液 B、NaCl浓溶液 C、冷水 D、沸水(2)、从下列选项中选择适当的字母填空:
A.渗析 B.聚沉 C.电泳 D.丁达尔现象
①氢氧化铁胶体呈红褐色,插入两个惰性电极,通直流电一段时间,阴极附近的颜色逐渐变深,这种现象叫。
②强光通过氢氧化铁胶体,可看到光带,这种现象叫。
③淀粉与食盐的混合液放在肠衣中,并把它悬挂在盛有蒸馏水的烧瓶里,从而使淀粉与食盐分离,这种方法。
④若取少量制得的胶体加入试管中,加入硫酸铵溶液,产生红褐色沉淀,这种现象称为胶体的。
(3)、Fe(OH)3胶体区别于FeCl3溶液最本质的特征是____;A、Fe(OH)3胶体是均一的分散系 B、Fe(OH)3胶体具有丁达尔效应 C、Fe(OH)3胶体粒子的直径在1~100nm之间 D、Fe(OH)3胶体的分散质粒子能透过滤纸(4)、将制得的胶体放入半透膜制成的袋内,如图所示,放置2min后,取少量半透膜外的液体于试管中,置于暗处,用一束强光从侧面照射,观察(填“有”或“无 ”)丁达尔现象,再向试管中加入用稀硝酸酸化的硝酸银溶液,可观察到的现象为(填序号)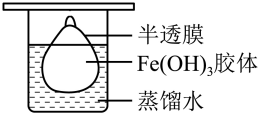
A.无明显现象 B.有白色沉淀产生
三、综合题
-
23. A和B两支试管所盛的溶液中共含有K+、Ag+、Mg2+、Cl−、OH−、六种离子,向试管A的溶液中滴入酚酞溶液,溶液呈红色。
请回答下列问题:
(1)、若向某试管中滴入稀盐酸产生沉淀,则该试管为(填“A”或“B”)。(2)、若向试管B的溶液中加入合适的药品,过滤后可以得到相应的金属和仅含一种溶质的溶液,则加入的药品是(填化学式)。(3)、若将试管A和试管B中的溶液按一定体积比混合后过滤,蒸干所得滤液可得到一种纯净物,则混合过程中发生反应的离子方程式为、(不考虑Ag+与OH−的反应)。(4)、配平下列氧化还原反应方程式 H2S +
H2S +  HNO3(稀) =
HNO3(稀) =  H2O +
H2O +  S↓+
S↓+  NO↑24. 按要求填空,已知反应:
NO↑24. 按要求填空,已知反应:①SO3+H2O=H2SO4
②3NO2+H2O=2HNO3+NO
③2F2+2H2O=4HF+O2
④2Na+2H2O=2NaOH+H2↑
⑤Na2O+2HCl=2NaCl+H2O
⑥Al2O3+2NaOH=2NaAlO2+H2O
(1)、上述反应不属于氧化还原反应的有(填序号,下同)。H2O被氧化的是 , H2O被还原的是 , 属于氧化还原反应,但其中的H2O既不被氧化又不被还原的是。(2)、在3Cu+8HNO3(稀)=3Cu(NO3)2+2NO↑+4H2O反应中,是还原剂;元素被还原。用双线桥表示电子的转移:(3)、用双线桥法表示反应②的电子转移方向和数目:。(4)、用单线桥法表示反应③的电子转移方向和数目:。(5)、写出反应④的离子方程式:。