山东省烟台市牟平区2021-2022学年九年级上学期期末化学试题
试卷更新日期:2022-11-07 类型:期末考试
一、单选题
-
1. 下列关于金属的说法正确的是( )A、人类使用金属铝的年代早于钢、铁 B、“真金不怕火炼”表明金在高温条件下也很难与氧气反应 C、通过高炉炼得的铁为纯铁 D、生铁是铁和碳的化合物2. 除去下列物质中混有的少量杂质(括号内为杂质),拟定的实验方案不可行的是( )A、FeCl2溶液(CuCl2)—加入过量的铁粉,过滤 B、KNO3固体(NaCl)—蒸发结晶,过滤 C、CO气体(CO2)—通过足量的NaOH溶液,并干燥 D、NaCl溶液(MgCl2)—加入过量的NaOH溶液,过滤,滤液中加稀盐酸至pH=73. 下列化学反应在生活、生产中应用的观点错误的是( )A、治疗胃酸过多可用呈碱性的氢氧化钠 B、毒虫的毒液中含蚁酸,人被叮咬后可除抹肥皂水之类的碱性物质以减轻痛痒 C、酸性土壤可加熟石灰进行改良 D、开水壶或热水瓶内的水垢可用温热的食醋浸泡清洗4. 下列有关物质的比较推理中正确的是( )A、酸能使石蕊试液变红,二氧化碳也能使石蕊试液变红,所以二氧化碳是酸 B、NaCl和NaNO2都是有咸味的盐,所以可以用NaNO2代替NaCl作食用盐 C、铁和铜都是金属,铁与稀硫酸反应产生氢气,所以铜也能与稀硫酸反应产生氢气 D、H2O和H2O2的组成元素相同,但由于它们分子的组成不同,所以它们的化学性质是不同的5. 编号为甲、乙、丙、丁的4种无色溶液,分别是氯化钙、硝酸银、盐酸、碳酸钠中的一种,将它们两两混合后的现象如下表所示。根据实验现象判断乙溶液中溶质的化学式是( )
实验顺序
实验内容
实验现象
⑴
甲+乙
有气泡产生
⑵
甲+丙
有沉淀产生
⑶
丙+丁
有沉淀产生
⑷
乙+丙
无明显现象发生
A、Na2CO3 B、AgNO3 C、HCl D、CaCl26. 在氢氧化钠溶液中加入一定量的稀盐酸后,下列实验能证明两者恰好完全中和的是( )A、滴入适量FeCl3溶液,溶液变黄,但无沉淀生成 B、滴入几滴酚酞试液,酚酞试液不变色 C、测得反应后溶液中Na+与Cl-的个数比为1:1 D、滴入适量AgNO3溶液和稀硝酸,观察到有白色沉淀7. 生活中一些食物和饮料的pH 如下表所示,若某位病患者的胃酸过多,你提出建议他在空腹时最适宜食用的是( )食物与饮料
葡萄
糖水
牛奶
玉米粥
pH
3.5~4.5
7
6.3~6.6
6.8~8.0
A、葡萄 B、糖水 C、牛奶 D、玉米粥8. 实验室里有三瓶失去标签的无色溶液,只知道分别是澄清石灰水、氢氧化钠溶液和稀盐酸中的一种,下列四种试剂能将无色溶液只需要一次性鉴别开来的是( )A、碳酸钠溶液 B、稀硫酸 C、氢氧化钡溶液 D、无色酚酞溶液9. 甲、乙的溶解度曲线如图所示。下列有关说法错误的是( ) A、t2℃时,甲的饱和溶液中溶质和溶剂的质量之比为2:5 B、乙的饱和溶液从t2℃降温到t1℃,溶液仍饱和 C、t1℃时,甲、乙两种饱和溶液中溶质的质量相等 D、甲、乙的饱和溶液分别从t2℃降温到t1℃,两溶液中溶质质量分数相等10. 下列实验能用如图表示的是( )
A、t2℃时,甲的饱和溶液中溶质和溶剂的质量之比为2:5 B、乙的饱和溶液从t2℃降温到t1℃,溶液仍饱和 C、t1℃时,甲、乙两种饱和溶液中溶质的质量相等 D、甲、乙的饱和溶液分别从t2℃降温到t1℃,两溶液中溶质质量分数相等10. 下列实验能用如图表示的是( )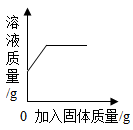 A、向硫酸铜溶液中加入铁粉 B、向过氧化氢溶液中加入二氧化锰 C、向一杯接近饱和的石灰水中加入氧化钙(已知:) D、向不饱和的硝酸钾溶液中加入硝酸钾固体11. 推理是学习化学的一种重要方法,下列推理正确的是( )A、氧化物中含有氧元素,所以含有氧元素的化合物都是氧化物 B、溶液中有晶体析出时,溶质质量减小,所以溶质的质量分数一定减小 C、碱性溶液能使紫色石蕊试液变蓝,所以能使石蕊试液变蓝的溶液一定呈碱性 D、碳酸盐与盐酸反应放出气体,所以与盐酸反应放出气体的物质一定是碳酸盐
A、向硫酸铜溶液中加入铁粉 B、向过氧化氢溶液中加入二氧化锰 C、向一杯接近饱和的石灰水中加入氧化钙(已知:) D、向不饱和的硝酸钾溶液中加入硝酸钾固体11. 推理是学习化学的一种重要方法,下列推理正确的是( )A、氧化物中含有氧元素,所以含有氧元素的化合物都是氧化物 B、溶液中有晶体析出时,溶质质量减小,所以溶质的质量分数一定减小 C、碱性溶液能使紫色石蕊试液变蓝,所以能使石蕊试液变蓝的溶液一定呈碱性 D、碳酸盐与盐酸反应放出气体,所以与盐酸反应放出气体的物质一定是碳酸盐二、多选题
-
12. 如图是稀盐酸和氢氧化钠溶液反应的pH变化曲线图,据图分析能得出的结论正确的是( )
 A、该反应是稀盐酸滴入NaOH溶液中 B、a克是指加入NaOH溶液的质量 C、A点时,溶液的溶质为NaOH、NaCl D、B点表示稀盐酸和加入的NaOH溶液质量一定相同13. 下列有关物质鉴别方案中,正确的是( )A、HCl、NaCl、KOH三种溶液,只用酸碱指示剂即可鉴别 B、MgCl2、NaOH、HCl、Na2SO4四种溶液,不加任何试剂即可鉴别 C、Fe2O3、CuO、C、Fe只用一种试剂无法鉴别 D、K2CO3、H2SO4、BaCl2、HCl四种溶液,不加任何试剂即可鉴别14. 往硫酸和硫酸铜的混合溶液中,逐滴加入氢氧化钠溶液直至过量,根据实验实施绘制如图所示曲线。下列说法正确的是( )
A、该反应是稀盐酸滴入NaOH溶液中 B、a克是指加入NaOH溶液的质量 C、A点时,溶液的溶质为NaOH、NaCl D、B点表示稀盐酸和加入的NaOH溶液质量一定相同13. 下列有关物质鉴别方案中,正确的是( )A、HCl、NaCl、KOH三种溶液,只用酸碱指示剂即可鉴别 B、MgCl2、NaOH、HCl、Na2SO4四种溶液,不加任何试剂即可鉴别 C、Fe2O3、CuO、C、Fe只用一种试剂无法鉴别 D、K2CO3、H2SO4、BaCl2、HCl四种溶液,不加任何试剂即可鉴别14. 往硫酸和硫酸铜的混合溶液中,逐滴加入氢氧化钠溶液直至过量,根据实验实施绘制如图所示曲线。下列说法正确的是( ) A、a至b段有蓝色沉淀生成 B、d点溶质种类为两种 C、c至d段,溶液pH不断减少 D、a至b段,溶液pH不断增大15. 两个烧杯中装有等质量的金属锌和镁,然后分别逐渐加入同浓度的稀硫酸,产生氢气的质量与加入硫酸的质量关系如图所示。下列说法正确的是( )
A、a至b段有蓝色沉淀生成 B、d点溶质种类为两种 C、c至d段,溶液pH不断减少 D、a至b段,溶液pH不断增大15. 两个烧杯中装有等质量的金属锌和镁,然后分别逐渐加入同浓度的稀硫酸,产生氢气的质量与加入硫酸的质量关系如图所示。下列说法正确的是( )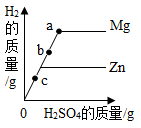 A、该图反映出镁比锌的金属活动性强 B、a点时,两个烧杯中的酸都恰好完全反应 C、b点时,盛金属锌的烧杯中硫酸有剩余 D、c点时,两个烧杯中都有金属剩余
A、该图反映出镁比锌的金属活动性强 B、a点时,两个烧杯中的酸都恰好完全反应 C、b点时,盛金属锌的烧杯中硫酸有剩余 D、c点时,两个烧杯中都有金属剩余三、填空题
-
16. 写出下列反应的化学方程式。(1)、①工业炼铁的主要反应原理:。
②天然气完全燃烧:。
(2)、利用如图所示实验,验证铁和铜的金属活动性顺序。
①A中可观察到的现象是。
②B中反应的化学方程式为。
③请判断C装置能否验证铁和铜的金属活动性顺序。
17. 回答:(1)、我国科研团队率先提出“单原子催化”概念。单原子催化剂用于合成气制造燃料甲醇(CH3OH)的微观示意图如图所示。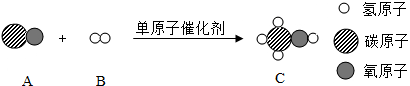
①A、B、C中属于单质的是(填字母序号);
②反应中A与B的分子个数比为。
(2)、利用食盐水制取ClO2的工业流程如图所示:
已知:装置I中发生的反应为 :Cl2是一种有毒气体。
①ClO2中Cl的化合价是。
②完成装置Ⅱ中反应的化学方程式::
③下列说法正确的是。(填字母序号)
A.装置Ⅲ中H2与Cl2发生化合反应生成HCl
B.该生产过程需要消耗电能
C.Cl2的循环利用可以减少生产过程对环境造成的污染
四、综合题
-
18. 回答:(1)、如图为A、B、C三种固体物质的溶解度曲线图(ABC析出时均不含结晶水),根据曲线图回答下列问题。

①t1℃时,溶解度最大的物质是 , A、B、C三种物质饱和溶液中,溶质质量分数的大小关系是。
②若将M点处A的不饱和溶液变成饱和溶液,可以选择的方法是(填序号);
A.降低温度 B.增加溶质 C.蒸发溶剂
③t2℃时,将等质量的A、B、C的饱和溶液都升温到t3℃,溶液中溶剂质量的大小关系是(忽略水的挥发)。
(2)、已知氢氧化钡也是一种重要的碱,其化学性质与氢氧化钙相似。①若向氢氧化钡的溶液中通入二氧化碳,溶液中出现白色浑浊现象,请写出该反应的化学方程式为。
②若向氢氧化钡的溶液中滴入酚酞试液,则溶液呈红色,然后向溶液中倒入稀盐酸,一会儿溶液变成了无色,此时溶液中一定含有的溶质是;可能含有的溶质是;为了证明可能含有的溶质的存在,你的实验方案是;可能看到的现象是。
(3)、A~E都是初中化学中常见的不同类别物质,A是人体胃液中帮助消化的成分,B俗称烧碱,C是红色固体粉末,D是通常时密度最小的气体,它们之间的相互或转化关系如图所示。请回答下列问题: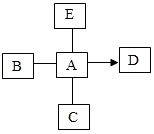
①写物质化学式:D为。
②按物质分类,B属于(填序号):
A.酸 B.碱 C.盐 D.氧化物
③物质性质决定其用途,A可用于金属除锈,写出A与C反应时的化学方程式为。
19. 海水是巨大的资源宝库。以下是某工厂对海水资源综合利用的示意图。 (1)、操作I和操作II的名称分别是、。母液中一定含有的金属元素是;(2)、反应(2)的化学反应方程式是.反应(1)的基本反应类型是。20. 回答:(1)、某气体可能含有氢气、一氧化碳、二氧化碳、水蒸气中的一种或几种。某兴趣小组利用下图中的实验装置设计实验,探究气体的成分。请用符合题目要求的装置序号填空(装置可以重复使用,除杂试剂均足量)。
(1)、操作I和操作II的名称分别是、。母液中一定含有的金属元素是;(2)、反应(2)的化学反应方程式是.反应(1)的基本反应类型是。20. 回答:(1)、某气体可能含有氢气、一氧化碳、二氧化碳、水蒸气中的一种或几种。某兴趣小组利用下图中的实验装置设计实验,探究气体的成分。请用符合题目要求的装置序号填空(装置可以重复使用,除杂试剂均足量)。提示: , ;无水硫酸铜粉末遇水变蓝色。

①若检验气体中是否存在水蒸气,可将该气体通入装置。
②将气体依次通过装置 , 可检验并除去该气体中的二氧化碳;
③若检验气体中是否存在一氧化碳,可将该气体依次通过装置。
④将气体依次通过装置 , 可一次性确定该气体的成分。
(2)、日常生活中,人们利用碳酸钠溶液具有碱性,清洗餐具上的油污,碱性越强,去油污的效果越好,化学小组同学决定对影响碳酸钠溶液碱性的因素展开探究。回答有关问题。I、用不同温度的水,分别配制2%、6%、10%的碳酸钠溶液,测量溶液的pH值如下表:
序号
A1
A2
A3
B1
B2
B3
Cl
C2
C3
质量分数
2%
2%
2%
6%
6%
6%
10%
10%
10%
水温(℃)
20
40
60
20
50
60
20
40
70
溶液pH
10.90
11.18
11.26
11.08
11.27
11.30
11.22
11.46
11.50
①溶液碱性最强的是(填实验序号)
②要得出碳酸钠溶液的溶质质量分数变化与pH变化关系的结论,可选择的一组实验是(填实验序号),结论是。
Ⅱ、测得10%的碳酸钠溶液从20℃升温至70℃的pH值如下表:
温度(℃)
20
30
40
50
60
70
溶液pH
11.22
11.35
11.46
11.48
11.50
11.50
①由上表可知,温度对碳酸钠溶液的pH影响是。
②将适量碳酸钠粉末洒在沾有油污的餐具上,并冲入适量的热水,再进行擦洗,达到较好的洗涤效果,这是因为。
III、碳酸钠溶于水,有部分碳酸钠能与水发生反应生成氢氧化钠,致使溶液呈碱性。实验室鉴别碳酸钠溶液和氢氧化钠溶液可选用的试剂是。
A.酚酞试液 B.稀盐酸 C.氯化钠溶液 D.氢氧化钙溶液
21. 某化学兴趣小组在完成“金属的性质”实验时进行了以下一些探究活动。【探究话动】:将铝丝插入硫酸铜溶液中未发现明显的实验现象。
(1)、【现象分析】:请分析出现上述实验现象的原因:;为顺利完成实验,你的建议是。(2)、【继续实验】:兴趣小组同学根据你的建议,重新进行了实验,观察到了明显的实验现象。经充分反应后,该实验的现象是:。(3)、经研究发现该反应的微观示意图如图所示(图中微粒未完全画出)。则实际参加反应的微粒(用符号来表示)是。 (4)、兴趣小组在完成上述实验时,还发现了铝丝表面有少量气泡生成。根据已有知识和资料信息判断这种气体有可能是(资料信息:硫酸铜在水中会发生一些变化,生成微量的稀硫酸),反应的化学方程式是。22. 设计方案是实验探究的保证,感悟方法是探究的根本目的。某合作学习小组开展了如下探究:(1)、KOH溶液中含有H2O、K+、OH- , 能使无色酚酞试液变成红色。某化学兴趣小组想探究KOH溶液使无色酚酞试液变成红色的原因。
(4)、兴趣小组在完成上述实验时,还发现了铝丝表面有少量气泡生成。根据已有知识和资料信息判断这种气体有可能是(资料信息:硫酸铜在水中会发生一些变化,生成微量的稀硫酸),反应的化学方程式是。22. 设计方案是实验探究的保证,感悟方法是探究的根本目的。某合作学习小组开展了如下探究:(1)、KOH溶液中含有H2O、K+、OH- , 能使无色酚酞试液变成红色。某化学兴趣小组想探究KOH溶液使无色酚酞试液变成红色的原因。【提出问题】。
(2)、【提出猜想】猜想1:KOH溶液中的H2O使无色酚酞试液变红;猜想2:KOH溶液中的K+使无色酚酞试液变红;
猜想3:。
(3)、【实验探究】实验操作
实验现象
结论
①用试管取少量蒸馏水,滴入1~2滴无色酚酞试液
试管内溶液不变色
猜想1不成立
②用试管取少量KCl溶液,滴入1~2滴无色酚酞试液
猜想2不成立
③ , 滴入1~2滴无色酚酞试液
试管内溶液变红
(4)、【讨论反思】有同学认为猜想1不需要实验验证就可以排除,你认为该同学的理由是:。(5)、【拓展提高】向Ba(OH)2溶液中滴入几滴无色酚酞试液,观察到的现象是。(6)、某化学兴趣小组的同学向一定量的NaHCO3溶液中加入一定量的稀H2SO4。待反应充分后(假设反应所产生的气体全部逸出),对反应后溶液中溶质的成分进行如下探究:【实验用品】pH试纸、Zn片、氧化铜粉末、稀H2SO4、NaOH溶液、BaCl2溶液。
【假设猜想】猜想一:Na2SO4
猜想二:Na2SO4、NaHCO3
猜想三:Na2SO4、H2SO4
【实验探究】同学们取反应后的溶液用不同方案进行如下实验,请根据现象或结论填空。
实验方案
A
B
C
D
实验操作




实验现象
无气泡产生
产生白色沉淀
实验结论
猜想三正确
猜想三正确
猜想三正确
【得出结论】猜想三正确
(7)、【评价反思】老师对同学们能用多种方案进行探究,并且得出正确的实验结论给予了肯定,同时指出探究中存在的两处明显不正确,分别是:①。
②。
(8)、【总结提高】依据所给实验用品,你还有什么不同方法确认猜想三是正确的。请写出你的实验方案及现象。五、计算题
-
23. 侯氏制碱法生产的碳酸钠中常含有少量的氯化钠。现有碳酸钠和氯化钠的混合物样品12.5g,将其放入干净的烧杯中,加入100g水,使其完全溶解。向所得溶液中加入溶质质量分数为7.3%的稀盐酸,烧杯中溶液的质量与加入稀盐酸的质量关系曲线如图所示。请回答下列问题。
 (1)、B点时,烧杯中溶液里存在的阳离子为(填写离子符号)。(2)、A点时生成CO2的质量为:。(3)、样品中NaCl的质量为:。(4)、A点时,求此温度下所得不饱和溶液中溶质质量分数(计算结果精确至0.1%)。
(1)、B点时,烧杯中溶液里存在的阳离子为(填写离子符号)。(2)、A点时生成CO2的质量为:。(3)、样品中NaCl的质量为:。(4)、A点时,求此温度下所得不饱和溶液中溶质质量分数(计算结果精确至0.1%)。