福建省福州市闽清县2021-2022学年九年级上学期期末化学试题
试卷更新日期:2022-11-07 类型:期末考试
一、单选题
-
1. 地壳含量最高的元素是( )A、氧 B、硅 C、铝 D、铁2. 下列气体能引起酸雨的是( )A、二氧化硫 B、一氧化碳 C、二氧化碳 D、水蒸气3. 化石燃料开发和利用新能源已迫在眉睫,下列属于新能源的是( )A、潮汐能 B、煤 C、石油 D、天然气4. 东汉炼丹家魏伯阳所著《周易参同契》记有“胡粉投火中,色坏还为铅”。“胡粉”受热会变为Pb3O4 , Pb3O4属于( )A、酸 B、氧化物 C、混合物 D、单质5. 厨房炒菜时,油锅过热着火,下列灭火措施适宜的是( )A、加少量水 B、倒掉油 C、盖上锅盖 D、撒上沙子6. 下列实验操作正确的是( )A、
 熄灭酒精灯
B、
熄灭酒精灯
B、 取用固体药品
C、
取用固体药品
C、 倾倒液体
D、
倾倒液体
D、 检查气密性
7. 下列属于置换反应的是( )A、 B、 C、NaOH+HCl=NaCl+H2O D、2Al+6HCl=2AlCl3+3H2↑8. 根据下图提供的信息,下列说法正确的是( )
检查气密性
7. 下列属于置换反应的是( )A、 B、 C、NaOH+HCl=NaCl+H2O D、2Al+6HCl=2AlCl3+3H2↑8. 根据下图提供的信息,下列说法正确的是( ) A、钠原子最外层有11个电子 B、钠的相对原子质量是22.99g C、钠属于非金属元素 D、钠的原子序数为119. 酸奶中含有大量乳酸菌,乳酸菌把乳糖转化成乳酸,使得牛奶的酸度升高。研究者选取某种市面常见的酸奶进行实验,数据如图所示:下列说法中,不合理的是( )
A、钠原子最外层有11个电子 B、钠的相对原子质量是22.99g C、钠属于非金属元素 D、钠的原子序数为119. 酸奶中含有大量乳酸菌,乳酸菌把乳糖转化成乳酸,使得牛奶的酸度升高。研究者选取某种市面常见的酸奶进行实验,数据如图所示:下列说法中,不合理的是( ) A、温度越高,酸奶酸度升高的越快 B、酸奶喝得过多会导致胃酸过多 C、酸奶的酸度升高的过程属于化学变化 D、随着时间推移酸奶的酸度从零开始不断增加10. 已知:C+2CuO2Cu+CO2↑。如图表示一定量的木炭和氧化铜固体混合物受热过程中,某变量y随加热时间的变化趋势,其中纵坐标y表示( )
A、温度越高,酸奶酸度升高的越快 B、酸奶喝得过多会导致胃酸过多 C、酸奶的酸度升高的过程属于化学变化 D、随着时间推移酸奶的酸度从零开始不断增加10. 已知:C+2CuO2Cu+CO2↑。如图表示一定量的木炭和氧化铜固体混合物受热过程中,某变量y随加热时间的变化趋势,其中纵坐标y表示( )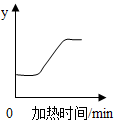 A、固体的质量 B、固体中氧化铜的质量 C、二氧化碳的质量 D、固体中铜元素的质量分数
A、固体的质量 B、固体中氧化铜的质量 C、二氧化碳的质量 D、固体中铜元素的质量分数二、填空题
-
11. 化学源于生活,生活中蕴含着许多化学知识:(1)、点燃蚊香闻到气味,这是因为分子。(2)、打开汽水瓶盖时,汽水会自动喷出来,其中气体是。(3)、“真金不怕火炼”是指金即使在高温下也不与反应。(4)、金刚石与石墨可称为“同素异形体”,物理性质存在差异的原因是。(5)、钢铁车身喷漆处理既美观又防锈,喷漆防锈的原理是。(6)、燃料:近些年厨房燃料的更新换代如下图所示:

①煤燃烧可能产生的污染物有(填标号)。
A.二氧化碳 B.二氧化硫 C.一氧化碳 D.粉尘固体颗粒
②天然气主要成分是(填化学名称),其完全燃烧,产物不会对空气有污染,请你写出其燃烧的化学方程式是。
12. 在“宏观一微观一符号”之间建立联系,是化学特有的思维方式。(1)、下图是四种粒子结构示意图。
①D中的X=。
②A、B、C、D中属于同种元素的粒子是(填序号)。
(2)、汽车尾气催化转换器可减少有害气体排放,其反应过程的微观变化如图所示。
①已知丁是一种单质,则丁是(写化学式);
②写出该反应的化学方程式。
三、综合题
-
13. 水生活的应用
收集到一瓶浑浊的河水,他要模拟自来水厂的净水过程,最终制成蒸馏水,其实验过程如图1所示,请回答下列问题。
 (1)、操作①的名称是(2)、操作②应选用的装置为(填图2序号),该过程主要是变化;
(1)、操作①的名称是(2)、操作②应选用的装置为(填图2序号),该过程主要是变化; (3)、装置Ⅰ中仪器a的名称是。(4)、操作③的过程中,发生变化的是____(填序号);A、分子质量 B、分子的种类 C、分子间隔(5)、取经过操作③后的液体于试管中,加入少量肥皂水振荡,可观察到的实验现象是。(6)、水在化学实验中的作用不可忽视,请结合图示回答下列问题:
(3)、装置Ⅰ中仪器a的名称是。(4)、操作③的过程中,发生变化的是____(填序号);A、分子质量 B、分子的种类 C、分子间隔(5)、取经过操作③后的液体于试管中,加入少量肥皂水振荡,可观察到的实验现象是。(6)、水在化学实验中的作用不可忽视,请结合图示回答下列问题:
①实验A中水的作用是提供热量和。
②实验B中的水是。
③在C实验中,集气瓶内预先装入少量水,可以起到的作用有。
14. 海水素有“液体工业原料”之美誉。工业“从海水中提取镁”的主要流程如下: (1)、煅烧炉中反应的化学方程式为:CaCO3CaO+CO2↑,此反应属于基本类型中的反应。(2)、反应沉淀池中发生如下反应:
(1)、煅烧炉中反应的化学方程式为:CaCO3CaO+CO2↑,此反应属于基本类型中的反应。(2)、反应沉淀池中发生如下反应:①CaO+H2O=Ca(OH)2;
②Ca(OH)2+MgSO4=CaSO4+Mg(OH)2↓,
操作Ⅰ为。
(3)、电解槽中,能生成镁的反应物为。15. 下列物质由C、H、O三种元素中的一种或几种组成,它们是初中化学常见的物质:(1)、若某单质为最清洁的燃料,它的化学式是。(2)、若某化合物能燃烧,则化合物中一定含有的元素是。(3)、甲、乙、丙三种物质在一定条件下存在如下转化关系(图中已略去部分物质)。
若只有甲为固体,其他物质均为气体,则X是。乙→丙反应的化学方程是。
16. 实验室常用下列装置制备气体,请回答下列问题。 (1)、实验室用B装置制取CO2 , 写出反应的化学方程式是 , 若用装置E收集CO2 , 验满的方法是。(2)、实验室用氯酸钾制取氧气,选用装置A和D,实验操作有:a.停止加热 b.固定试管 c.将导管从水槽中取出 d.装入药品并加热 e.收集氧气
(1)、实验室用B装置制取CO2 , 写出反应的化学方程式是 , 若用装置E收集CO2 , 验满的方法是。(2)、实验室用氯酸钾制取氧气,选用装置A和D,实验操作有:a.停止加热 b.固定试管 c.将导管从水槽中取出 d.装入药品并加热 e.收集氧气①b操作在试管口略向下倾斜的原因是;②上述操作中缺少的一个步骤是 , 假设该操作步骤为f,则上述制氧气正确的操作顺序是(填序号)。写出反应的化学方程式是。
(3)、若收集氨气的装置只能用D,由此可知氨气所具有的性质。17. 常温下没有氧气存在时,铁与水几乎不反应,但在高温下,铁与水蒸气能反生成一种常见的铁的氧化物和一种气体。小明设计如下实验探究铁粉与水蒸气反应后的产物。 (1)、试管底部放一团湿棉花的目的是。(2)、探究生成的气体是什么?用燃着的木条靠近肥皂泡,有爆鸣声,稍后有肥皂泡飘到空中,说明生成的气体是。(3)、探究试管中剩余固体成分是什么?
(1)、试管底部放一团湿棉花的目的是。(2)、探究生成的气体是什么?用燃着的木条靠近肥皂泡,有爆鸣声,稍后有肥皂泡飘到空中,说明生成的气体是。(3)、探究试管中剩余固体成分是什么?【查阅资料】
资料Ⅰ:常见的铁的氧化物如下表。
常见铁的氧化物
氧化亚铁(FeO)
氧化铁(Fe2O3)
四氧化三铁(Fe3O4)
颜色、状态
黑色粉末
红色粉末
黑色粉末
能否被磁铁吸引
否
否
能
资料Ⅱ:Fe3O4与稀盐酸反应化学方程为Fe3O4+8HCl=FeCl2+2FeCl3+4H2O。
【初步验证】试管中剩余固体为黑色,能全部被磁铁吸引。
【讨论】该黑色固体不可能是FeO也不可能是Fe2O3。请写出不可能是Fe2O3的理由。
(4)、【猜 想】猜想Ⅰ.试管中剩余固体是铁。猜想Ⅱ.试管中剩余固体是四氧化三铁。猜想Ⅲ.试管中剩余固体是。
(5)、【实验探究】实验操作
实验现象
实验结论
取适量试管中黑色固体于烧杯中,加入足量稀硫酸,搅拌
黑色固体全部溶解,无气泡产生
正确的猜想是
(填“Ⅰ”、“Ⅱ”或“Ⅲ”)
(6)、【实验结论】铁与水蒸气反应的化学方程式为。四、计算题
-
18. 取一定量碱式碳酸铜[Cu2(OH)2CO3]粉末放入烧杯中,加入稀硫酸至恰好完全反应(假设气体全部扩散),测得实验过程中烧杯及烧杯内物质的质量随时间变化关系如图所示。[反应原理:Cu2(OH)2CO3+2H2SO4=2CuSO4+CO2↑+3H2O]
请计算:
 (1)、生成的二氧化碳质量为g。(2)、参加反应的硫酸质量。
(1)、生成的二氧化碳质量为g。(2)、参加反应的硫酸质量。