天津市红桥区2022-2023学年九年级上学期期中化学试题
试卷更新日期:2022-11-04 类型:期中考试
一、单选题
-
1. 《天工开物》是我国古代科技发展的智慧结晶,下列书中记载的造物过程涉及化学变化的是( )A、机杼织布 B、粉碎矿石 C、海水晒盐 D、五谷醇酒2. 从9月1日起,农村中小学生采取课间、加餐模式,每天为每个孩子提供一盒学生饮用奶。喝牛奶可以补钙,这里“钙”指的是( )A、单质 B、元素 C、分子 D、原子3. 下列实验操作正确的是( )A、
 液体读数
B、
液体读数
B、 液体取用
C、
液体取用
C、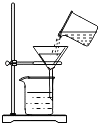 过滤
D、
过滤
D、 滴加液体
4. 表示下列各项大小或高低关系正确的是( )A、元素在地壳中的含量:O<Al B、化合物中氮元素的化合价:NH3>NO C、空气中气体的含量:氧气<氮气 D、酒精灯火焰的温度:内焰>外焰5. 下列各选项中,解释与事实不吻合的是( )
滴加液体
4. 表示下列各项大小或高低关系正确的是( )A、元素在地壳中的含量:O<Al B、化合物中氮元素的化合价:NH3>NO C、空气中气体的含量:氧气<氮气 D、酒精灯火焰的温度:内焰>外焰5. 下列各选项中,解释与事实不吻合的是( )选项
事实
解释
A
水在通电条件下,可分解为氧气和氢气
化学反应中分子是可分的
B
降温加压条件下,空气液化后体积变小
降温加压时,分子本身体积变小
C
某物质在空气中燃烧生成水
该物质中一定含有氢元素
D
食物变质
分子本身发生了变化
A、A B、B C、C D、D6. 北斗卫星采用铷原子钟提供精确时间。铷元素在元素周期表中的相关信息如图所示。下列说法正确的是( )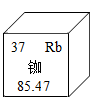 A、拉瓦锡发现了元素周期律 B、铷属于非金属元素 C、铷原子的核内质子数为37 D、铷的相对原子质量为85.47g7. 下列各图中
A、拉瓦锡发现了元素周期律 B、铷属于非金属元素 C、铷原子的核内质子数为37 D、铷的相对原子质量为85.47g7. 下列各图中 和
和 分别表示不同元素的原子,从物质分类看,下面有纯净物和混合物,也有单质和化合物,则其中表示化合物的是( ) A、
分别表示不同元素的原子,从物质分类看,下面有纯净物和混合物,也有单质和化合物,则其中表示化合物的是( ) A、 B、
B、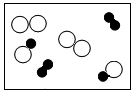 C、
C、 D、
D、 8. 下列有关物质燃烧现象的描述,与事实不符的是( )A、白磷燃烧产生黑烟 B、镁在空气中燃烧发出耀眼的白光 C、硫在氧气中燃烧发出蓝紫色火焰 D、木炭在氧气中燃烧发出白光9. 速效感冒冲剂的主要成分之一是“对乙酰氨基酚”,其化学式为C8H9NO2 , 有关它的叙述错误的是( )A、“对乙酰氨基酚”的相对分子质量是151 B、“对乙酰氨基酚”中碳、氢、氮、氧元素质量比是8:9:1:2 C、一个“对乙酰氨基酚”分子中含有20个原子 D、“对乙酰氨基酚”由碳、氢、氮、氧四种元素组成10. 借助质量守恒定律进行定量分析是研究化学反应的重要方法,现将20gA和足量B在一定条件下充分反应,生成16gC和11gD,则参加反应的A和B的质量比是( )A、20:11 B、5:4 C、20:7 D、16:1111. 化学反应方程式是解决宏、微、符三重表征的重要化学用语,根据化学方程式中元素守恒、原子守恒原则,分析中X的化学式为( )A、N2 B、N2O C、NO D、NO212. 逻辑推理是学好化学的重要思维方法,下面是从小明同学学习笔记中摘录出来的一些推理,你认为正确的是( )A、分子、原子都是不带电的粒子,所以水分子、硫原子都不带电 B、在化合物里,正负化合价的代数和为零,所以在同一化合物中金属元素显正价,则非金属元素一定都显负价 C、氧气是由氧元素组成的,所以制取氧气的反应物中一定含氧分子 D、单质是由一种元素组成的,所以同种元素组成的物质一定是单质13. 下列含铁混合物中,铁元素的质量分数最高的是( )A、FeO B、Fe2O3 C、Fe2(SO4)3 D、Fe3O4
8. 下列有关物质燃烧现象的描述,与事实不符的是( )A、白磷燃烧产生黑烟 B、镁在空气中燃烧发出耀眼的白光 C、硫在氧气中燃烧发出蓝紫色火焰 D、木炭在氧气中燃烧发出白光9. 速效感冒冲剂的主要成分之一是“对乙酰氨基酚”,其化学式为C8H9NO2 , 有关它的叙述错误的是( )A、“对乙酰氨基酚”的相对分子质量是151 B、“对乙酰氨基酚”中碳、氢、氮、氧元素质量比是8:9:1:2 C、一个“对乙酰氨基酚”分子中含有20个原子 D、“对乙酰氨基酚”由碳、氢、氮、氧四种元素组成10. 借助质量守恒定律进行定量分析是研究化学反应的重要方法,现将20gA和足量B在一定条件下充分反应,生成16gC和11gD,则参加反应的A和B的质量比是( )A、20:11 B、5:4 C、20:7 D、16:1111. 化学反应方程式是解决宏、微、符三重表征的重要化学用语,根据化学方程式中元素守恒、原子守恒原则,分析中X的化学式为( )A、N2 B、N2O C、NO D、NO212. 逻辑推理是学好化学的重要思维方法,下面是从小明同学学习笔记中摘录出来的一些推理,你认为正确的是( )A、分子、原子都是不带电的粒子,所以水分子、硫原子都不带电 B、在化合物里,正负化合价的代数和为零,所以在同一化合物中金属元素显正价,则非金属元素一定都显负价 C、氧气是由氧元素组成的,所以制取氧气的反应物中一定含氧分子 D、单质是由一种元素组成的,所以同种元素组成的物质一定是单质13. 下列含铁混合物中,铁元素的质量分数最高的是( )A、FeO B、Fe2O3 C、Fe2(SO4)3 D、Fe3O4二、多选题
-
14. 关于分子和原子的说法正确的是( )A、原子不能直接构成物质 B、同种原子能构成不同的分子 C、同种分子能构成混合物 D、化学变化中原子的个数一定不会变15. 阅读图中蕴含的信息是一种重要的摄取信息能力,“价-类”二维图能反映元素的化合价与物质类别之间的关系。下图是碳元素的“价-类”二维图。下列说法错误的是( )
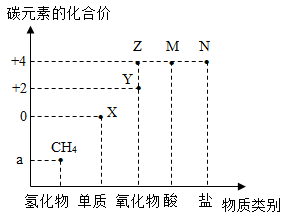 A、a=-2 B、X点对应的物质可以是金刚石或足球烯(C60) C、X、Y点对应的物质都可以通过一步反应转化为Z D、M、N点对应的物质化学式符合题意书写是H2CO3和NaCO3
A、a=-2 B、X点对应的物质可以是金刚石或足球烯(C60) C、X、Y点对应的物质都可以通过一步反应转化为Z D、M、N点对应的物质化学式符合题意书写是H2CO3和NaCO3三、填空题
-
16. 请从下列物质中选择合适的物质,用相应化学符号填空。(1)、最清洁的燃料是。(2)、过氧化氢中氧元素的化合价。(3)、若用
 表示一个氯原子,则
表示一个氯原子,则 表示的化学符号是。 (4)、两个氢氧根离子。17. 元素周期表是研究化学的重要化学工具,下图是几种元素在元素周期表中的相对位置以及部分信息。请回答下列问题:
表示的化学符号是。 (4)、两个氢氧根离子。17. 元素周期表是研究化学的重要化学工具,下图是几种元素在元素周期表中的相对位置以及部分信息。请回答下列问题: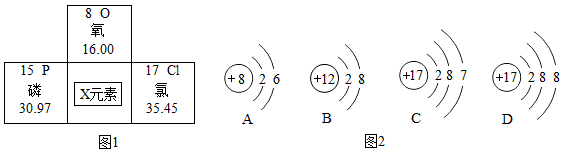 (1)、下列说法错误的是____(填写字母标号)。A、氯原子的核外电子数为17,最外层电子数为7 B、磷的相对原子质量为15 C、根据X元素的位置推出其质子数为16 D、保持氧气化学性质的最小粒子是O原子(2)、图2所示粒子共表示种元素。X元素的化学性质与图2中的化学性质相似(填写字母标号)。(3)、氯化镁是由(填具体粒子的化学符号)构成的,写出镁与氯气点燃生成氯化镁的方程式。(4)、稀有气体氩原子序数是18,其化学性质很不活泼的原因是。18. 写出下列反应的化学方程式。(1)、铁丝在氧气中燃烧。(2)、白磷燃烧生成五氧化二磷。(3)、过氧化氢溶液中加入少量二氧化锰制取氧气。19. 阅读化学科普是提高化学科学素养的重要途径,请阅读思考并用化学用语回答问题:
(1)、下列说法错误的是____(填写字母标号)。A、氯原子的核外电子数为17,最外层电子数为7 B、磷的相对原子质量为15 C、根据X元素的位置推出其质子数为16 D、保持氧气化学性质的最小粒子是O原子(2)、图2所示粒子共表示种元素。X元素的化学性质与图2中的化学性质相似(填写字母标号)。(3)、氯化镁是由(填具体粒子的化学符号)构成的,写出镁与氯气点燃生成氯化镁的方程式。(4)、稀有气体氩原子序数是18,其化学性质很不活泼的原因是。18. 写出下列反应的化学方程式。(1)、铁丝在氧气中燃烧。(2)、白磷燃烧生成五氧化二磷。(3)、过氧化氢溶液中加入少量二氧化锰制取氧气。19. 阅读化学科普是提高化学科学素养的重要途径,请阅读思考并用化学用语回答问题:我国提出:二氧化碳排放力争于2030年前达到峰值,努力争取2060年前实现“碳中和”的目标,下面是三种捕捉CO2技术。
(1)、二氧化碳中碳元素的化合价为(选填+2或+4);(2)、化学吸收法可利用钙基吸收剂(主要成分为CaO)控制560℃~700℃捕捉CO2转化成CaCO3。该反应的化学方程式为。(3)、使用纳米纤维作催化剂,可以将CO2和H2合成为甲醇(CH3OH)同时生成水。该反应的化学方程式为。(4)、我国科学家以CO2、H2为原料,通过十步反应制得淀粉[化学式为(C6H10O5)n],实现了CO2到淀粉的人工合成。关于二氧化碳合成淀粉的意义。(写出一条即可)四、综合题
-
20. 水是宝贵的自然资源,图中六个实验都用到了水。请回答:
 (1)、实验A中玻璃棒的作用是。(2)、实验B中水的作用。(3)、实验C中通过烧杯中的水进入集气瓶中的体积可得出结论:氧气约占空气体积的。(4)、实验D中,加入1/3瓶水,盖好瓶盖,振荡,塑料瓶变瘪。说明二氧化碳可能有的物理性质:(5)、实验E中,写出电解一定量的水的化学反应方程式 , 通电一段时间后,用带火星的木条在玻璃管尖嘴口检验A气体,现象是 , 化学反应的实质:分子破裂成原子,原子重新结合形成新分子。水通电反应中不变的粒子是(填微粒名称)。(6)、实验室常利用蒸馏(图F)的方法将天然水净化,所得水为(填“混合物”或“纯净物”)。21. 根据下列实验装置图,按要求回答确有关问题:
(1)、实验A中玻璃棒的作用是。(2)、实验B中水的作用。(3)、实验C中通过烧杯中的水进入集气瓶中的体积可得出结论:氧气约占空气体积的。(4)、实验D中,加入1/3瓶水,盖好瓶盖,振荡,塑料瓶变瘪。说明二氧化碳可能有的物理性质:(5)、实验E中,写出电解一定量的水的化学反应方程式 , 通电一段时间后,用带火星的木条在玻璃管尖嘴口检验A气体,现象是 , 化学反应的实质:分子破裂成原子,原子重新结合形成新分子。水通电反应中不变的粒子是(填微粒名称)。(6)、实验室常利用蒸馏(图F)的方法将天然水净化,所得水为(填“混合物”或“纯净物”)。21. 根据下列实验装置图,按要求回答确有关问题: (1)、数字标号①的仪器名称::标号②的仪器名称:。(2)、实验室用氯酸钾和二氧化锰制取并收集纯净的O2 , 应选用的装置是 , 反应的化学方程式为。(3)、排空气法收集O2验满的操作方法是:。(4)、在盛有双氧水的B装置中加入一氧化锰后,观察到带火星的木条复燃。甲同学根据实验现象得出:工氧化锰能过氧化氢分解的速率,因此,甲同学认为二氧化锰是过氧化氢分解的催化剂。(5)、如果使用下图所示装置收集O2 , 如将装置中充满水,O2由口进入。
(1)、数字标号①的仪器名称::标号②的仪器名称:。(2)、实验室用氯酸钾和二氧化锰制取并收集纯净的O2 , 应选用的装置是 , 反应的化学方程式为。(3)、排空气法收集O2验满的操作方法是:。(4)、在盛有双氧水的B装置中加入一氧化锰后,观察到带火星的木条复燃。甲同学根据实验现象得出:工氧化锰能过氧化氢分解的速率,因此,甲同学认为二氧化锰是过氧化氢分解的催化剂。(5)、如果使用下图所示装置收集O2 , 如将装置中充满水,O2由口进入。 (6)、氢气是一种用途较广泛的气体,在实验室中常用锌粒与稀硫酸(液体)反应制取氢气。那么实验室制取氢气的收集装置是。(7)、补全实验报告。
(6)、氢气是一种用途较广泛的气体,在实验室中常用锌粒与稀硫酸(液体)反应制取氢气。那么实验室制取氢气的收集装置是。(7)、补全实验报告。装置及药品
现象
解释或结论

a:木炭
b:
木炭燃烧,发白光,放热,溶液b变浑浊
木炭在氧气中燃烧生成二氧化碳
22. A、B、C、D、E、F是初中化学常见的物质,已知通常状态下C、E、F是气体,A、B、D都是固体。其中A是暗紫色固体(含有K、Mn、O三种元素),在纯净的C中点燃生成E过程有蓝紫色火焰,E是一种有刺激性气味气体,F是光合作用的主要原料。反应条件已省略。试回答: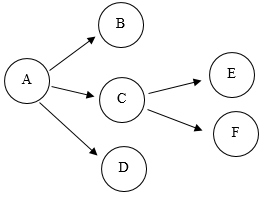 (1)、写出C的一种用途:;物质F的化学式为。(2)、写出C生成E的化学反应方程式为 , 基本反应类型是。(3)、反应A生成C的化学反应方程式为 , 其基本反应类型是。23. “5G”改变生活,中国芯彰显中国“智”造。芯片的基材主要是高纯硅,如图是一种制备高纯硅的工艺流程图(盐酸是的水溶液):
(1)、写出C的一种用途:;物质F的化学式为。(2)、写出C生成E的化学反应方程式为 , 基本反应类型是。(3)、反应A生成C的化学反应方程式为 , 其基本反应类型是。23. “5G”改变生活,中国芯彰显中国“智”造。芯片的基材主要是高纯硅,如图是一种制备高纯硅的工艺流程图(盐酸是的水溶液): (1)、二氧化硅中硅元素的化合价。(2)、反应1:镁在反应中作(填“催化剂”或“反应物”):(3)、操作I:操作名称是。(4)、反应Ⅱ要隔绝空气进行的原因;发生反应的化学方程式为。(5)、可以循环利用的物质是。(6)、从微观角度可以更好的认识化学反应的实质,如下图是某化学反应的微观示意图,请问答以下问题:
(1)、二氧化硅中硅元素的化合价。(2)、反应1:镁在反应中作(填“催化剂”或“反应物”):(3)、操作I:操作名称是。(4)、反应Ⅱ要隔绝空气进行的原因;发生反应的化学方程式为。(5)、可以循环利用的物质是。(6)、从微观角度可以更好的认识化学反应的实质,如下图是某化学反应的微观示意图,请问答以下问题:
写出图中氧化物的化学式:;计算反应物中单质与化合物的质量比。
五、计算题
-
24. 乙醇是一种清洁能源。乙醇的燃烧可发生以下两个反应:
①C2H6O+3O2 2CO2+ 3H2O
②aC2H6O+5O2 2CO2+2CO+6H2O。
回答下列问题。
(1)、反应②中的化学计量数a=。(2)、反应 (选填化学方程式的序号)属于完全燃烧,产物无毒性。(3)、9.2g乙醇在空气中若按化学方程式②发生反应,计算生成一氧化碳的质量。25. 用图1所示的装置制取二氧化碳并测定石灰石中碳酸钙的质量,化学反应方程式是 , 将稀盐酸全部加入锥形瓶中,天平示数的变化如图2所示,请计算(计算结果精确到0.1) (1)、碳家族中能吸附水中的杂质;金刚石硬度大,而石墨却很软是因为不同;古代用墨书写的典籍保存至今而不变色,体现了碳在常温下的化学性质是。(2)、产生的二氧化碳气体的质量。(3)、计算石灰石样品中碳酸钙的质量。
(1)、碳家族中能吸附水中的杂质;金刚石硬度大,而石墨却很软是因为不同;古代用墨书写的典籍保存至今而不变色,体现了碳在常温下的化学性质是。(2)、产生的二氧化碳气体的质量。(3)、计算石灰石样品中碳酸钙的质量。