浙江省宁波市2022-2023学年九年级上学期科学学科期中测试卷
试卷更新日期:2022-10-19 类型:期中考试
一、选择题(本题共15小题,第1~10小题每题4分,第11~15小题每题3分,共55分.请选出一个符合题意的选项,不选、多选、错选均不给分)
-
1. 胃酸可以帮助食物的消化,但是胃酸过多,就会伤及胃、十二指肠黏膜,造成胃溃疡或十二指肠溃疡等疾病。药物治疗可以口服抑酸剂,饮食治疗可以适当食用的食物是( )A、苹果pH=3.4
 B、萝卜pH=4.6
B、萝卜pH=4.6  C、土豆pH=5.4
C、土豆pH=5.4  D、板栗pH=8.8
D、板栗pH=8.8  2. 正确规范的操作是实验成功的关键,下列实验操作不规范的是( )A、闻气味
2. 正确规范的操作是实验成功的关键,下列实验操作不规范的是( )A、闻气味 B、滴加液体
B、滴加液体 C、测定某溶液的pH
C、测定某溶液的pH D、稀释浓硫酸
D、稀释浓硫酸 3. 下列化学方程式书写正确的是( )A、3Fe+2O2Fe3O4 B、Mg+O2MgO2 C、2H2O22H2↑+O2↑ D、CH4+2O2CO2↑+2H2O↑4. 对下列用品的有效成分、分类及其用途所对应的表述中,有错误的是( )
3. 下列化学方程式书写正确的是( )A、3Fe+2O2Fe3O4 B、Mg+O2MgO2 C、2H2O22H2↑+O2↑ D、CH4+2O2CO2↑+2H2O↑4. 对下列用品的有效成分、分类及其用途所对应的表述中,有错误的是( )A
B
C
D
用品




有效成分
NaHCO3
CH3COOH
NH3·H2O
Ca(OH)2
有效成分分类
盐
氧化物
碱
碱
用途
制作糕点等
用作调味料
用作化学肥料
粉刷墙壁等
A、A B、B C、C D、D5. 下列物质的名称、俗名、化学式不完全一致的是( )A、氢氧化钠 烧碱 NaOH B、氢氧化钙 消石灰 Ca(OH)2 C、氧化钙 熟石灰 CaO D、固态二氧化碳 干冰 CO26. 如图表示两种气体发生的化学反应,其中相同的球代表同种原子。下列说法正确的是( )
 A、生成物一定是混合物 B、分子在化学变化中不可分 C、该反应既不是化合反应也不是分解反应 D、化学反应前后原子的种类不变7. “变化观念与平衡思想”是化学学科的核心素养之一,下列关于酸和碱的一些变化中不属于化学变化的是( )A、用浓硫酸在纸上写字 B、打开浓盐酸的瓶盖,瓶口产生大量白雾 C、将氢氧化钠敞口放置质量增加 D、氢氧化钙溶液久置表面产生一层白膜8. 逻辑推理是化学常用的思维方法。下列推理正确的是( )A、碱性溶液的pH>7,碳酸钠溶液的pH>7,所以碳酸钠溶液是碱性溶液 B、在同一化合物中,金属元素显正价,所以非金属元素一定显负价 C、单质是由同种元素组成,所以由同种元素组成的物质一定属于单质 D、碳酸钠与盐酸反应放出气体,所以与盐酸反应放出气体的物质一定是碳酸盐9. 如图是无色溶液X发生化学反应时的颜色变化,无色溶液X是( )
A、生成物一定是混合物 B、分子在化学变化中不可分 C、该反应既不是化合反应也不是分解反应 D、化学反应前后原子的种类不变7. “变化观念与平衡思想”是化学学科的核心素养之一,下列关于酸和碱的一些变化中不属于化学变化的是( )A、用浓硫酸在纸上写字 B、打开浓盐酸的瓶盖,瓶口产生大量白雾 C、将氢氧化钠敞口放置质量增加 D、氢氧化钙溶液久置表面产生一层白膜8. 逻辑推理是化学常用的思维方法。下列推理正确的是( )A、碱性溶液的pH>7,碳酸钠溶液的pH>7,所以碳酸钠溶液是碱性溶液 B、在同一化合物中,金属元素显正价,所以非金属元素一定显负价 C、单质是由同种元素组成,所以由同种元素组成的物质一定属于单质 D、碳酸钠与盐酸反应放出气体,所以与盐酸反应放出气体的物质一定是碳酸盐9. 如图是无色溶液X发生化学反应时的颜色变化,无色溶液X是( )
 A、稀盐酸 B、稀硫酸 C、澄清石灰水 D、硫酸钠溶液10. 如图所示的密闭实验装置,当胶头滴管内的液体滴下与固体接触时,液面a比液面b高,但过一段时间U形管内的液面又回到持平的一组固体和液体组合是( )
A、稀盐酸 B、稀硫酸 C、澄清石灰水 D、硫酸钠溶液10. 如图所示的密闭实验装置,当胶头滴管内的液体滴下与固体接触时,液面a比液面b高,但过一段时间U形管内的液面又回到持平的一组固体和液体组合是( ) A、固体氢氧化钠和水 B、石灰石和稀盐酸 C、食盐和水 D、硝酸铵和水11. 如图装置可用于气体的收集、检验、除杂和体积的测量等,不能完成的实验是( )
A、固体氢氧化钠和水 B、石灰石和稀盐酸 C、食盐和水 D、硝酸铵和水11. 如图装置可用于气体的收集、检验、除杂和体积的测量等,不能完成的实验是( ) A、气体从a端通入,收集氧气 B、瓶内装有澄清石灰水,检验氧气中是否混有二氧化碳 C、瓶内装有氢氧化钠溶液。吸收一氧化碳中混有的二氧化碳 D、在b端接量筒,瓶内装满水,测量气体的体积12. 关于化学方程式CO2+C 2CO的叙述中,正确的是( )A、二氧化碳和碳等于一氧化碳 B、1个二氧化碳分子和1个碳原子生成2个一氧化碳 C、二氧化碳和碳在高温的条件下生成一氧化碳 D、每44份质量的二氧化碳和12份质量的碳在高温条件下生成86份质量的一氧化碳13. 小强同学在用氯酸钾制取氧气时,误把高锰酸钾当作二氧化锰加入了。下列对该实验的分析不正确的是( )A、反应中高锰酸钾起催化作用 B、产生的氧气质晟增加了 C、生成氧气的速度加快了 D、反应过程中,试管中的固体种类最多5种,最少3种14. 下列实验过程与图像描述相符合的一组是( )A、
A、气体从a端通入,收集氧气 B、瓶内装有澄清石灰水,检验氧气中是否混有二氧化碳 C、瓶内装有氢氧化钠溶液。吸收一氧化碳中混有的二氧化碳 D、在b端接量筒,瓶内装满水,测量气体的体积12. 关于化学方程式CO2+C 2CO的叙述中,正确的是( )A、二氧化碳和碳等于一氧化碳 B、1个二氧化碳分子和1个碳原子生成2个一氧化碳 C、二氧化碳和碳在高温的条件下生成一氧化碳 D、每44份质量的二氧化碳和12份质量的碳在高温条件下生成86份质量的一氧化碳13. 小强同学在用氯酸钾制取氧气时,误把高锰酸钾当作二氧化锰加入了。下列对该实验的分析不正确的是( )A、反应中高锰酸钾起催化作用 B、产生的氧气质晟增加了 C、生成氧气的速度加快了 D、反应过程中,试管中的固体种类最多5种,最少3种14. 下列实验过程与图像描述相符合的一组是( )A、 向一定温度下某饱和氯化钠溶液中加入氯化钾固体
B、
向一定温度下某饱和氯化钠溶液中加入氯化钾固体
B、 向等质量的镁、锌中加入稀硫酸
C、
向等质量的镁、锌中加入稀硫酸
C、 向稀盐酸中加入氢氧化钠溶液
D、
向稀盐酸中加入氢氧化钠溶液
D、 向盐酸和氯化铁的混合溶液中加入氢氧化钠溶液
15. 在一个密闭容器中,有a、b、c、d四种物质,反应前各物质的质量关系如图刻度纸所示(例如:d的质量为2g)。在一定条件下发生反应,反应结束后,再次测得各物质的质量变化,并通过刻度的移动来表示,且记录在同一张刻度纸上;刻度线Ⅰ向右移动9格;刻度线Ⅱ向左移动8格;刻度线Ⅲ向左移动8格。下列说法正确的是( )
向盐酸和氯化铁的混合溶液中加入氢氧化钠溶液
15. 在一个密闭容器中,有a、b、c、d四种物质,反应前各物质的质量关系如图刻度纸所示(例如:d的质量为2g)。在一定条件下发生反应,反应结束后,再次测得各物质的质量变化,并通过刻度的移动来表示,且记录在同一张刻度纸上;刻度线Ⅰ向右移动9格;刻度线Ⅱ向左移动8格;刻度线Ⅲ向左移动8格。下列说法正确的是( ) A、反应结束后c的质量为14g B、该反应可能为置换反应 C、a、b变化的质量比一定为9:17 D、a、d的相对分子质量之比一定为9:8
A、反应结束后c的质量为14g B、该反应可能为置换反应 C、a、b变化的质量比一定为9:17 D、a、d的相对分子质量之比一定为9:8二、填空题(本题共7小题,每空2分,共36分)
-
16.(1)、复学防疫,化学助力。过氧乙酸用于教室消毒,其化学性质不稳定,分解的化学方程式为:2C2H4O3=2C2H4O2+X↑,则X的化学式为 .(2)、汽车作为一种常见交通工具,已走进千家万户。汽车尾气(含有CO、NO等物质)是城市空气的污染物,治理的方法之一是在汽车的排气管上装一个催化转换器,使CO和NO反应,生成两种无毒气体,试写出CO与NO反应的化学方程式。17. 宇轩同学用如图总结NaOH的四类化学性质(即NaOH能够与四类物质发生化学反应)。
 (1)、为了验证性质③,该同学可选择的物质是(填序号)。该反应可以看到的实验现象是。
(1)、为了验证性质③,该同学可选择的物质是(填序号)。该反应可以看到的实验现象是。A.Na2CO3
B.CO2
C.FeCl3
D.Ba(NO3)2
(2)、依据反应④说明NaOH必须密封保存,否则在空气中要变质,其化学方程式为。18. 张勇和高民两位同学在课外做中和反应探究实验时,用一种黄花汁作为酸碱指示剂滴入一些液体中,实验记录如下表,结合表中信息回答:实验物质
盐酸
水
氯化钠溶液
肥皂水
氢氧化钠溶液
现象
红色
黄色
黄鎟
浅蓝色
蓝色
(1)、张勇在盛有氢氧化钠稀溶液的烧杯中滴入几滴黄花汁,再用胶头滴管将盐酸逐滴滴入烧杯中,边滴边用玻璃棒搅拌,当烧杯中的溶液刚好变为黄色时,说明盐酸和氢氧化钠刚好完全反应,溶液显性。(2)、向某无色溶液中滴入黄花汁,溶液变红色,则此溶液中一定不存在H+、Ag+、Cu2+、OH-、五种离子中的(填离子符号)。(3)、蚊子的口器会分泌出一种有机酸——蚁酸,人被蚊子叮咬,在家里自我治疗时可选用上表实验物质中的涂抹患处,可止痒、止痛、消肿。19. 硫酸和盐酸是实验室中两种重要的试剂,用途广泛。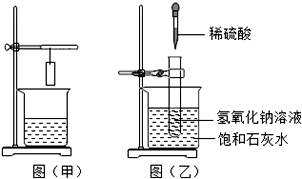 (1)、小柯将一张滤纸在某指示剂中浸泡后晾干,用蘸有氢氧化钠溶液的玻璃棒在上面写“化学”两字,立刻显红色。再将其悬挂于铁架台上,并在滤纸的下方(如图甲)放置一盛有某溶液的烧杯,立刻发现红色的字消失,则烧杯中的溶液可以是;(2)、探究酸碱反应的过程中是否伴随能量变化,小柯按乙图装置进行实验,其中澄清饱和石灰水的作用是;(3)、在稀盐酸的下列用途中,可以用稀硫酸代替的是 (填编号)。
(1)、小柯将一张滤纸在某指示剂中浸泡后晾干,用蘸有氢氧化钠溶液的玻璃棒在上面写“化学”两字,立刻显红色。再将其悬挂于铁架台上,并在滤纸的下方(如图甲)放置一盛有某溶液的烧杯,立刻发现红色的字消失,则烧杯中的溶液可以是;(2)、探究酸碱反应的过程中是否伴随能量变化,小柯按乙图装置进行实验,其中澄清饱和石灰水的作用是;(3)、在稀盐酸的下列用途中,可以用稀硫酸代替的是 (填编号)。①金凤表面除锈
②实验室利用它和块状大理石制取CO2
③除去NaCl中的少量NaOH
④制造药物氯化锌
20. 物质的结构决定性质,性质反映结构。据此回答下列问题。
 (1)、氢氧化钠溶液(NaOH)和氢氧化钙溶液[Ca(OH)2]具有相似的化学性质,原因是它们在电离时都产生了。(2)、氢氧化钠溶液和氢氧化钙溶液,为鉴别它们,小柯设计了如图四种方案(每种方案的两支试管中事先分别加入等量的上述两种碱),其中可行的方案有(填字母)。21. 小明同学在验证稀硫酸性质时用到了有毒的BaCl,进行如下实验,回答下列问题:
(1)、氢氧化钠溶液(NaOH)和氢氧化钙溶液[Ca(OH)2]具有相似的化学性质,原因是它们在电离时都产生了。(2)、氢氧化钠溶液和氢氧化钙溶液,为鉴别它们,小柯设计了如图四种方案(每种方案的两支试管中事先分别加入等量的上述两种碱),其中可行的方案有(填字母)。21. 小明同学在验证稀硫酸性质时用到了有毒的BaCl,进行如下实验,回答下列问题:
 (1)、步骤①中发生反应的化学方程式:。(2)、下列说法中,正确的是 。A、a试管中的液体可直接干燥CO2气体 B、将b试管中混合物过滤,滤液可用于鉴别Na2SO4和Hg(NO2)2两种无色液体 C、若向c试管中加入足量稀盐酸,沉淀全部溶解且有气泡产生 D、滤液d与适量的石灰水混合可制取NaOH溶液 E、理论上,滤渣e可用于医疗上的“钡餐”检查22. 一定条件下,2A+B=2C的反应中,若8g物质A和一定质量的B恰好完全反应生成72gC,则物质B的质量为;若B的相对分子质量为32,则A的相对分子质量为 , C的化学式可能为。
(1)、步骤①中发生反应的化学方程式:。(2)、下列说法中,正确的是 。A、a试管中的液体可直接干燥CO2气体 B、将b试管中混合物过滤,滤液可用于鉴别Na2SO4和Hg(NO2)2两种无色液体 C、若向c试管中加入足量稀盐酸,沉淀全部溶解且有气泡产生 D、滤液d与适量的石灰水混合可制取NaOH溶液 E、理论上,滤渣e可用于医疗上的“钡餐”检查22. 一定条件下,2A+B=2C的反应中,若8g物质A和一定质量的B恰好完全反应生成72gC,则物质B的质量为;若B的相对分子质量为32,则A的相对分子质量为 , C的化学式可能为。三、实验探究题(本题共4小题,年空3分,共39分)
-
23. 用如图装置进行实验。
 (1)、反应后电子秤示数变小的原因是。(2)、实验中如若装置不变,下列各 组药品不可用于验证质量守恒定律的是;
(1)、反应后电子秤示数变小的原因是。(2)、实验中如若装置不变,下列各 组药品不可用于验证质量守恒定律的是;A.硫酸铜溶液与铁钉
B.水与蔗糖
C.过氧化氢与二氧化锰
(3)、通过以上实验探究,你认为使用镁条在空气中燃烧来验证质量守恒定律应在(填“敞口”或“密闭”)容器中进行。24. 实验室制取气体时所需的一些装置如图所示,请回答下列问题: (1)、写出装置图中仪器名称:③。(2)、实验室里用石灰石和稀盐酸制取二氧化碳气体,其选用的制取装置为(填字母)。(3)、选择气体收集方法时,气体的下列性质:①颜色②密度③溶解性 ④可燃性,必须考虑的是 (填序号)。25. 小红在探究碱的化学性质时,将稀盐酸滴入到氢氧化钠溶液中,意外地发现有气泡产生,她认为氢氧化钠溶液已经变质。
(1)、写出装置图中仪器名称:③。(2)、实验室里用石灰石和稀盐酸制取二氧化碳气体,其选用的制取装置为(填字母)。(3)、选择气体收集方法时,气体的下列性质:①颜色②密度③溶解性 ④可燃性,必须考虑的是 (填序号)。25. 小红在探究碱的化学性质时,将稀盐酸滴入到氢氧化钠溶液中,意外地发现有气泡产生,她认为氢氧化钠溶液已经变质。[提出问题]变质后的氢氧化钠溶液中的溶质是什么?
[猜想假设]小红对变质后的氢氧化钠溶液中的溶质成分做出了两种猜想:
猜想一:Na2CO3
猜想二:NaOH和Na2CO3
[实验设计]为了验证上述猪想哪个正确,小红设计了如下方案:取少最氢氧化钠溶液样品于试管中,滴加几滴无色酚酞溶液,观察溶液颜色的变化可以得出结论.
小敏认为小红的实验方案不合理,理由是。
[实验与结论]小敏另外设计实验方案并进行了探究,请你帮她完成下面的实验报告:
实验步骤
实验现象
结论
步骤Ⅰ:取少量氢氧化钠溶液样品于试管中,向其中滴加过量的氯化钙溶液并振荡
有白色沉淀产生
猜想一正确
步骤2:将步骤Ⅰ试管中的混合物过滤,。
26. 我们接触过的有些化学反应是无明显现象的。如图三个实验都是通过滴加其他试剂的方法,使之产生明显的现象,以证明反应确实发生了。请回答下列问题:
 (1)、实验甲中能证明反应发生的现象是溶液由 色变为无色。(2)、实验乙中要证明反应的确发生了,应选用的酸碱指示剂是。(3)、小明同学选用甲反应后的溶液,滴入NaOH和CO2反应后的丙试管中,观察到先有气泡产生,后有白色沉淀生成。由此既证明了氢氧化钠溶液能与二氧化碳反应,又推断出甲试管反应后溶液中含有的溶质是(除指示剂外):请写出丙试管中气泡产生的化学方程式:。
(1)、实验甲中能证明反应发生的现象是溶液由 色变为无色。(2)、实验乙中要证明反应的确发生了,应选用的酸碱指示剂是。(3)、小明同学选用甲反应后的溶液,滴入NaOH和CO2反应后的丙试管中,观察到先有气泡产生,后有白色沉淀生成。由此既证明了氢氧化钠溶液能与二氧化碳反应,又推断出甲试管反应后溶液中含有的溶质是(除指示剂外):请写出丙试管中气泡产生的化学方程式:。四、解答题(本题共7小题,第29小题4分,第27、30小题各6分,第28小题10分,第31、32、33小题各8分,共50分)
-
27. “青团”是宁波的一种传统食物。在“青团”制作过程中,需要往糯米粉中添加艾草(或艾草汁)。艾草含有侧柏莲酮芳香油( C10H10O),侧柏莲酮芳香油是一种淡黄色液体,具有香脂香气,所以“青团”具有独特风味。(1)、一个侧柏莲酮芳香油分子中碳、氢、氧原子个数比是。(2)、7.3g侧柏莲桐芳香油中碳元素的质量g。(3)、侧柏莲桐芳香油在氧气中完全燃烧的产物是。28. 某兴趣小组按如图所示流程制取氧气,并回收提纯氯化钾和二氧化锰。回答下列问题:
 (1)、写出按上述方法制取氧气的化学方程式: , 经计算理论上可制得氧气的质量是 g;(2)、固体2的成分是 , 质量为g;(3)、在回收提纯的过程中需要控制水的用量,原因有 (填标号)。
(1)、写出按上述方法制取氧气的化学方程式: , 经计算理论上可制得氧气的质量是 g;(2)、固体2的成分是 , 质量为g;(3)、在回收提纯的过程中需要控制水的用量,原因有 (填标号)。A.保证所得溶液无色透明
B.保证固体1可溶物全部溶解
C.节约能源
29. 清代医学著作《本草纲目拾遗》中“强水”的条目下写到“性最烈,能蚀五金”。“强水”中有硝酸,“五金”是指金、银、铜、铁、锡。其中铜和稀硝酸反应的化学方程式为:3Cu+8HNO3=3Cu(NO3)2+2X↑+4H2O(1)、X 的化学式为。(2)、19.2 克铜完全反应最多可生成Cu(NO3)2多少克?30. 某化学兴趣小组,为了测定黄铜(由铜、锌组成)样品中锌的含量,称取样品10克于烧杯中,向其中加入25克稀硫酸至恰好完全反应,反应后烧杯中物质的总质量为34.9克,求:(1)、产生氢气的质量是 g。(2)、样品中锌的质量分数是多少?31. 将氯化钠和氯化铁的固体混合物40g完全溶于101.4g水中形成溶液,再将100g一定溶质质量分数的氢氧化钠溶液分5次加入到该溶液中,充分反应后,测得的实验数据如下表所示:[提示:化学方程式为FeCl3+3NaOH=3NaCl+Fe(OH)3↓]实验次数
1
2
3
4
5
加入氢氧化钠溶液的质量/g
20
20
20
220
20
共生成沉淀的质量/g
5.35
10.7
m
21.4
21.4
求:
(1)、表中m的值为。(2)、原混合物中氯化铁的质量为。(3)、恰好完全反应时,所得溶液的溶质质量分数是多少?(写出计算过程,结果精确到0.1%)32. 含CuCl2和HCl的100g混合溶液中,逐滴加入溶质质量分数为10%的NaOH溶液,参加反应的NaOH溶液质量与生成沉淀质量关系如图。据图回答: (1)、整个反应过程中,离子个数不变。(2)、P点溶液中的溶质是。(3)、m1为多少?(要求写出具体的解题过程)33. 向Ba(OH)2溶液中先滴加一定量CuSO4溶液,直至沉淀质量为m克,再不断滴加H2SO4溶液。整个过程中,产生沉淀的质量与加入溶液的质量关系如图所示。
(1)、整个反应过程中,离子个数不变。(2)、P点溶液中的溶质是。(3)、m1为多少?(要求写出具体的解题过程)33. 向Ba(OH)2溶液中先滴加一定量CuSO4溶液,直至沉淀质量为m克,再不断滴加H2SO4溶液。整个过程中,产生沉淀的质量与加入溶液的质量关系如图所示。 (1)、a点对应溶液pH(填“>”“=”或“<" )7。(2)、取c点对应的溶液,不断滴加NaOH溶液,观察到的现象是 。(3)、通过计算确定m的值。
(1)、a点对应溶液pH(填“>”“=”或“<" )7。(2)、取c点对应的溶液,不断滴加NaOH溶液,观察到的现象是 。(3)、通过计算确定m的值。