河南省开封市五县2022-2023学年高一上学期第一次月考联考化学试题
试卷更新日期:2022-10-14 类型:月考试卷
一、单选题
-
1. 化学与生活、社会发展息息相关,下列有关说法错误的是( )A、“青蒿一握,以水二升渍,绞取汁”,诗句中体现的屠呦呦对青蒿素的提取属物理变化 B、“墨滴无声入水惊,如烟袅袅幻形生”中的“墨滴”具有胶体的性质 C、石墨与“嫦娥五号”卫星所用的含碳量90%以上的碳纤维互为同素异形体 D、“朝坛雾卷,曙岭烟沉”,雾有丁达尔效应是因为胶体粒子对光有散射作用2. 下列实验操作能达到实验目的是( )A、除去NaCl固体中的少量 , 应将固体溶解后蒸发结晶 B、温度计被打破,洒在地面上的水银可以用水冲洗 C、配制浓和浓的混酸时,将浓慢慢加到浓中,并及时搅拌 D、向沸水中逐滴加入饱和氯化铁溶液并继续加热搅拌可得到氢氧化铁胶体3. 下列关于纯净物、混合物、电解质和非电解质分类正确的一组是( )
纯净物
混合物
电解质
非电解质
A
盐酸
天然气
硫酸
干冰
B
氨水
蓝矾
苛性钾
三氧化硫
C
熟石灰
蔗糖溶液
硫酸钡
氨气
D
硫酸
铝合金
氯化钠
氢气
A、A B、B C、C D、D4. 下列电离方程式错误的是( )A、在溶液中的电离方程式为 B、在水溶液中的电离方程式为 C、在熔融状态下的电离方程式为(熔融) D、的电离方程式为5. 一定温度下,溶液导电能力(I)变化如图所示,下列说法正确的是( ) A、图1表示向溶液中加入一定物质的量浓度的溶液至过量 B、图2表示向NaOH溶液中通入少量 C、图3表示向醋酸溶液中加入NaOH固体至过量 D、图4表示向溶液通入少量HCl气体6. 下列说法正确的是有几个( )
A、图1表示向溶液中加入一定物质的量浓度的溶液至过量 B、图2表示向NaOH溶液中通入少量 C、图3表示向醋酸溶液中加入NaOH固体至过量 D、图4表示向溶液通入少量HCl气体6. 下列说法正确的是有几个( )①易溶于水,故可用作净水剂
②盐酸和食醋既是化合物又是酸
③与的水溶液能导电,所以、是电解质
④碱性氧化物一定是金属氧化物
⑤不锈钢和目前流通的硬币都是合金
⑥强酸溶液的导电性一定强于弱酸溶液的导电性
⑦向某溶液中加入稀硫酸生成无色无味的气体,说明原溶液中有
A、2个 B、3个 C、4个 D、5个7. 下列液体中,不会出现丁达尔效应的是( )①鸡蛋清溶液 ②酒精 ③淀粉溶液 ④蔗糖溶液 ⑤FeCl3溶液 ⑥肥皂水 ⑦泥水
A、④⑤ B、②④⑤⑦ C、②④⑥ D、①③④⑦8. 最近,科学家开发出一种低成本光伏材料——蜂窝状石墨烯。生产原理是:(石墨烯),然后除去 , 即可制得蜂窝状石墨烯。下列说法错误的是( )。A、自然界中碳元素有游离态和化合态两种存在形式 B、石墨烯与金刚石互为同素异形体 C、该生产石墨烯的反应不属于置换反应 D、属于碱性氧化物,CO属于酸性氧化物,属于盐9. 下列反应不属于氧化还原反应的是( )A、 B、 C、 D、10. A、B、C、D、E中都含有同一种元素,它们之间的相互转化关系如图所示,其中所含的相同元素是( ) A、铜 B、碳 C、铁 D、钙11. 下列各组中两稀溶液间的反应可以用同一个离子方程式表示的是( )A、溶液(足量)与溶液;溶液(足量)与溶液 B、溶液与KOH溶液;盐酸与NaOH溶液 C、溶液与溶液;溶液与溶液 D、NaHCO3溶液与过量溶液;溶液与溶液12. 某溶液中含有较大量的Cl-、 、OH-三种阴离子,如果只取一次该溶液就能够分别将3种阴离子依次检验出来。下列实验操作的操作顺序中, 正确的是( )
A、铜 B、碳 C、铁 D、钙11. 下列各组中两稀溶液间的反应可以用同一个离子方程式表示的是( )A、溶液(足量)与溶液;溶液(足量)与溶液 B、溶液与KOH溶液;盐酸与NaOH溶液 C、溶液与溶液;溶液与溶液 D、NaHCO3溶液与过量溶液;溶液与溶液12. 某溶液中含有较大量的Cl-、 、OH-三种阴离子,如果只取一次该溶液就能够分别将3种阴离子依次检验出来。下列实验操作的操作顺序中, 正确的是( )①滴加Mg(NO3)2溶液 ②过滤 ③滴加AgNO3溶液 ④滴加Ba(NO3)2溶液
A、①②④②③ B、④②③②① C、①②③②④ D、④②①②③13. 在给定的四种溶液中加入以下各种离子,能在原溶液中大量共存的是( )A、使石蕊显蓝色的溶液:、、、 B、25℃的溶液:、、、 C、含的溶液中:、、、 D、与铁反应产生氢气的溶液:、、、14. 下列离子方程式中正确的是( )A、与溶液反应: B、溶液中滴加至溶液呈中性: C、向NaOH溶液中加入过量溶液,有白色沉淀生成: D、溶液与NaOH溶液反应:15. 日常生话中的许多现象与化学反应有关,下列现象与氧化还原反应无关的是( )A、铝锅表面生成致密的氧化膜 B、铁制菜刀生锈 C、大理石雕像被酸雨腐蚀毁坏 D、铜铸塑像上出现铜绿[Cu2(OH)2CO3]16. 某溶液中只含有、、、四种离子,已知前三种离子的个数比为1:3:4,则溶液中和的离子个数比为( )A、1:2 B、3:4 C、1:3 D、3:217. 下列氧化还原反应中,电子转移的方向和数目均正确的是( )A、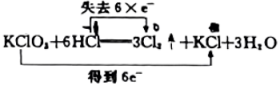 B、
B、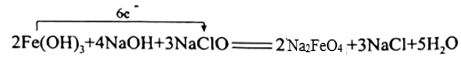 C、
C、 D、
D、 18. 甲、乙、丙、丁分别是Na2CO3、AgNO3、BaCl2、盐酸四种无色溶液中的一种,它们两两反应后的现象如下:甲+丁→沉淀;丁+丙→沉淀;甲+丙→沉淀;丙+乙→沉淀;甲+乙→无色无味气体。则甲、乙、丙、丁四种溶液依次是( )A、Na2CO3、BaCl2、AgNO3、HCl B、HCl、Na2CO3、AgNO3、BaCl2 C、HCl、BaCl2、AgNO3、Na2CO3 D、Na2CO3、HCl、AgNO3、BaCl2
18. 甲、乙、丙、丁分别是Na2CO3、AgNO3、BaCl2、盐酸四种无色溶液中的一种,它们两两反应后的现象如下:甲+丁→沉淀;丁+丙→沉淀;甲+丙→沉淀;丙+乙→沉淀;甲+乙→无色无味气体。则甲、乙、丙、丁四种溶液依次是( )A、Na2CO3、BaCl2、AgNO3、HCl B、HCl、Na2CO3、AgNO3、BaCl2 C、HCl、BaCl2、AgNO3、Na2CO3 D、Na2CO3、HCl、AgNO3、BaCl2二、填空题
-
19. 现有下列物质:①草木灰②③熔融④胶体⑤液态氯化氢⑥稀硫酸⑦溶液⑧金刚石⑨氨水⑩酒精⑪⑫澄清石灰水。请将序号分别填入下面的横线处:(1)、上述状态下可导电的是 , 属于电解质的是 , 属于非电解质的是 , 属于纯净物的是 , 属于盐的是。(2)、⑦与少量的⑫的离子反应方程式是。(3)、写出物质③溶于水的电离方程式:。(4)、将过量⑪通入⑫溶液中的现象是。(5)、将⑦加入溶液中出现红褐色沉淀和无色无味气体的离子方程式。
三、综合题
-
20. 现有甲、乙、丙三名同学分别进行胶体的制备实验。
甲同学:向的溶液中加少量NaOH溶液。
乙同学:向25mL沸水中逐滴加入5~6滴饱和溶液,继续煮沸至溶液呈红褐色,停止加热。
丙同学:直接加热饱和溶液。
试回答下列问题
(1)、其中操作正确的同学是 , 反应的化学方程式为。(2)、证明有胶体生成的方法是。(3)、将其装入U型管内,用石墨棒做电极,接通直流电源,通电一段时间后发现阴极附近颜色 , 这表明。(4)、向其中逐滴加入过量稀硫酸,现象是。(5)、可用如图所示的装置除去胶体中的杂质离子来提纯胶体,实验过程中需不断更换烧杯中的蒸馏水。更换蒸馏水若干次后,取少量烧杯中的液体,向其中加入溶液,若(填实验现象),则说明该胶体中的杂质离子已经完全除去。 21. 某无色透明溶液中只可能含有、、、、、、、中的一种或几种,对其进行如下实验操作:(1)、不做任何实验就可以肯定,原溶液中不存在的离子是。(2)、取少量溶液,滴加无色酚酞试剂,酚酞变红;说明原溶液中肯定存在的离子是。(3)、另取少量溶液,加入足量溶液,产生白色沉淀;再加入足量盐酸,沉淀部分溶解,并有无色气体生成:说明原溶液中肯定存在的离子是 , 肯定不存在。(4)、将(3)所得混合物过滤,向滤液中加入溶液,有白色沉淀生成。(填能/不能)说明原溶液中含 , 原因是:。22. 某无色溶液中含有K+、Cl-、OH-、、 , 为了检验除OH-外的其他所有阴离子,拟用盐酸、硝酸、硝酸银溶液、氯化钡溶液、澄清石灰水等试剂(每种试剂仅使用一次),设计如图实验步骤,并记录相关现象:
21. 某无色透明溶液中只可能含有、、、、、、、中的一种或几种,对其进行如下实验操作:(1)、不做任何实验就可以肯定,原溶液中不存在的离子是。(2)、取少量溶液,滴加无色酚酞试剂,酚酞变红;说明原溶液中肯定存在的离子是。(3)、另取少量溶液,加入足量溶液,产生白色沉淀;再加入足量盐酸,沉淀部分溶解,并有无色气体生成:说明原溶液中肯定存在的离子是 , 肯定不存在。(4)、将(3)所得混合物过滤,向滤液中加入溶液,有白色沉淀生成。(填能/不能)说明原溶液中含 , 原因是:。22. 某无色溶液中含有K+、Cl-、OH-、、 , 为了检验除OH-外的其他所有阴离子,拟用盐酸、硝酸、硝酸银溶液、氯化钡溶液、澄清石灰水等试剂(每种试剂仅使用一次),设计如图实验步骤,并记录相关现象: (1)、试剂(化学式):①;②;③;⑤;(2)、现象1中白色沉淀为(化学式);(3)、产生现象2的离子方程式是:;(4)、分离现象2中白色沉淀的方法 , 对该沉淀进行称量前需要进行、处理。
(1)、试剂(化学式):①;②;③;⑤;(2)、现象1中白色沉淀为(化学式);(3)、产生现象2的离子方程式是:;(4)、分离现象2中白色沉淀的方法 , 对该沉淀进行称量前需要进行、处理。
-