云南省昭通市永善、绥江县2021-2022学年高二上学期期末考试化学试题
试卷更新日期:2022-10-10 类型:期末考试
一、单选题
-
1. 熟悉元素周期表有助很好理解化学知识。原子序数为x的元素位于周期表中的第IIA族,则原子序数为x+1的元素不可能处在( )A、IIIA族 B、IA族 C、镧系 D、IIIB族2. 下列说法正确的是( )A、明矾常用作净水剂,是因为明矾具有杀菌消毒的功能 B、从碘水中萃取碘,可以选择裂化汽油作萃取剂 C、“酸雨”“臭氧层空洞”“光化学烟雾”都可能与氮氧化物有关 D、利用工业废水灌溉农作物实现“水循环”3. 短周期元素X、Y、Z、W、Q在元素周期表中的位置如图所示,其中W的气态氢化物摩尔质量为34g·mol-1 , Y的最低价氢化物为非电解质,则下列说法正确的是( )
X
Y
Z
W
Q
A、Na与Y能形成化合物Na2Y2 , 且与水反应后溶液呈碱性 B、Q元素氧化物的水化物的酸性比Y元素氧化物的水化物的酸性强 C、Z的最高价氧化物可与氢氧化钠反应 D、阴离子还原性: W<Q4. 关于下列反应的离子方程式正确的是( )A、向稀硝酸中滴加少量亚硫酸钠溶液:+2H+=SO2↑+H2O B、向碳酸钠溶液中滴入少量硫酸:+2H+=CO2↑+H2O C、向溴化亚铁溶液中通入少量氯气:2Fe2++Cl2=2Fe3++2Cl- D、向碳酸氢铵溶液中加入足量氢氧化钠溶液:+OH-=NH3·H2O5. 可逆反应2NO2 2NO+O2在体积固定的绝热密闭容器中进行,反应达到平衡状态的标志是 ( )①单位时间内生成n mol的O2 , 同时进生成2n mol的NO2
②单位时间内生成n mol的O2 , 同时生成2n mol的NO
③用NO2、NO、O2的物质的量浓度变化表示的反应速率之比为2:2: 1
④混合气体的密度不再改变
⑤混合气体的颜色不再改变
⑥密闭容器中的温度不再改变
A、①⑤ B、①⑤⑥ C、②④ D、以上全部6. 下列说法正确的是( )A、苯甲酸重结晶实验中粗苯甲酸溶解后还要加点水,目的是减少过滤时苯甲酸的损失 B、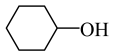 的核磁共振氢谱中有4种峰
C、石油是混合物,其分馏产品汽油为纯净物
D、苯中滴加浓溴水,充分振荡后溴水层褪色,是因为苯与溴水中的溴发生了加成反应
7. 下列反应只能得到一种有机物的是( )A、丙烯与HCl发生反应 B、在FeBr3催化下,甲苯与液溴反应 C、乙苯与酸性高锰酸钾溶液反应 D、甲苯在光照条件下与Cl2反应8. 王浆酸是从蜂王浆中分离出的一种有机酸,它有很好的杀菌、抗癌、抗放射及强化机体、增强免疫力的作用,其结构如图所示。下列有关王浆酸的说法错误的是( )
的核磁共振氢谱中有4种峰
C、石油是混合物,其分馏产品汽油为纯净物
D、苯中滴加浓溴水,充分振荡后溴水层褪色,是因为苯与溴水中的溴发生了加成反应
7. 下列反应只能得到一种有机物的是( )A、丙烯与HCl发生反应 B、在FeBr3催化下,甲苯与液溴反应 C、乙苯与酸性高锰酸钾溶液反应 D、甲苯在光照条件下与Cl2反应8. 王浆酸是从蜂王浆中分离出的一种有机酸,它有很好的杀菌、抗癌、抗放射及强化机体、增强免疫力的作用,其结构如图所示。下列有关王浆酸的说法错误的是( ) A、分子式为C10H18O3 B、1mol 王浆酸最多能中和2mol NaOH C、一定条件下能发生取代反应和氧化反应 D、1mol王浆酸只能与1mol H2发生加成反应9. 下列说法错误的是( )A、护肤品中常含有机醇等强亲水性物质,乙二醇可用于汽车防冻液 B、石油的裂化、煤的液化、海带中提碘等都必须通过化学变化实现 C、蒸馏“地沟油”可以获得汽油 D、聚乳酸、聚乙烯琥珀酸酯等可降解产品的广泛使用将有效缓解白色污染10. 下列实验方案中,操作正确且可以达到实验目的的是( )
A、分子式为C10H18O3 B、1mol 王浆酸最多能中和2mol NaOH C、一定条件下能发生取代反应和氧化反应 D、1mol王浆酸只能与1mol H2发生加成反应9. 下列说法错误的是( )A、护肤品中常含有机醇等强亲水性物质,乙二醇可用于汽车防冻液 B、石油的裂化、煤的液化、海带中提碘等都必须通过化学变化实现 C、蒸馏“地沟油”可以获得汽油 D、聚乳酸、聚乙烯琥珀酸酯等可降解产品的广泛使用将有效缓解白色污染10. 下列实验方案中,操作正确且可以达到实验目的的是( )序号
实验目的
实验操作和现象
①
除去苯中混有的苯酚
向溶液中滴加少量浓溴水充分反应后过滤弃去沉淀
②
检验CH3CH2Br中存在的溴元素
将CH3CH2Br与NaOH溶液共热,冷却后,取出上层水
溶液,加入AgNO3溶液,观察是否产生淡黄色沉淀
③
蔗糖未水解
向20%蔗糖溶液中加入少量稀H2SO4 , 加热;再加入银
氨溶液;未出现银镜
④
证明溴乙烷发生消去反应有乙烯生成
向试管中加入适量的溴乙烷和NaOH的乙醇溶液,加热,
将反应产生的气体通入溴水中,溴水褪色
⑤
检验绿茶中是否含有酚类物质
向茶水中滴加FeCl3溶液
⑥
实验室制备乙酸乙酯
向试管中依次加入浓硫酸、乙醇、乙酸和碎瓷片,加热
A、②③④⑤ B、④⑤ C、①⑤⑥ D、②④⑤11. 下列说法正确的是( )A、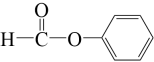 属于醛类,官能团为
B、
属于醛类,官能团为
B、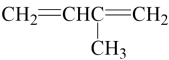 的名称为甲基二丁烯
C、
的名称为甲基二丁烯
C、 与
与 含有相同的官能团,互为同系物
D、
含有相同的官能团,互为同系物
D、 的名称为乙基丁烯
12. 当用卤化铁做催化剂时,卤素与苯及苯的同系物作用,只有苯环上的氢原子被卤素原子取代。分子式为C9H12的苯的同系物在有溴化铁存在时,与溴单质反应所得到的一溴代物种类最多的是( )A、丙苯 B、邻-甲乙苯 C、对-甲乙苯 D、1, 2, 4-三甲苯13. 化合物X是一种医药中间体,其结构简式如图所示。下列有关化合物X的说法正确的是( )
的名称为乙基丁烯
12. 当用卤化铁做催化剂时,卤素与苯及苯的同系物作用,只有苯环上的氢原子被卤素原子取代。分子式为C9H12的苯的同系物在有溴化铁存在时,与溴单质反应所得到的一溴代物种类最多的是( )A、丙苯 B、邻-甲乙苯 C、对-甲乙苯 D、1, 2, 4-三甲苯13. 化合物X是一种医药中间体,其结构简式如图所示。下列有关化合物X的说法正确的是( ) A、分子式为C16H12O4 B、分子中两个苯环一定处于同一平面 C、在酸性条件下水解,水解产物有2种 D、不能与饱和Na2CO3溶液反应14. 设NA为阿伏加德罗常数的值,下列说法正确的是( )A、将1 mol SO2和0.5 mol O2混合后充分反应,生成SO3的分子数为NA B、1 L0.5 mol/LNH4NO3溶液中含N原子的总数为NA C、0.1 mol Cl2通入足量水中,充分反应后,转移的电子数为0.1NA D、1 L0.1 mol/L的H2SO3溶液中含H+的数目为0.2NA15. 下列说法正确的是( )A、天然橡胶
A、分子式为C16H12O4 B、分子中两个苯环一定处于同一平面 C、在酸性条件下水解,水解产物有2种 D、不能与饱和Na2CO3溶液反应14. 设NA为阿伏加德罗常数的值,下列说法正确的是( )A、将1 mol SO2和0.5 mol O2混合后充分反应,生成SO3的分子数为NA B、1 L0.5 mol/LNH4NO3溶液中含N原子的总数为NA C、0.1 mol Cl2通入足量水中,充分反应后,转移的电子数为0.1NA D、1 L0.1 mol/L的H2SO3溶液中含H+的数目为0.2NA15. 下列说法正确的是( )A、天然橡胶 和杜仲胶
和杜仲胶 互为同分异构体
B、
互为同分异构体
B、 与
与 属于同系物
C、合成
属于同系物
C、合成 的单体为乙烯和2-丁烯
D、
的单体为乙烯和2-丁烯
D、 是由苯酚和甲醛发生加成反应后的产物脱水缩合而成
16. 下列有机物关系判断正确的是( )A、熔点: 2, 2-二甲基戊烷>2, 3-二甲基丁烷>正戊烷>新戊烷>丙烷 B、密度: CCl4>H2O>CHCl3>1-戊烯>苯 C、同质量的物质燃烧耗O2量:丙炔>乙烷>乙烯>乙炔>甲烷 D、同物质的量物质燃烧耗O2量:己烷>环己烷>苯>苯甲酸17. 一定量的乙醇在氧气不足的情况下燃烧,得到CO2、CO和H2O的总质量为26.8g,其中H2O的质量为10.8g,则CO的质量是( )A、1.4g B、2.8g C、4.4g D、在2. 8g和4.4g之间18. 下列醇类物质中既能发生消去反应,又能发生催化氧化反应生成醛类的物质是( )A、
是由苯酚和甲醛发生加成反应后的产物脱水缩合而成
16. 下列有机物关系判断正确的是( )A、熔点: 2, 2-二甲基戊烷>2, 3-二甲基丁烷>正戊烷>新戊烷>丙烷 B、密度: CCl4>H2O>CHCl3>1-戊烯>苯 C、同质量的物质燃烧耗O2量:丙炔>乙烷>乙烯>乙炔>甲烷 D、同物质的量物质燃烧耗O2量:己烷>环己烷>苯>苯甲酸17. 一定量的乙醇在氧气不足的情况下燃烧,得到CO2、CO和H2O的总质量为26.8g,其中H2O的质量为10.8g,则CO的质量是( )A、1.4g B、2.8g C、4.4g D、在2. 8g和4.4g之间18. 下列醇类物质中既能发生消去反应,又能发生催化氧化反应生成醛类的物质是( )A、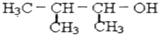 B、
B、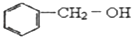 C、
C、 D、
D、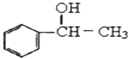 19. 茶是我国的传统饮品,茶叶中含有的茶多酚可以替代食品添加剂中对人体有害的合成抗氧化剂,用于多种食品保鲜等,如图所示是茶多酚中含量最高的一种儿茶素A的结构简式,下列关于这种儿茶素A的有关叙述正确的是( )
19. 茶是我国的传统饮品,茶叶中含有的茶多酚可以替代食品添加剂中对人体有害的合成抗氧化剂,用于多种食品保鲜等,如图所示是茶多酚中含量最高的一种儿茶素A的结构简式,下列关于这种儿茶素A的有关叙述正确的是( )
①分子式为C15H14O7
②1mol儿茶素A与足量的浓溴水反应,最多消耗Br2 4mol
③1mol儿茶素A在一定条件下最多能与6mol H2加成
④等质量的儿茶素A分别与足量的金属钠和氢氧化钠反应消耗金属钠和氢氧化钠的物质的量之比为1:1
A、①②③ B、②③④ C、①③④ D、①②④20. 有下列8种物质:①丁烷 ②丙烯 ③1-戊炔 ④苯 ⑤甲苯 ⑥乙烯与溴的反应产物 ⑦聚丙烯 ⑧环己烯。其中既不能使酸性KMnO4溶液褪色,也不能与溴水反应使溴水褪色的是( )A、①②③⑤ B、④⑥⑦⑧ C、①④⑥⑦ D、②③⑤⑧二、综合题
-
21. 溴乙烷在不同溶剂中与NaOH发生不同类型的反应,生成不同的反应产物。
某同学依据溴乙烷的性质,用如图实验装置(铁架台、酒精灯略)验证取代反应和消去反应的产物,请你一起参与探究。

实验操作Ⅰ:在试管中加入5 mL 1 mol/L NaOH溶液和5 mL 溴乙烷,振荡。
实验操作II:将试管如图固定后,水浴加热。
(1)、用水浴加热而不直接用酒精灯加热的原因是。(2)、观察到现象时,表明溴乙烷与NaOH溶液已完全反应。(3)、鉴定生成物中乙醇的结构,可用的波谱是。(4)、为证明溴乙烷在NaOH乙醇溶液中发生的是消去反应,在你设计的实验方案中,需要检验的是 , 检验的方法是(需说明:所用的试剂、简单的实验操作及预测产生的实验现象)。22. 有机物W~H有如图所示的转化关系。已知W、B为芳香族化合物,X为卤素原子,W 、A、B均能与NaHCO3溶液反应,A分子中有2个甲基,H分子中含有醛基且苯环上的取代基处于对位。
已知:

 。
。 请回答下列有关问题:
(1)、反应①、②分别属于反应、反应(填有机反应类型);A、B中均含有的含氧官能团的名称是。(2)、B的结构简式为 。(3)、反应②的化学方程式是。(4)、D L有机玻璃[(C5H8O2)n],反应④的化学方程式是。(5)、H有多种同分异构体,且满足下列3个条件:①遇FeCl3显紫色
②苯环上一取代物有两种
③除苯环外无其他环状结构
请写出符合条件的物质的结构简式:。
23. 以铝土矿(主要成分为Al2O3 , 含SiO2和Fe2O3等杂质)为原料制备耐高温陶瓷材料AlN和FeCl3·6H2O晶体的工艺流程如图所示: (1)、提高“酸溶”一步反应速率的方法有 (任意写出一种即可),滤渣I的主要成分是(填化学式)。(2)、向滤液I中加入过量NaOH溶液;发生的离子反应有H++OH-=H2O、Fe3++3OH-=Fe(OH)3↓和。(3)、在滤渣II中加入盐酸,经过蒸发浓缩、、、低温干燥, 获得FeCl3·6H2O晶体。(4)、已知X是一种有毒气体,写出高温制备AlN的化学方程式:。当制备AlN的反应中产生3.36 L(标准状况)气体X时,制得AlNg。
(1)、提高“酸溶”一步反应速率的方法有 (任意写出一种即可),滤渣I的主要成分是(填化学式)。(2)、向滤液I中加入过量NaOH溶液;发生的离子反应有H++OH-=H2O、Fe3++3OH-=Fe(OH)3↓和。(3)、在滤渣II中加入盐酸,经过蒸发浓缩、、、低温干燥, 获得FeCl3·6H2O晶体。(4)、已知X是一种有毒气体,写出高温制备AlN的化学方程式:。当制备AlN的反应中产生3.36 L(标准状况)气体X时,制得AlNg。